I.有人设想合成具有以下结构的烃分子:

(1)结构D显然是不可能合成的,原因是_______ 。
(2)在结构A的每两个碳原子之间插入一个CH2原子团,可以形成金刚烷的结构( )。写出金刚烷的分子式
)。写出金刚烷的分子式_______ ,其一氯代物有_______ 种。
(3)烃B的一种同分异构体是最简单的芳香烃,能证明该芳香烃中的化学键不是单双键交替排列的事实是_______ 。
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种。
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
(4)烃C的一种属于芳香烃的同分异构体是生产某塑料的单体,写出合成该塑料的化学方程式为_______ 。
II.研究有机物的官能团,完成下列对比实验。
(5)由实验①可知,与碳酸钙发生反应的官能团是_______ 。
(6)由实验②可知,CH3CH2OH与金属钠反应时_______ 键断裂。
(7)设计并完成实验③,比较CH3CH2OH中的O-H键与CH3CH2COOH中的O-H键的活性。请将试剂a和实验现象补充完整。

(1)结构D显然是不可能合成的,原因是
(2)在结构A的每两个碳原子之间插入一个CH2原子团,可以形成金刚烷的结构(
 )。写出金刚烷的分子式
)。写出金刚烷的分子式(3)烃B的一种同分异构体是最简单的芳香烃,能证明该芳香烃中的化学键不是单双键交替排列的事实是
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种。
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
(4)烃C的一种属于芳香烃的同分异构体是生产某塑料的单体,写出合成该塑料的化学方程式为
II.研究有机物的官能团,完成下列对比实验。
| 实验① | 实验② | |
| 实验 方案 | 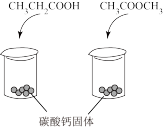 | 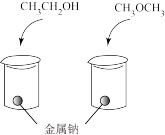 |
| 实验 现象 | 左侧烧杯内固体溶解,有无色气泡产生;右侧烧杯内无明显现象 | 左侧烧杯内有无色气泡产生;右侧烧杯内无明显现象 |
(6)由实验②可知,CH3CH2OH与金属钠反应时
(7)设计并完成实验③,比较CH3CH2OH中的O-H键与CH3CH2COOH中的O-H键的活性。请将试剂a和实验现象补充完整。
| 实验③ | |
| 实验方案 |  试剂a 试剂a |
| 实验现象 |
更新时间:2022-06-02 10:46:37
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
真题
解题方法
【推荐1】直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,最终生成硫酸钙。硫酸钙可在下图所示的循环燃烧装置的燃料反应器中与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧化碳,从而有利于二氧化碳的回收利用,达到减少碳排放的目的。
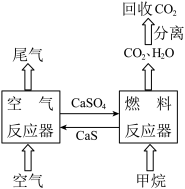
请回答下列问题:
(1)煤燃烧产生的烟气直接排放到空气中,引发的主要环境问题有__________。(填写字母编号)
(2)在烟气脱硫的过程中,所用的石灰石浆液在进入脱硫装置前,需通一段时间二氧化碳以增加其脱硫效率;脱硫时控制浆液的pH值,此时浆液含有的亚硫酸氢钙可以被氧气快速氧化生成硫酸钙。
①二氧化碳与石灰石浆液反应得到的产物为_____________ 。
②亚硫酸氢钙被足量氧气氧化生成硫酸钙的化学方程式为___________________ 。
(3)已知1 mol CH4在燃料反应器中完全反应生成气态水时吸收 160.1 kJ,1 mol CH4在氧气中完全燃烧生成气态水时放热802.3 kJ。写出空气反应器中发生的热化学方程式:___________________ 。
(4)回收的CO2与苯酚钠在一定条件反应生成有机物M,其化学式为C7H5O3Na,M经稀硫酸酸化后得到一种药物中间体N,N的结构简式为 。
。
①M的结构简式为__________________ 。
②分子中无—O—O—,醛基与苯环直接相连的N的同分异构体共有________ 种。

请回答下列问题:
(1)煤燃烧产生的烟气直接排放到空气中,引发的主要环境问题有__________。(填写字母编号)
| A.温室效应 | B.酸雨 | C.粉尘污染 | D.水体富营养化 |
①二氧化碳与石灰石浆液反应得到的产物为
②亚硫酸氢钙被足量氧气氧化生成硫酸钙的化学方程式为
(3)已知1 mol CH4在燃料反应器中完全反应生成气态水时吸收 160.1 kJ,1 mol CH4在氧气中完全燃烧生成气态水时放热802.3 kJ。写出空气反应器中发生的热化学方程式:
(4)回收的CO2与苯酚钠在一定条件反应生成有机物M,其化学式为C7H5O3Na,M经稀硫酸酸化后得到一种药物中间体N,N的结构简式为
 。
。①M的结构简式为
②分子中无—O—O—,醛基与苯环直接相连的N的同分异构体共有
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有机物N( )是一种常见的有机合成中间体,在生产中用途广泛。以有机物A为原料合成M和N的路线如下所示:
)是一种常见的有机合成中间体,在生产中用途广泛。以有机物A为原料合成M和N的路线如下所示:

已知:I. R-CH=CH2+HBr R-CH2-CH2Br
R-CH2-CH2Br
II. R-CH2-CN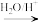 R-CH2-COOH
R-CH2-COOH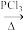

请回答下列问题:
(1)A分子中共面的原子数最多为________ 个,-CN的电子式为_______________ 。
(2)②的反应类型为________________ , E分子中所含官能团的名称为____________ ,G的结构简式为_____________________ 。
(3)写出反应⑤的化学方程式__________________________________________ ,写出M在酸性条件下水解的化学方程式_________________________________ 。
(4)D的同分异构体中,能发生银镜反应,且能与钠反应放出H2的共有______ 种,写出核磁共振氢谱有4组峰,且峰面积比为1:1:2:6的一种同分异构体的结构简式:____________________ 。
(5)结合信息,写出用E和乙醇为原料制备化合物N的合成路线:(其他试剂任选)_____________

 )是一种常见的有机合成中间体,在生产中用途广泛。以有机物A为原料合成M和N的路线如下所示:
)是一种常见的有机合成中间体,在生产中用途广泛。以有机物A为原料合成M和N的路线如下所示:
已知:I. R-CH=CH2+HBr
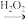 R-CH2-CH2Br
R-CH2-CH2BrII. R-CH2-CN
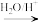 R-CH2-COOH
R-CH2-COOH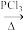

请回答下列问题:
(1)A分子中共面的原子数最多为
(2)②的反应类型为
(3)写出反应⑤的化学方程式
(4)D的同分异构体中,能发生银镜反应,且能与钠反应放出H2的共有
(5)结合信息,写出用E和乙醇为原料制备化合物N的合成路线:(其他试剂任选)

您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】物质J是一种具有生物活性的化合物。该化合物的合成路线如下:

已知:
① ;
;
②
回答下列问题:
(1)B中含氧官能团的名称为___________ 、___________ ;
(2)B→C、G→H的反应类型分别是___________ 、___________ ;
(3)C→D反应方程式为___________ ;
(4) 是一种重要的化工原料,其同分异构体中能够发生银镜反应的有
是一种重要的化工原料,其同分异构体中能够发生银镜反应的有___________ 种(考虑立体异构),其中核磁共振氢谱有3组峰,且峰面积之比为4∶1∶1的结构简式为________ 。
(5)I中的手性碳原子个数为___________ (连四个不同的原子或原子团的碳原子称为手性碳原子);
(6)参照上述合成路线,以 和
和 为原料,设计合成
为原料,设计合成 的路线
的路线________ (无机试剂任选)。

已知:
①
 ;
;②

回答下列问题:
(1)B中含氧官能团的名称为
(2)B→C、G→H的反应类型分别是
(3)C→D反应方程式为
(4)
 是一种重要的化工原料,其同分异构体中能够发生银镜反应的有
是一种重要的化工原料,其同分异构体中能够发生银镜反应的有(5)I中的手性碳原子个数为
(6)参照上述合成路线,以
 和
和 为原料,设计合成
为原料,设计合成 的路线
的路线
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平。现以A为主要原料合成F,其合成路线如下图所示。

(1)A分子中官能团的名称是____________ ,D中官能团的名称是________ 反应①的反应类型是___________ 反应。
(2)反应②的化学方程式是___________________________ 。
反应④的化学方程式是___________________________ 。
(3)E是常见的高分子材料,合成E的化学方程式是_____________________________ 。

(4)某同学用如右图所示的实验装置制取少量F。实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
① 实验开始时,试管甲中的导管不伸入液面下的原因是______________ 。
②上述实验中饱和碳酸钠溶液的作用是(填字母)________ 。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
③在实验室利用B和D制备F的实验中,若用1mol B和1mol D充分反应,__________ (能/不能)生成1mol F,原因是 __________________ 。

(1)A分子中官能团的名称是
(2)反应②的化学方程式是
反应④的化学方程式是
(3)E是常见的高分子材料,合成E的化学方程式是

(4)某同学用如右图所示的实验装置制取少量F。实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
① 实验开始时,试管甲中的导管不伸入液面下的原因是
②上述实验中饱和碳酸钠溶液的作用是(填字母)
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
③在实验室利用B和D制备F的实验中,若用1mol B和1mol D充分反应,
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】乙酸乙酯是日常生活中饮料、糖果中常使用的香料,聚丙烯酸乙酯是一种安全的化妆品粘合剂。它们均可用石油裂化和裂解得到的熔经来合成,合成路线如下图,其中有机物F的产量是衡量一个国家石油化工水平的标志,回答下列问题:
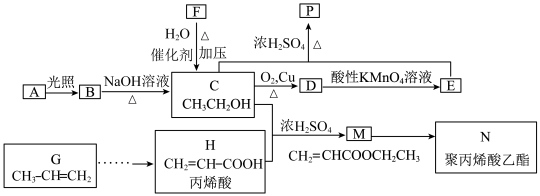
已知: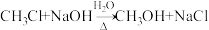
(1)F的名称为___________ ,B→C的反应类型是___________ ,H中所含官能团名称是___________ 。
(2)N的结构简式___________ 。
(3)鉴别C和E的常用试剂有___________ (写两种)。
(4)某同学用如图所示的实验装置利用C与E制取P,实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
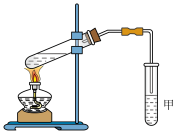
①实验开始前装置甲中所盛液体为___________ 。
②实验开始后,当观察到试管甲中___________ 时,认为反应基本完成。
(5)写出C→D反应的化学方程式___________ 。

已知:
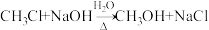
(1)F的名称为
(2)N的结构简式
(3)鉴别C和E的常用试剂有
(4)某同学用如图所示的实验装置利用C与E制取P,实验结束后,试管甲中上层为透明的、不溶于水的油状液体。

①实验开始前装置甲中所盛液体为
②实验开始后,当观察到试管甲中
(5)写出C→D反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】为测定某烃A的分子组成和结构,对这种烃进行以下实验:
①取一定量的该烃,使其充分燃烧后的气体通过装有CaCl2干燥管,干燥管增重7.2g;再通过石灰水,石灰水增重17.6g。
②经测定,该烃(气体)在标准状况下的密度为1.25g·L-1。
现以A为主要原料合成乙酸乙酯,其合成路线如图1所示。

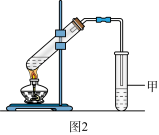
(1)E是常见的高分子材料,写出E的结构简式___________ ;合成E的反应类型___________ ;
(2)B中官能团的名称是___________ ,B可通过加入强氧化剂为___________ (任填一种)一步直接氧化为D.
(3)写出A→B化学方程式:___________ 。
(4)0.1mol该烃A能与___________ g溴发生加成反应;加成产物需___________ mol溴蒸气完全取代。
(5)某同学用如图2所示的实验装置制取少量乙酸乙酯。实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
①写出乙酸乙酯制备原理方程式:___________ 。
②实验开始时,试管甲中的导管不伸入液面下的原因是___________ 。
③上述实验中饱和碳酸钠溶液的作用是___________ 。
①取一定量的该烃,使其充分燃烧后的气体通过装有CaCl2干燥管,干燥管增重7.2g;再通过石灰水,石灰水增重17.6g。
②经测定,该烃(气体)在标准状况下的密度为1.25g·L-1。
现以A为主要原料合成乙酸乙酯,其合成路线如图1所示。


(1)E是常见的高分子材料,写出E的结构简式
(2)B中官能团的名称是
(3)写出A→B化学方程式:
(4)0.1mol该烃A能与
(5)某同学用如图2所示的实验装置制取少量乙酸乙酯。实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
①写出乙酸乙酯制备原理方程式:
②实验开始时,试管甲中的导管不伸入液面下的原因是
③上述实验中饱和碳酸钠溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】根据下列实验,总结苯的某些性质。
(1)向试管中加入 苯,再加入
苯,再加入 溴水,振荡后静置。观察到的现象是
溴水,振荡后静置。观察到的现象是________________________ 。
(2)向试管中加入 苯,再加入
苯,再加入 酸性高锰酸钾溶液,振荡后静置。观察到的现象是
酸性高锰酸钾溶液,振荡后静置。观察到的现象是_________________________________________________________________________________________ 。
(3)实验结论:苯________ (填“能”或“不能”)与溴水和酸性高锰酸钾溶液发生反应。
(4)根据上述实验结论可知:苯分子中________ (填“存在”或“不存在”)碳碳双键。
(1)向试管中加入
 苯,再加入
苯,再加入 溴水,振荡后静置。观察到的现象是
溴水,振荡后静置。观察到的现象是(2)向试管中加入
 苯,再加入
苯,再加入 酸性高锰酸钾溶液,振荡后静置。观察到的现象是
酸性高锰酸钾溶液,振荡后静置。观察到的现象是(3)实验结论:苯
(4)根据上述实验结论可知:苯分子中
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是A、B、C、D、E五种有机物的有关信息
回答下列问题:
(1)A~E中,属于烃的是___________ (填字母)。
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为__________
(3)C和E生成的酯在碱性(氢氧化钠溶液)条件下水解的化学方程式为_______
(4)有机物B具有的性质是________________ (填序号)。
①无色无味的液体;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是_____ (用化学方程式说明)。
A | ①能使溴的四氯化碳溶液褪色 ②能与水在一定条件下反应生成C ③比例模型为:  |
B | ①由C、H两种元素组成 ②球棍模型为:  |
C | ①由C、H、O三种元素组成②能与钠反应 ③与E反应生成相对分子质量为88的酯 |
D | ①相对分子质量比C少2 ②能比C催化氧化得到 |
E | ①由C、H、O三种元素组成 ②其水溶液能使紫色石蕊试液变红 |
(1)A~E中,属于烃的是
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为
(3)C和E生成的酯在碱性(氢氧化钠溶液)条件下水解的化学方程式为
(4)有机物B具有的性质是
①无色无味的液体;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】德国化学家凯库勒认为:苯分子是由6个碳原子以单双键相互交替结合而成的环状结构,为了验证凯库勒有关苯环的观点,甲同学设计了如图实验方案。

①按如图所示的装置图连接好各仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;
④待C中烧瓶收集满气体后,将导管b的下端插入烧杯里的水中,挤压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题。
(1)A中所发生反应的反应方程式为_____ ,能证明凯库勒观点错误的实验现象是_____ 。
(2)装置B的作用是_________ 。
(3)C中烧瓶的容器为500 mL,收集气体时,由于空气未排尽,最终水未充满烧瓶,假设烧瓶中混合气体对H2的相对密度为37.9,那么实验结束时,可计算进入烧瓶中的水的体积为_______ mL。(空气的平均相对分子质量为29)
(4)已知乳酸的结构简式为: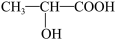 。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:
。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:______ 。

①按如图所示的装置图连接好各仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;
④待C中烧瓶收集满气体后,将导管b的下端插入烧杯里的水中,挤压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题。
(1)A中所发生反应的反应方程式为
(2)装置B的作用是
(3)C中烧瓶的容器为500 mL,收集气体时,由于空气未排尽,最终水未充满烧瓶,假设烧瓶中混合气体对H2的相对密度为37.9,那么实验结束时,可计算进入烧瓶中的水的体积为
(4)已知乳酸的结构简式为:
 。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:
。试回答: 乳酸跟氢氧化钠溶液反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】用燃烧法测定某有机物的实验式常用装置如图:

(1)使生成的O2按从左到右的方向流动,则所选装置中各导管的连接顺序g____ b(或a),其中装置C和装置E中CuO的作用分别是____ 。
(2)有机物H常用于食品行业,准确称取9.0gH置于上述装置E中,在足量O2中充分燃烧,B中质量增重5.4g,A中质量增重13.2g,请回答下列问题:

①H分子的质谱图如图所示,从图中可知其相对分子质量是____ ,则H的分子式是____ 。
②H能与NaHCO3溶液发生反应,H一定含有的官能团名称是____ 。
③H分子的核磁共振氢谱有4个峰,峰面积之比是1∶1∶1∶3,则H的结构简式是____ 。

(1)使生成的O2按从左到右的方向流动,则所选装置中各导管的连接顺序g
(2)有机物H常用于食品行业,准确称取9.0gH置于上述装置E中,在足量O2中充分燃烧,B中质量增重5.4g,A中质量增重13.2g,请回答下列问题:

①H分子的质谱图如图所示,从图中可知其相对分子质量是
②H能与NaHCO3溶液发生反应,H一定含有的官能团名称是
③H分子的核磁共振氢谱有4个峰,峰面积之比是1∶1∶1∶3,则H的结构简式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】乳酸正丙酯具有高沸点、低毒性和较好的水溶性,广泛应用于涂料、化妆品及生物溶剂领域。某小组同学欲通过实验研究乳酸的结构,并制备乳酸正丙酯。
【实验1】研究乳酸的结构
i.确定分子式。利用元素分析法和质谱法测得乳酸的分子式为C3H6O3。
ii.确定官能团。通过红外光谱初步确定乳酸分子的官能团为-COOH和-OH,并进行如下实验验证。
(1)实验①中,检测试剂为___________ 。
(2)实验②中,观察到的现象为___________ 。
iii.确定结构简式。
(3)乳酸分子的核磁共振氢谱如下图所示。结合上述信息推测乳酸的结构简式为___________ 。

【实验2】制备乳酸正丙酯
实验室制备乳酸正丙酯的步骤如下:

i.将乳酸、正丙醇(物质的量之比为1:3)和浓硫酸投入三口瓶中(装置如图,加热、夹持、搅拌装置已略去),加热至102~105℃,反应6h。
ii.酯化结束后,降温至60℃以下,加入与硫酸等物质的量的纯碱。
iii.常压蒸馏至110℃左右,收集到的馏分经处理后循环使用。
iv.当温度高于110℃时,停止加热,冷却,当温度降至40℃以下时,接好减压装置,进行减压蒸馏,收集120℃左右的馏分,获得乳酸正丙酯。资料:相关物质的沸点如下表。
(4)步骤i中,乳酸与正丙醇发生酯化反应的化学方程式为___________ 。
(5)步骤iii中,收集到的可循环使用的物质主要是___________ 。
(6)步骤iv中,减压蒸馏的目的之一是防止温度过高乳酸分子间生成交酯(六元环状酯),该交酯的结构简式为___________ 。
【实验1】研究乳酸的结构
i.确定分子式。利用元素分析法和质谱法测得乳酸的分子式为C3H6O3。
ii.确定官能团。通过红外光谱初步确定乳酸分子的官能团为-COOH和-OH,并进行如下实验验证。
| 序号 | 待验证官能团 | 检测试剂 | 实验现象 | 实验结论 |
| ① | -COOH | ___________ | 产生无色气泡 | 含有-COOH |
| ② | -OH | 酸性KMnO4溶液 | ___________ | 含有-OH |
(2)实验②中,观察到的现象为
iii.确定结构简式。
(3)乳酸分子的核磁共振氢谱如下图所示。结合上述信息推测乳酸的结构简式为

【实验2】制备乳酸正丙酯
实验室制备乳酸正丙酯的步骤如下:

i.将乳酸、正丙醇(物质的量之比为1:3)和浓硫酸投入三口瓶中(装置如图,加热、夹持、搅拌装置已略去),加热至102~105℃,反应6h。
ii.酯化结束后,降温至60℃以下,加入与硫酸等物质的量的纯碱。
iii.常压蒸馏至110℃左右,收集到的馏分经处理后循环使用。
iv.当温度高于110℃时,停止加热,冷却,当温度降至40℃以下时,接好减压装置,进行减压蒸馏,收集120℃左右的馏分,获得乳酸正丙酯。资料:相关物质的沸点如下表。
| 物质 | 乳酸 | 正丙醇 | 乳酸正丙酯 |
| 沸点/℃ | 227.6 | 97.2 | 168 |
(5)步骤iii中,收集到的可循环使用的物质主要是
(6)步骤iv中,减压蒸馏的目的之一是防止温度过高乳酸分子间生成交酯(六元环状酯),该交酯的结构简式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】奥拉帕尼是一种多聚ADP聚糖聚合酶抑制剂,可以通过肿瘤DNA修复途径缺陷,优先杀死癌细胞。其中一种合成方法如图:
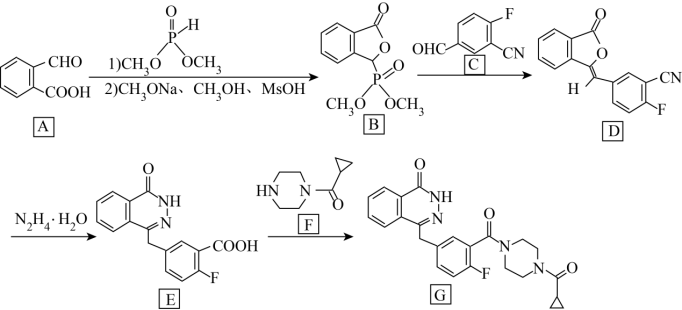
回答下列问题:
(1)化合物A中的官能团有______ (写名称)。
(2)化合物C中碳原子的杂化方式______ 。
(3)化合物D可能发生的反应有______ (填标号)。
(4)化合物A与足量新制氢氧化铜反应的化学方程式为_____ 。
(5)已知由B生成D的过程分两步进行:第①步:B+C→M;第②步:M→D+W。则W的结构简式为______ 。
(6)符合下列条件的F的同分异构体有_____ 种(不考虑立体异构)。
a.能发生银镜反应 b.含有碳碳双键 c.具有 结构片段
结构片段
写出其中核磁共振氢谱峰有6个峰,且面积比为1∶1∶2∶2∶4∶4的有机物的结构简式_____ 。

回答下列问题:
(1)化合物A中的官能团有
(2)化合物C中碳原子的杂化方式
(3)化合物D可能发生的反应有
| A.加成反应 | B.酯化反应 | C.水解反应 | D.消去反应 |
(5)已知由B生成D的过程分两步进行:第①步:B+C→M;第②步:M→D+W。则W的结构简式为
(6)符合下列条件的F的同分异构体有
a.能发生银镜反应 b.含有碳碳双键 c.具有
 结构片段
结构片段写出其中核磁共振氢谱峰有6个峰,且面积比为1∶1∶2∶2∶4∶4的有机物的结构简式
您最近一年使用:0次



