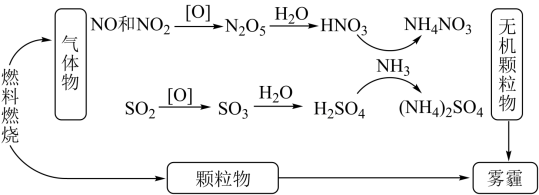
我国“蓝天保卫战”成果显著。科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:
回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有(写化学式)_______ 。
(2)图中物质溶于水溶液呈碱性的是_______ 。
(3)写出SO2转化为SO3的化学方程式_______ 。
(4)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为(用化学方程式表示)_______ 。
(5)氨气与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为_______ 。

回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有(写化学式)
(2)图中物质溶于水溶液呈碱性的是
(3)写出SO2转化为SO3的化学方程式
(4)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为(用化学方程式表示)
(5)氨气与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为
更新时间:2022-06-27 15:51:40
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室用如下方法测定 与
与 的混合物中
的混合物中 的质量分数。
的质量分数。
(1)称取该混合物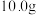 ,溶于水配成
,溶于水配成 溶液,下列操作会使所配溶液浓度偏小的有
溶液,下列操作会使所配溶液浓度偏小的有____ (填标号)。
A.未将洗涤液转移至容量瓶中
B.定容时俯视刻度线
C.定容振荡摇匀后液面低于刻度线,未做处理
(2)量取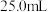 上述溶液于烧杯中,滴加足量
上述溶液于烧杯中,滴加足量 溶液,将
溶液,将 、
、 完全转化为沉淀,其中
完全转化为沉淀,其中 参与反应的离子方程式为
参与反应的离子方程式为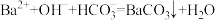 ,
, 属于
属于_______ (填“酸碱”或“盐”)。
(3)简述证明溶液中 、
、 已完全转化为沉淀的操作及现象:
已完全转化为沉淀的操作及现象:________ 。
 与
与 的混合物中
的混合物中 的质量分数。
的质量分数。(1)称取该混合物
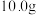 ,溶于水配成
,溶于水配成 溶液,下列操作会使所配溶液浓度偏小的有
溶液,下列操作会使所配溶液浓度偏小的有A.未将洗涤液转移至容量瓶中
B.定容时俯视刻度线
C.定容振荡摇匀后液面低于刻度线,未做处理
(2)量取
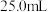 上述溶液于烧杯中,滴加足量
上述溶液于烧杯中,滴加足量 溶液,将
溶液,将 、
、 完全转化为沉淀,其中
完全转化为沉淀,其中 参与反应的离子方程式为
参与反应的离子方程式为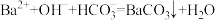 ,
, 属于
属于(3)简述证明溶液中
 、
、 已完全转化为沉淀的操作及现象:
已完全转化为沉淀的操作及现象:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】中药常采用硫黄熏蒸法以达到防霉、防虫等目的。我国规定党参等中药 残留量不得超过
残留量不得超过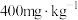 。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
① 残留量是指残留硫的总量,以
残留量是指残留硫的总量,以 计;
计;
②中药中残留的 已大部分转化为
已大部分转化为 。
。
(1)将200g所售党参研碎,用500mL 0.01 NaOH溶液充分浸泡,得无色浸泡液X,将X分成两等份。用NaOH溶液浸泡的目的
NaOH溶液充分浸泡,得无色浸泡液X,将X分成两等份。用NaOH溶液浸泡的目的___________ (用化学方程式表示)。
(2)甲同学取一份X溶液采用如下方案测定党参中 残留量:
残留量: 溶液已过量的操作为
溶液已过量的操作为___________ 。
②党参中 残留量的表达式为
残留量的表达式为___________  (用含m的式子表示)。
(用含m的式子表示)。
(3)乙同学取另一份X溶液采用如下方案进行测定(整个过程无气体放出),判断该党参___________ (填“符合”或“不符合”)国家标准。 排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应
排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应 。
。
①通入的气体中氧气的浓度偏低时,产生的CO与 反应生成CaO等三种氧化物,该反应的化学方程式为
反应生成CaO等三种氧化物,该反应的化学方程式为___________ ,被氧化的元素为___________ (填元素符号)。
②从物质类别角度分析,上述①中方程式涉及的物质中,既属于电解质又属于盐的是___________ 。
 残留量不得超过
残留量不得超过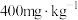 。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:①
 残留量是指残留硫的总量,以
残留量是指残留硫的总量,以 计;
计;②中药中残留的
 已大部分转化为
已大部分转化为 。
。(1)将200g所售党参研碎,用500mL 0.01
 NaOH溶液充分浸泡,得无色浸泡液X,将X分成两等份。用NaOH溶液浸泡的目的
NaOH溶液充分浸泡,得无色浸泡液X,将X分成两等份。用NaOH溶液浸泡的目的(2)甲同学取一份X溶液采用如下方案测定党参中
 残留量:
残留量: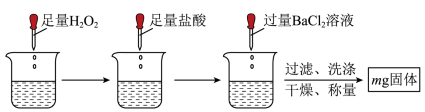
 溶液已过量的操作为
溶液已过量的操作为②党参中
 残留量的表达式为
残留量的表达式为 (用含m的式子表示)。
(用含m的式子表示)。(3)乙同学取另一份X溶液采用如下方案进行测定(整个过程无气体放出),判断该党参
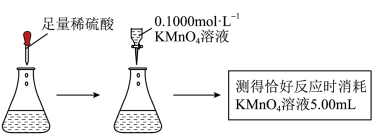
 排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应
排放。在煤炭中加入一定量石灰石,850℃在氧气的作用下,发生反应 。
。①通入的气体中氧气的浓度偏低时,产生的CO与
 反应生成CaO等三种氧化物,该反应的化学方程式为
反应生成CaO等三种氧化物,该反应的化学方程式为②从物质类别角度分析,上述①中方程式涉及的物质中,既属于电解质又属于盐的是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E五种物质均为中学化学中常见的化合物,已知A、B、C、D、E五种物质里含有相同的一种金属元素,并且A、B、C、D都可与物质M反应生成E,物质之间按箭头方向都可通过一步反应实现转化。实验室通常用碱B的澄清溶液检验CO2。
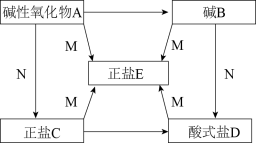
回答下列问题:
(1)写出物质的化学式:A__________ 、B__________ 、C__________ 、E__________ 。
(2)M属于__________ (填“酸”“碱”“盐”“酸性氧化物”或“碱性氧化物”)。
(3)写出正盐C转化为酸式盐D的化学方程式:____________________ 。
(4)写出碱B转化为酸式盐D的化学方程式:____________________ 。

回答下列问题:
(1)写出物质的化学式:A
(2)M属于
(3)写出正盐C转化为酸式盐D的化学方程式:
(4)写出碱B转化为酸式盐D的化学方程式:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】已知氨气极易溶解于水;在加热条件下氨气可与灼热的氧化铜反应,产物为氮气、水和金属铜。用下图的装置可以实现该反应(加持装置已略去)。
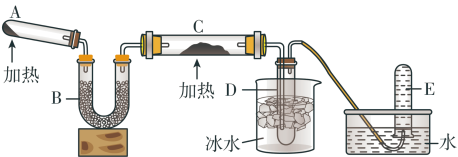
回答下列问题:
(1)A中发生反应的化学方程式是______
(2)B中加入的物质的名称是______ ,其作用是______
(3)实验时在C中观察到的现象是______ ,发生反应的化学方程式是______ 该反应中还原剂的化学式为______ 。
(4)实验结束后在D中观察到的现象是______ ,D中收集到的物质为______ (填“酸性”、“中性”,“碱性”),E中收集到气体的摩尔质量为______ 。

回答下列问题:
(1)A中发生反应的化学方程式是
(2)B中加入的物质的名称是
(3)实验时在C中观察到的现象是
(4)实验结束后在D中观察到的现象是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学研究性学习小组利用以下装置制取并探究氨气的性质。在A装置中发生反应的化学方程式为: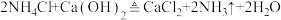
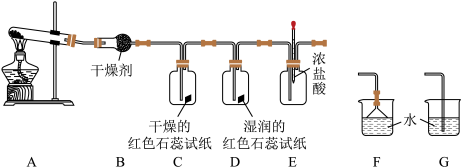
(1)B装置中的干燥剂是_______ (填“碱石灰”或“浓硫酸”)。
(2)C、D装置中试纸颜色会发生变化的是_______ (填“C”或“D”)。
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入 滴浓盐酸,可观察到E装置中的现象是产生
滴浓盐酸,可观察到E装置中的现象是产生______ (填“白烟”或“白雾”)。写出发生的化学反应方程式:______ 。
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是_______ (填“F”或“G”)。
(5)氨气具有较强的还原性,在催化剂(如铂丝或Cr2O3)催化下,氨气与氧气反应生成一氧化氮和水,写出相应的方程式:_______ 。
(6)生石灰与水反应生成 并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是
并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是_______ (填“a”“b”或“c”)。
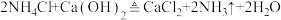

(1)B装置中的干燥剂是
(2)C、D装置中试纸颜色会发生变化的是
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入
 滴浓盐酸,可观察到E装置中的现象是产生
滴浓盐酸,可观察到E装置中的现象是产生(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是
(5)氨气具有较强的还原性,在催化剂(如铂丝或Cr2O3)催化下,氨气与氧气反应生成一氧化氮和水,写出相应的方程式:
(6)生石灰与水反应生成
 并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是
并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
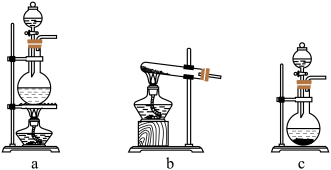
【推荐3】某研究性学习小组设计用如图所示实验装置(夹持仪器省略),制取干燥的NH3并验证NH3的性质。
(1)实验室用装置甲制备NH3的化学方程式为___________ 。
(2)装置乙的作用是___________ ,若装置丙用于收集NH3,应将导管___________ (填“a”或“b”)延长至集气瓶底部。
(3)装置戊所用仪器的名称为___________ 。
(4)观察到丁中红色Fe2O3粉末变黑,戊中无水硫酸铜变蓝,同时收集到一种无色无味的气体,取反应后的黑色粉末加入稀盐酸,产生气泡,证明NH3具有___________ 性,写出NH3和Fe2O3反应的化学方程式___________ 。
(5)为防止环境污染,可用以下装量(盛放的液体均为水)吸收多余NH3的是___________ (填标号)。
a. b.
b. c.
c. d.
d.

(1)实验室用装置甲制备NH3的化学方程式为
(2)装置乙的作用是
(3)装置戊所用仪器的名称为
(4)观察到丁中红色Fe2O3粉末变黑,戊中无水硫酸铜变蓝,同时收集到一种无色无味的气体,取反应后的黑色粉末加入稀盐酸,产生气泡,证明NH3具有
(5)为防止环境污染,可用以下装量(盛放的液体均为水)吸收多余NH3的是
a.
 b.
b. c.
c. d.
d.
您最近半年使用:0次



