海洋资源的利用具有广阔前景。
I.海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海带中提取碘的流程如下:

(1)步骤①灼烧海带时,盛放海带的仪器名称是_______ 。
(2)步骤④中反应的离子方程式为_______ 。
(3)步骤⑤的操作为:向含I2的水溶液加入有机试剂,用力震荡后静置分层后分液,则可以选择的有机试剂是_______(填标号)。
II.为除去粗盐中含有的可溶性杂质硫酸钠、氯化钙和氯化镁,某同学利用给定试剂NaOH溶液、BaCl2溶液、 溶液和盐酸,设计了如图实验流程:
溶液和盐酸,设计了如图实验流程:
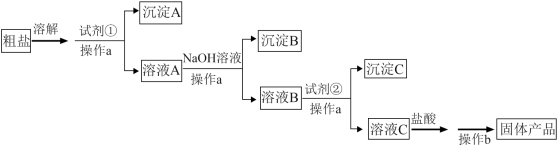
(4)操作a和操作b的名称依次是_______ 、_______ 试剂①是_______ 。
(5)加入试剂②后,发生反应的离子方程式是_______ 。
(6)加入盐酸的作用是_______ 。你设计的流程和该同学的一样吗?简述不同之处_______ (若一样则此空不填)。
I.海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海带中提取碘的流程如下:

(1)步骤①灼烧海带时,盛放海带的仪器名称是
(2)步骤④中反应的离子方程式为
(3)步骤⑤的操作为:向含I2的水溶液加入有机试剂,用力震荡后静置分层后分液,则可以选择的有机试剂是_______(填标号)。
| A.四氯化碳 | B.酒精 | C.苯 | D.醋酸 |
II.为除去粗盐中含有的可溶性杂质硫酸钠、氯化钙和氯化镁,某同学利用给定试剂NaOH溶液、BaCl2溶液、
 溶液和盐酸,设计了如图实验流程:
溶液和盐酸,设计了如图实验流程:
(4)操作a和操作b的名称依次是
(5)加入试剂②后,发生反应的离子方程式是
(6)加入盐酸的作用是
更新时间:2022-07-16 10:37:34
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】现有含有少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。

(1)沉淀A的主要成分是_______ (填化学式)。
(2)②中反应的离子方程式是_______ 。
(3)①②③中均进行的分离操作是_______ 。
(4)溶液3经过处理可以得到NaNO3固体,为了除去溶液3中含有的杂质,可向溶液3中加入适量的_______ (填化学式)。

(1)沉淀A的主要成分是
(2)②中反应的离子方程式是
(3)①②③中均进行的分离操作是
(4)溶液3经过处理可以得到NaNO3固体,为了除去溶液3中含有的杂质,可向溶液3中加入适量的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】海盐(含泥沙、 、
、 、
、 、
、 、
、 等杂质)可用于制备试剂级
等杂质)可用于制备试剂级 。流程如图所示:
。流程如图所示:

回答下列问题:
(1)从物质分类的角度看,海盐属于_______ 。
(2)除杂时能除去一些可溶性杂质离子,在表中填写除杂时依次添加的试剂及其预期沉淀的离子:
(3)制得的试剂级 晶体中一定还有的杂质阳离子为
晶体中一定还有的杂质阳离子为_______ 。请设计实验检验该杂质离子_______ (简述实验操作与现象)。
(4)称取制得的试剂级 晶体
晶体 ,加蒸馏水溶解,通过阳离子交换树脂(用
,加蒸馏水溶解,通过阳离子交换树脂(用 表示),将溶液中的少量杂质阳离子全部转化为钠离子(如图),反应的离子方程式为
表示),将溶液中的少量杂质阳离子全部转化为钠离子(如图),反应的离子方程式为_______ 。收集纯氯化钠溶液蒸发结晶,得到固体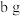 ,则制得试剂级
,则制得试剂级 晶体中杂质阳离子的物质的量为
晶体中杂质阳离子的物质的量为_______  (用含a、b的代数式表示)。
(用含a、b的代数式表示)。

 、
、 、
、 、
、 、
、 等杂质)可用于制备试剂级
等杂质)可用于制备试剂级 。流程如图所示:
。流程如图所示:
回答下列问题:
(1)从物质分类的角度看,海盐属于
(2)除杂时能除去一些可溶性杂质离子,在表中填写除杂时依次添加的试剂及其预期沉淀的离子:
| 实验步骤 | 试剂 | 预期沉淀的离子 |
| 步骤1 |  溶液 溶液 |  和 和 |
| 步骤2 | ||
| 步骤3 |
 晶体中一定还有的杂质阳离子为
晶体中一定还有的杂质阳离子为(4)称取制得的试剂级
 晶体
晶体 ,加蒸馏水溶解,通过阳离子交换树脂(用
,加蒸馏水溶解,通过阳离子交换树脂(用 表示),将溶液中的少量杂质阳离子全部转化为钠离子(如图),反应的离子方程式为
表示),将溶液中的少量杂质阳离子全部转化为钠离子(如图),反应的离子方程式为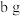 ,则制得试剂级
,则制得试剂级 晶体中杂质阳离子的物质的量为
晶体中杂质阳离子的物质的量为 (用含a、b的代数式表示)。
(用含a、b的代数式表示)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】食盐是一种日常生活中必不可少的调味品。中国最早提纯食盐的方法称为“夙沙作煮盐”,而今随着工业发展,通常采用化学沉淀法提纯粗盐。回答下列问题:
(1)图中实验操作与海水晒盐的基本原理相同的是_______ (填字母)。

(2)化学沉淀法提纯粗盐(含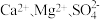 等杂质)的工艺流程如下。
等杂质)的工艺流程如下。
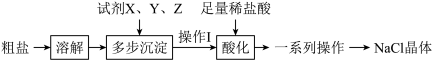
①试剂X、Y、Z分别是下列三种溶液中的一种:a.足量BaCl2溶液b.足量NaOH溶液c.足量Na₂CO₃溶液,则加入顺序为b→_______ 。
②粗盐溶液中加入足量BaCl2溶液,发生反应的离子方程式为_______ 。
③加入足量Na2CO3溶液生成沉淀的化学式为_______ 。
④操作Ⅰ为_______ ;“酸化”中加入足量稀盐酸,导致最终产率_______ (填“偏大”“偏小”或“不变”)。
⑤取12g产品,加入足量水溶解,再加入足量AgNO3溶液,过滤、洗涤、干燥沉淀,得到沉淀28.7g,则氯化钠的纯度为_______ %。
(1)图中实验操作与海水晒盐的基本原理相同的是

(2)化学沉淀法提纯粗盐(含
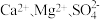 等杂质)的工艺流程如下。
等杂质)的工艺流程如下。
①试剂X、Y、Z分别是下列三种溶液中的一种:a.足量BaCl2溶液b.足量NaOH溶液c.足量Na₂CO₃溶液,则加入顺序为b→
②粗盐溶液中加入足量BaCl2溶液,发生反应的离子方程式为
③加入足量Na2CO3溶液生成沉淀的化学式为
④操作Ⅰ为
⑤取12g产品,加入足量水溶解,再加入足量AgNO3溶液,过滤、洗涤、干燥沉淀,得到沉淀28.7g,则氯化钠的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】从海带中提取碘,有甲、乙两种实验方案如下:

已知:3I2+6NaOH═5NaI+NaIO3+3H2O.请回答:
(1)步骤 X 的操作为萃取分液,分液时需用到分液漏斗,分液漏斗在使用前需_____ .
(2)方案甲进行蒸馏操作时,通常使用水浴加热,其优点是_____ .
(3)方案乙在上层溶液中加入 H2SO4溶液得到 I2的水溶液,发生反应的化学方程式是_____
(4)操作 Z 的名称是_____ .

已知:3I2+6NaOH═5NaI+NaIO3+3H2O.请回答:
(1)步骤 X 的操作为萃取分液,分液时需用到分液漏斗,分液漏斗在使用前需
(2)方案甲进行蒸馏操作时,通常使用水浴加热,其优点是
(3)方案乙在上层溶液中加入 H2SO4溶液得到 I2的水溶液,发生反应的化学方程式是
(4)操作 Z 的名称是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
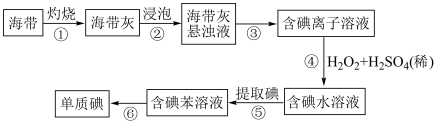
请填写下列空白:
(1)步骤①灼烧海带时,盛放海带的仪器名称是______________ 。
(2)步骤③的实验操作名称是_________ ,步骤⑥的目的是从含碘苯溶液中分离出碘单质和回收苯,该步骤的实验操作名称是_______________ 。
(3)步骤④反应的离子方程式是______________________________ 。
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法___________ 。

请填写下列空白:
(1)步骤①灼烧海带时,盛放海带的仪器名称是
(2)步骤③的实验操作名称是
(3)步骤④反应的离子方程式是
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】从海水中可以获得淡水、食盐并可提取镁和溴等物质。
实验(一)海水提溴:空方气吹出法是工业规模提溴的常用法,其流程如图:
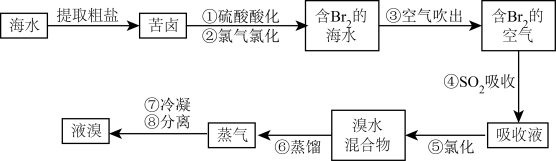
(1)步骤④反应的离子方程式为___________ 。除SO2外,步骤④还可以选用Na2CO3溶液吸收溴,主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),吸收3molBr2时,转移电子的物质的量为___________ mol。
实验(二)碘的制取:另取海带浸取原液,甲、乙两种实验方案如图:

已知:3I2+6KOH=5NaI+NaIO3+3H2O;酸性条件下,I2在水中的溶解度很小。
(2)“适量O2”中能代替O2的最佳物质是___________ 。
(3)步骤X中,萃取后分液漏斗内观察到的现象是___________ 。
(4)步骤Y中提纯的方法称为___________ 。
(5)方案乙中,上层液体中加入H2SO4溶液,反应的离子方程式为___________ ,其中操作Z的名称是___________ 。
实验(一)海水提溴:空方气吹出法是工业规模提溴的常用法,其流程如图:

(1)步骤④反应的离子方程式为
实验(二)碘的制取:另取海带浸取原液,甲、乙两种实验方案如图:

已知:3I2+6KOH=5NaI+NaIO3+3H2O;酸性条件下,I2在水中的溶解度很小。
(2)“适量O2”中能代替O2的最佳物质是
(3)步骤X中,萃取后分液漏斗内观察到的现象是
(4)步骤Y中提纯的方法称为
(5)方案乙中,上层液体中加入H2SO4溶液,反应的离子方程式为
您最近一年使用:0次



