磷酸(H3PO4)、亚磷酸(H3PO3)和次磷酸(H3PO2)都是重要的化工产品。已知:1 mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3 mol、2 mol、1 mol。下列推断正确的是
| A.磷酸与氢氧化钠反应能生成2种盐 |
| B.NaH2PO4、NaH2PO3、NaH2PO2都是酸式盐 |
| C.H3PO4是三元酸、H3PO3是二元酸、H3PO2是一元酸 |
| D.H3PO3是三元酸,又是还原性酸 |
更新时间:2022-08-03 18:26:20
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】图中相连物质间在一定条件下可以发生反应,表中提供的四组物质符合要求的是
 | 选项 | 甲 | 乙 | 丙 | 丁 |
| A | H2 | O2 | HCl | CuO | |
| B | Mg | HCl | CuCl2 | NaOH | |
| C | Na2CO3 | BaCl2 | HCl | Ca(OH)2 | |
| D | Ca(OH)2 | CO2 | NaOH | CuSO4 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】分类是科学研究的重要方法,下列物质分类不正确的是
| A.化合物:干冰、冰水混合物、烧碱、小苏打 |
B.同素异形体:活性炭、 、石墨、金刚石 、石墨、金刚石 |
| C.非电解质:乙醇、四氯化碳、氯气、葡萄糖 |
| D.混合物:漂白粉、纯净矿泉水、盐酸、大理石 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某小组在验证反应“Fe+2Ag+=Fe2++2Ag”的实验中检测到Fe3+,实验过程如下:向硝酸酸化的0.05mol/L硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。取上层清液,滴加KSCN溶液,溶液变红,同时发现有白色沉淀产生,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
(资料:Ag+与SCN-生成白色沉淀AgSCN)
依据上述实验现象,不能 得出的结论是
| 序号 | 取样时间/min | 现象 |
| ⅰ | 3 | 产生大量白色沉淀;溶液呈红色 |
| ⅱ | 30 | 产生白色沉淀,较3min时量少;溶液红色较3min时加深 |
| ⅲ | 120 | 产生白色沉淀,较30min时量少;溶液红色较30min时变浅 |
依据上述实验现象,
| A.上层清液中滴加KSCN溶液,溶液变红,说明溶液中含有Fe3+ |
| B.上层清液中滴加KSCN溶液,产生白色沉淀,说明溶液中含有Ag+ |
C.Fe3+产生的原因是由于酸性溶液中的 具有氧化性 具有氧化性 |
| D.30min时“白色沉淀量减少,溶液红色加深”的原因可能是:Fe2++Ag+=Fe3++Ag |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
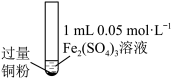
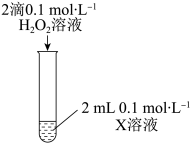
【推荐2】某小组同学通过实验研究 溶液与铜粉发生的氧化还原反应。实验记录如下:
溶液与铜粉发生的氧化还原反应。实验记录如下:
下列说法不正确的是
 溶液与铜粉发生的氧化还原反应。实验记录如下:
溶液与铜粉发生的氧化还原反应。实验记录如下:序号 | Ⅰ | Ⅱ | Ⅲ |
实验步骤 |
|
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
A.实验Ⅰ、Ⅱ、Ⅲ中均涉及 被还原 被还原 |
| B.对比实验Ⅰ、Ⅱ说明白色沉淀的产生与铜粉的量有关 |
C.实验Ⅱ、Ⅲ中加入蒸馏水后 相同 相同 |
| D.向实验Ⅲ反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀 |
您最近半年使用:0次



 +5H2O2+6H+=2Mn2++5O2↑+8H2O
+5H2O2+6H+=2Mn2++5O2↑+8H2O =SO
=SO +H2O
+H2O

