化学键
(1)化学键
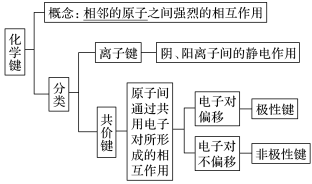
(2)离子键和共价键的比较
(3)化学反应的本质:一个化学反应过程,本质上就是____ 的断裂和____ 的形成过程。
(1)化学键

(2)离子键和共价键的比较
| 离子键 | 共价键 | ||
| 非极性键 | 极性键 | ||
| 概念 | 带相反电荷离子之间的相互作用 | 原子间通过共用电子对(电子云重叠)而形成的化学键 | |
| 成键粒子 | 阴、阳离子 | 原子 | |
| 成键实质 | 阴、阳离子的静电作用 | 共用电子对不偏向任何一方 | 共用电子对偏向一方原子 |
| 形成条件 | 活泼金属元素与活泼非金属元素经电子得失形成离子键 | 同种元素原子之间成键 | 不同种元素原子之间成键 |
| 形成的物质 | 离子化合物 | 非金属单质;某些共价化合物或离子化合物 | 共价化合物或离子化合物 |
(3)化学反应的本质:一个化学反应过程,本质上就是
更新时间:2022-08-18 07:16:50
|
【知识点】 化学键与化学反应本质联系解读
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下列变化①碘的升华②烧碱熔化③氯化钠溶于水④氯化氢溶于水⑤氧气溶于水⑥氯化铵受热分解。
氯化铵的电子式是______________ ;未发生化学键破坏的是______________ (填序号,下同);仅发生离子键破坏的是______________ ;仅发生共价键破坏的是______________ ;既发生离子键又发生共价键破坏的是______________ 。
氯化铵的电子式是
您最近一年使用:0次
【推荐2】碳与硅是十分重要的两种元素,金刚石、SiC具有耐磨、耐腐蚀特性,应用广泛。
(1)碳元素在周期表中的位置是_______________ ,其原子核外通常未成对电子数为___________ 个。
(2)已知2Ca3(PO4)2(s)+10C(s)→P4(g)+6CaO(s)+10CO(g)反应中,被破坏的化学键有________ 。
a.离子键 b.极性共价键 c. 非极性共价键
(3)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,除去粗产品中少量钠的试剂为_______________ 。
(4)下列叙述正确的有____________ 填序号),
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③NaSiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④Si在一定条件下可与FeO发生置换反应
(1)碳元素在周期表中的位置是
(2)已知2Ca3(PO4)2(s)+10C(s)→P4(g)+6CaO(s)+10CO(g)反应中,被破坏的化学键有
a.离子键 b.极性共价键 c. 非极性共价键
(3)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,除去粗产品中少量钠的试剂为
(4)下列叙述正确的有
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③NaSiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④Si在一定条件下可与FeO发生置换反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.下图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,试问:
(1)步骤1、2分别是吸热过程还是放热过程?步骤1:________ ,步骤2:________ 。
(2)比较E1、E2、E3的大小:____________________ 。
II. 下列变化 ①碘的升华 ②烧碱熔化 ③氯化钠溶于水 ④氯化氢溶于水 ⑤氧气溶于水 ⑥氯化铵受热分解。
(1)未发生化学键破坏的是__________ ;(填序号,下同)仅发生离子键破坏的是______________ ;
(2)若上述物质都为纯净物时,属于共价化合物的是_______ ;属于离子化合物的是__________ ;
III. 写出下列物质的电子式:
S_______ CsOH_______ CO2_________
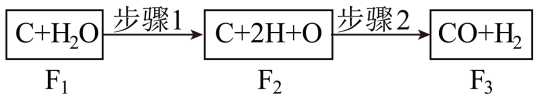
(1)步骤1、2分别是吸热过程还是放热过程?步骤1:
(2)比较E1、E2、E3的大小:
II. 下列变化 ①碘的升华 ②烧碱熔化 ③氯化钠溶于水 ④氯化氢溶于水 ⑤氧气溶于水 ⑥氯化铵受热分解。
(1)未发生化学键破坏的是
(2)若上述物质都为纯净物时,属于共价化合物的是
III. 写出下列物质的电子式:
S
您最近一年使用:0次



