已知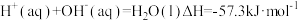 。下列说法正确的是
。下列说法正确的是
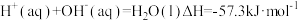 。下列说法正确的是
。下列说法正确的是A. 盐酸和 盐酸和 NaOH溶液反应放出热量为57.3 kJ NaOH溶液反应放出热量为57.3 kJ |
B. CH3COOH溶液和 CH3COOH溶液和 NaOH溶液反应放出热量为57.3 kJ NaOH溶液反应放出热量为57.3 kJ |
C.含 的浓硫酸和 的浓硫酸和 NaOH溶液反应放出热量为57.3 kJ NaOH溶液反应放出热量为57.3 kJ |
D. 稀硫酸和 稀硫酸和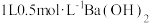 溶液反应放出热量为57.3 kJ 溶液反应放出热量为57.3 kJ |
更新时间:2022-09-08 09:37:02
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是
| A.测定盐酸和NaOH溶液反应的中和热时,每次实验均应测量三个温度,即盐酸的起始温度、NaOH溶液的起始温度和反应后的终止温度 |
| B.HCl和NaOH反应的中和热ΔH=−57.3 kJ·mol−1,则稀H2SO4和稀Ca(OH)2溶液反应的中和热 ΔH=−2×57.3 kJ·mol−1 |
| C.燃烧热是指在101 kPa时可燃物完全燃烧时所放出的热量 |
D.S(s)+  O2(g) O2(g) SO3(g) ΔH=−315 kJ·mol−1(燃烧热) SO3(g) ΔH=−315 kJ·mol−1(燃烧热) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列方程式书写正确的是

A.NaHSO4在熔融状态下的电离方程式:NaHSO4 = Na+ + HSO |
B.H2SO4溶液与NaOH溶液发生中和反应的热化学方程式为 已知 H2SO4 溶液与NaOH溶液发生反应的中和热为57.3kJ/mol : H2SO4(aq) + 2NaOH(aq) = 2H2O(l) + Na2SO4(aq) △H =-57.3kJ/mol 已知 H2SO4 溶液与NaOH溶液发生反应的中和热为57.3kJ/mol : H2SO4(aq) + 2NaOH(aq) = 2H2O(l) + Na2SO4(aq) △H =-57.3kJ/mol |
C.CO 的水解方程式: CO 的水解方程式: CO + 2H2O ⇌ H2CO3 +2OH- + 2H2O ⇌ H2CO3 +2OH- |
D.CaCO3的沉淀溶解平衡方程式: CaCO3(s) = Ca2+(aq) + CO (aq) (aq) |
您最近一年使用:0次

 C(金刚石,s)
C(金刚石,s) H>0,则金刚石比石墨稳定
H>0,则金刚石比石墨稳定 O2(g)=CO(g)
O2(g)=CO(g)

