Ⅰ.厨房中有下列用品:①食盐②小苏打③纯碱④食醋(主要成分为醋酸)。
(1)主要成分属于酸的是_______ (填序号);
(2)水溶液呈碱性的是_______ (填序号);
(3)食盐在水中的电离方程式是_______ 。
(4)纯碱中含有少量NaCl。检验此混合物中的 、
、 的实验操作步骤如下,将少量混合物加水溶解后,分别置于两支试管中。
的实验操作步骤如下,将少量混合物加水溶解后,分别置于两支试管中。
向第一支试管中加入稀盐酸,可观察到产生无色气泡,说明溶液中存在_______ 离子,该反应的离子方程式为_______ 。
向第二支试管中先加入足量稀硝酸,再加入_______ 溶液,可观察到白色沉淀,说明溶液中存在 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
Ⅱ. 和
和 热稳定性对比实验如下图所示。
热稳定性对比实验如下图所示。
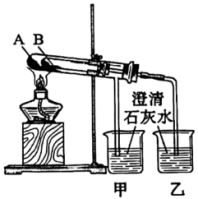
(5)物质A是_______ (填化学式)。
(6)能够证明 的热稳定性强于
的热稳定性强于 的证据是
的证据是_______ 。
(7)试管中发生反应的化学方程式是_______ 。烧杯中发生反应的离子方程式是_______ 。
(1)主要成分属于酸的是
(2)水溶液呈碱性的是
(3)食盐在水中的电离方程式是
(4)纯碱中含有少量NaCl。检验此混合物中的
 、
、 的实验操作步骤如下,将少量混合物加水溶解后,分别置于两支试管中。
的实验操作步骤如下,将少量混合物加水溶解后,分别置于两支试管中。向第一支试管中加入稀盐酸,可观察到产生无色气泡,说明溶液中存在
向第二支试管中先加入足量稀硝酸,再加入
 ,该反应的离子方程式为
,该反应的离子方程式为Ⅱ.
 和
和 热稳定性对比实验如下图所示。
热稳定性对比实验如下图所示。
(5)物质A是
(6)能够证明
 的热稳定性强于
的热稳定性强于 的证据是
的证据是(7)试管中发生反应的化学方程式是
更新时间:2022-11-06 17:34:03
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】P元素有三种含氧酸:H3PO4、H3PO3、H3PO2,它们依次为三元、二元、一元弱酸。H3PO2可将溶液中的Ag+还原为Ag,从而可用于化学镀银。请回答下列问题:
(1)写出H3PO4与足量NaOH溶液反应的化学方程式:___________ 。
(2)H3PO3中,P元素的化合价为___________ ;H3PO2的电离方程式是___________ 。
(3)Na2HPO3、NaH2PO2均属于___________ 盐(填“酸式”、“碱式”、“正”)。
(4)用H3PO2进行化学镀银时,氧化剂与还原剂的粒子个数之比为 ,则氧化产物可能为下列选项中的
,则氧化产物可能为下列选项中的___________ (填字母序号)。
a.H3PO3 b.H3PO4 c.无法确定
据此,写出上述镀银反应的离子方程式:___________ 。
(1)写出H3PO4与足量NaOH溶液反应的化学方程式:
(2)H3PO3中,P元素的化合价为
(3)Na2HPO3、NaH2PO2均属于
(4)用H3PO2进行化学镀银时,氧化剂与还原剂的粒子个数之比为
 ,则氧化产物可能为下列选项中的
,则氧化产物可能为下列选项中的a.H3PO3 b.H3PO4 c.无法确定
据此,写出上述镀银反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】分类是研究物质性质的重要方法,图中对某些物质进行分类。
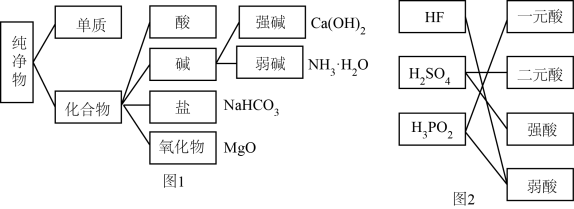
(1)图1的分类方法是_______ 分类法。
(2)写出 的电离方程式
的电离方程式_______ 。
(3)写出MgO与 反应的离子方程式
反应的离子方程式_______ ,由该反应可推断MgO为_______ 氧化物(填“酸性”或“碱性”)。
(4)写出 与足量NaOH反应的化学方程式
与足量NaOH反应的化学方程式_______ 。
(5)在工业上次磷酸( )常用于化学镀银,酸性条件下发生的反应如下:
)常用于化学镀银,酸性条件下发生的反应如下:
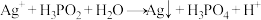 (未配平)
(未配平)
 中,P元素的化合价为
中,P元素的化合价为_______ ;该反应中, 发生
发生_______ (填“氧化”或“还原”)反应,氧化剂与还原剂的物质的量之比为_______ 。

(1)图1的分类方法是
(2)写出
 的电离方程式
的电离方程式(3)写出MgO与
 反应的离子方程式
反应的离子方程式(4)写出
 与足量NaOH反应的化学方程式
与足量NaOH反应的化学方程式(5)在工业上次磷酸(
 )常用于化学镀银,酸性条件下发生的反应如下:
)常用于化学镀银,酸性条件下发生的反应如下: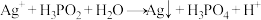 (未配平)
(未配平) 中,P元素的化合价为
中,P元素的化合价为 发生
发生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】2022年1月,南太平洋岛国汤加境内发生了“21世纪至今最剧烈的火山喷发”,对该国造成了严重的破坏。火山喷发过程部分化学反应如下:
① ;
;
②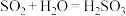 ;
;
③
(1)在上述方程式涉及的物质中,能与盐酸反应的氧化物有_______ (填化学式),属于酸的有_______ (填化学式)。
(2) 与
与 具有某些相似的化学性质,写出用NaOH溶液吸收
具有某些相似的化学性质,写出用NaOH溶液吸收 的化学方程式:
的化学方程式:_______ 。
(3) 是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。已知
是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。已知 称为正盐,
称为正盐, 称为酸式盐,写出
称为酸式盐,写出 的一种酸式盐的化学式:
的一种酸式盐的化学式:_______ 。
(4)互为同素异形体的物质均为_______ (选填“化合物”或“单质”)。请列举一组互为同素异形体的物质:_______ 。
①
 ;
;②
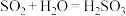 ;
;③

(1)在上述方程式涉及的物质中,能与盐酸反应的氧化物有
(2)
 与
与 具有某些相似的化学性质,写出用NaOH溶液吸收
具有某些相似的化学性质,写出用NaOH溶液吸收 的化学方程式:
的化学方程式:(3)
 是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。已知
是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。已知 称为正盐,
称为正盐, 称为酸式盐,写出
称为酸式盐,写出 的一种酸式盐的化学式:
的一种酸式盐的化学式:(4)互为同素异形体的物质均为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请按要求写出对应的方程式
(1)NaHSO4在熔融状态下的电离方程式为:___________
(2)制备Fe(OH)3胶体的化学方程式___________
(3)碳酸氢钙与过量氢氧化钠溶液反应的离子方程式___________
(4)除去Na2CO3固体中的NaHCO3的化学方程式:___________
(5)除去NaHCO3溶液中的Na2CO3的离子方程式:___________
(1)NaHSO4在熔融状态下的电离方程式为:
(2)制备Fe(OH)3胶体的化学方程式
(3)碳酸氢钙与过量氢氧化钠溶液反应的离子方程式
(4)除去Na2CO3固体中的NaHCO3的化学方程式:
(5)除去NaHCO3溶液中的Na2CO3的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有以下11种物质,请回答下列问题:①石墨 ②氧化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧醋酸 ⑨盐酸 ⑩硫酸铝 ⑪稀硫酸。
(1)属于电解质的是____________________ ;属于非电解质的是___________ 。
(2)写出物质⑥溶于水的电离方程式:___________________________________ 。
(3)写出物质⑤和少量⑦反应的化学方程式:_______________________________________ 。
(4)写出物质⑥和⑧在水中发生反应的离子方程式:______________________________ 。
(1)属于电解质的是
(2)写出物质⑥溶于水的电离方程式:
(3)写出物质⑤和少量⑦反应的化学方程式:
(4)写出物质⑥和⑧在水中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有以下13种物质,请回答下列问题:
①石墨 ②氧化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩硫酸铝 ⑪稀硫酸 ⑫氯化银 ⑬硫酸氢钠
(1)其中能导电的是_________ ; 属于电解质的是 _________ ;属于非电解质的是 _________ 。
(2)写出物质⑬溶于水的电离方程式:__________________ 。物质⑬属于________ (填“酸”、“碱”或“盐”)。
(3)写出物质⑦和⑪反应的离子方程式:___________________ 。
(4)写出物质⑥和⑨在水中发生反应的离子方程式:_____________________ 。
①石墨 ②氧化钠 ③酒精 ④氨水 ⑤二氧化碳 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧冰醋酸 ⑨氯化氢 ⑩硫酸铝 ⑪稀硫酸 ⑫氯化银 ⑬硫酸氢钠
(1)其中能导电的是
(2)写出物质⑬溶于水的电离方程式:
(3)写出物质⑦和⑪反应的离子方程式:
(4)写出物质⑥和⑨在水中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】高铁酸钠(Na2FeO4)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为 (胶体)
(胶体)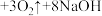 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
(1)高铁酸钠(Na2FeO4)属于___________ (“酸”、“碱”、“盐”或“氧化物”),其中铁的化合价为___________ 价;与O2互为同素异形体的物质的化学式为___________ 。
(2)将上述反应的化学方程式改写成离子方程式:___________ ,该反应中的O2为___________ (填标号)。
a.氧化产物 b.还原产物 c.既不是氧化产物又不是还原产物
(3)实验室制备 胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴
胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴___________ (填化学式)饱和溶液,继续煮沸至液体呈___________ 色,停止加热。
(4)当生成48g O2时,至少有___________ g水参与反应,生成的NaOH的质量为___________ g。
 (胶体)
(胶体)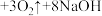 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:(1)高铁酸钠(Na2FeO4)属于
(2)将上述反应的化学方程式改写成离子方程式:
a.氧化产物 b.还原产物 c.既不是氧化产物又不是还原产物
(3)实验室制备
 胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴
胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴(4)当生成48g O2时,至少有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩矿泉水请回答下列问题:
(1)以上物质中属于混合物的是_______ (填序号),以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是_______
(3)写出④在水溶液中的电离方程式_______ 。
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的离子方程式_______ 。
(1)以上物质中属于混合物的是
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是
(3)写出④在水溶液中的电离方程式
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学反应在生产、生活中有广泛的用途。
素材I:海洋约占地球表面积的71%,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种物质,如NaCl(①)、MgSO4(②)等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水(③)用以生产NaOH(④)、Na2CO3(⑤)、Na(⑥)、Cl2(⑦)、盐酸(⑧)等,苦卤经过氯气氧化,热空气吹出、SO2(⑨)吸收等一系列操作可获得Br2。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
(1)上述标有序号的物质中,属于电解质的是_______ (填序号)。
(2)写出⑤在水中的电离方程式_______ 。
(3)已知SO2为酸性氧化物,试写出将足量SO2通入④的水溶液中发生反应的离子方程式_______ 。
(4)向空气中排放SO2会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
该雨水中氢离子的浓度a=_______ m mol/L。
素材II:储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,此反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、Cr2(SO4)3、K2SO4、H2O七种物质。
(5)请用上述物质填空,并配平化学方程式:_______ 。
______C+______+______ H2SO4→______ K2SO4+_____+_______+_______H2O。
(6)H2SO4在上述反应中表现出来的性质是_______(填选项编号)。
素材I:海洋约占地球表面积的71%,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种物质,如NaCl(①)、MgSO4(②)等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和食盐水(③)用以生产NaOH(④)、Na2CO3(⑤)、Na(⑥)、Cl2(⑦)、盐酸(⑧)等,苦卤经过氯气氧化,热空气吹出、SO2(⑨)吸收等一系列操作可获得Br2。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
(1)上述标有序号的物质中,属于电解质的是
(2)写出⑤在水中的电离方程式
(3)已知SO2为酸性氧化物,试写出将足量SO2通入④的水溶液中发生反应的离子方程式
(4)向空气中排放SO2会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
| 离子 |  |  | Na+ | Cl- | H+ |
| 浓度(mmol/L) | 0.06 | 0.08 | 0.02 | 0.04 |  |
该雨水中氢离子的浓度a=
素材II:储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,此反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、Cr2(SO4)3、K2SO4、H2O七种物质。
(5)请用上述物质填空,并配平化学方程式:
______C+______+______ H2SO4→______ K2SO4+_____+_______+_______H2O。
(6)H2SO4在上述反应中表现出来的性质是_______(填选项编号)。
| A.氧化性 | B.氧化性和酸性 | C.酸性 | D.还原性和酸性 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】食盐(NaCl)、纯碱(Na2CO3)和小苏打(NaHCO3)是日常家庭厨房中常见用品,请回答下面问题:
(1)有关食盐(NaCl)、纯碱(Na2CO3)和小苏打(NaHCO3)的说法正确的是______ 。
A.食盐属于盐、纯碱属于碱、小苏打属于酸
B.分别取三种物质做焰色反应实验,火焰颜色均呈现黄色
C.用三支小试管取适量三种物质加入少量水溶解,用手轻轻触摸试管,温度升高的是纯碱,温度明显降低的是小苏打
D.用三支试管取适量三种物质加入少量水溶解,滴加少量酚酞溶液,溶液变红的只有纯碱
(2)用化学方法鉴别三种物质有很多种方法。
①用三支小试管取适量三种物质加水溶解配制成溶液,加入少量CaCl2溶液,有白色沉淀生成的是纯碱,写出该反应的离子方程式____________ 。
②用三支小试管取适量三种物质分别加热,有使澄清石灰水变浑浊的气体产生的是小苏打。写出小苏打加热分解的方程式____________ 。
若所取小苏打的质量是8.4 g,充分加热后固体质量减少了______ g。
③用三支小试管取适量三种物质加水溶解配制成的溶液,加入少量NaOH溶液,均没有现象,但是有同学认为有一个试管中发生了化学反应,写出其离子方程式____________ 。
(3)Na2CO3俗称“苏打”,市场上销售的“苏打水”是一种非常受欢迎的饮用水,其溶质是NaHCO3(小苏打),而不是苏打(Na2CO3),请你设计一个简单的实验方案进行鉴别:______ 。
(1)有关食盐(NaCl)、纯碱(Na2CO3)和小苏打(NaHCO3)的说法正确的是
A.食盐属于盐、纯碱属于碱、小苏打属于酸
B.分别取三种物质做焰色反应实验,火焰颜色均呈现黄色
C.用三支小试管取适量三种物质加入少量水溶解,用手轻轻触摸试管,温度升高的是纯碱,温度明显降低的是小苏打
D.用三支试管取适量三种物质加入少量水溶解,滴加少量酚酞溶液,溶液变红的只有纯碱
(2)用化学方法鉴别三种物质有很多种方法。
①用三支小试管取适量三种物质加水溶解配制成溶液,加入少量CaCl2溶液,有白色沉淀生成的是纯碱,写出该反应的离子方程式
②用三支小试管取适量三种物质分别加热,有使澄清石灰水变浑浊的气体产生的是小苏打。写出小苏打加热分解的方程式
若所取小苏打的质量是8.4 g,充分加热后固体质量减少了
③用三支小试管取适量三种物质加水溶解配制成的溶液,加入少量NaOH溶液,均没有现象,但是有同学认为有一个试管中发生了化学反应,写出其离子方程式
(3)Na2CO3俗称“苏打”,市场上销售的“苏打水”是一种非常受欢迎的饮用水,其溶质是NaHCO3(小苏打),而不是苏打(Na2CO3),请你设计一个简单的实验方案进行鉴别:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Na2CO3和NaHCO3都是重要的化工原料,在生产和生活中有着广泛的应用。
(1)Na2CO3俗称_______ ,往Na2CO3溶液中滴加酚酞,溶液呈_______ 色。
(2)NaHCO3是常见的膨松剂,为使膨松效果更佳,NaHCO3与醋酸组成复合膨松剂。请用化学方程式说明这种复合膨松剂使面团膨松的原理:_______ 。
(3)实验室中需0.05mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是_______ (填字母,Na2CO3的摩尔质量为106g/mol)。
A.950mL;10.6g B.1000mL;10.6g C.950mL;5.3g D.1000mL;5.3g
某同学配制过程溶液过程中,忘记洗涤烧杯和玻璃棒,直接进行定容操作,将导致所配溶液浓度_______ (填“偏高”“偏低”或“无影响”,下同);另一位同学在定容时俯视容量瓶瓶颈上的刻度线,将导致所配溶液浓度_______ 。
(4)除去Na2CO3粉末中混有的少量NaHCO3的方法是_______ ,化学方程式为_______ 。
(5)在含有一定量NaHCO3和Na2CO3溶质的溶液中,逐滴滴入一定浓度的稀盐酸,产生CO2的物质的量与滴入盐酸的量的关系如图,回答下列问题:

①0~a点发生反应的离子方程式为_______ 。
②a~b点发生反应的离子方程式为_______ 。
③Na2CO3与NaHCO3物质的量之比为_______ 。
(1)Na2CO3俗称
(2)NaHCO3是常见的膨松剂,为使膨松效果更佳,NaHCO3与醋酸组成复合膨松剂。请用化学方程式说明这种复合膨松剂使面团膨松的原理:
(3)实验室中需0.05mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是
A.950mL;10.6g B.1000mL;10.6g C.950mL;5.3g D.1000mL;5.3g
某同学配制过程溶液过程中,忘记洗涤烧杯和玻璃棒,直接进行定容操作,将导致所配溶液浓度
(4)除去Na2CO3粉末中混有的少量NaHCO3的方法是
(5)在含有一定量NaHCO3和Na2CO3溶质的溶液中,逐滴滴入一定浓度的稀盐酸,产生CO2的物质的量与滴入盐酸的量的关系如图,回答下列问题:

①0~a点发生反应的离子方程式为
②a~b点发生反应的离子方程式为
③Na2CO3与NaHCO3物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】胃酸过多是常见的胃病之一,下面是甲、乙两种常见胃药的说明摘要。
甲:(1)白色结晶状粉末,可缓慢分解,焰色反应为黄色;(2)能溶于水水溶液呈弱碱性;(3)遇酸及酸性药物则产生二氧化碳;(4)胃酸过多患者服用多见胃胀气,甚至有引起胃溃疡穿孔的危险。
乙:(1)与胃酸发生中和作用缓慢而持久,可维持3到4小时。(2)凝胶本身覆盖于溃疡面上具有保护作用。(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测甲中含有的主要化学成分是___ ;乙中含有的主要化学成分是___ 。(填化学式)
(2)试写出甲中主要成分引起胃胀气的反应的离子方程式:___ 。
(3)试写出乙中的主要成分与氢氧化钠溶液反应的离子方程式:___ 。
甲:(1)白色结晶状粉末,可缓慢分解,焰色反应为黄色;(2)能溶于水水溶液呈弱碱性;(3)遇酸及酸性药物则产生二氧化碳;(4)胃酸过多患者服用多见胃胀气,甚至有引起胃溃疡穿孔的危险。
乙:(1)与胃酸发生中和作用缓慢而持久,可维持3到4小时。(2)凝胶本身覆盖于溃疡面上具有保护作用。(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测甲中含有的主要化学成分是
(2)试写出甲中主要成分引起胃胀气的反应的离子方程式:
(3)试写出乙中的主要成分与氢氧化钠溶液反应的离子方程式:
您最近一年使用:0次



