人们可以从不同的角度、不同的层面来认识物质的变化。请以2H2+O2 2H2O为例,谈谈你对化学变化的认识
2H2O为例,谈谈你对化学变化的认识____ 。
 2H2O为例,谈谈你对化学变化的认识
2H2O为例,谈谈你对化学变化的认识
更新时间:2022-11-26 14:04:19
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】由化学能产生热能是目前人类使用能源的主要途径。回答下列问题:
(1)图1表示反应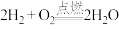 的能量变化。
的能量变化。
已知断开 键、
键、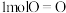 键和
键和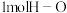 键分别需要消耗
键分别需要消耗 、
、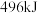 和
和 的能量。则反应过程(Ⅱ)中生成
的能量。则反应过程(Ⅱ)中生成 时放出
时放出_______  能量。
能量。

(2)由 和
和 反应生成
反应生成 和
和 的能量变化如图2所示。其正反应的活化能为
的能量变化如图2所示。其正反应的活化能为_______  ,若反应生成
,若反应生成 ,其
,其
_______  。
。

(3)已知某温度时,反应Ⅰ: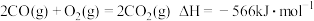 ;
;
反应Ⅱ: 。
。
 与
与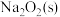 反应生成
反应生成 ,该反应的热化学方程式为
,该反应的热化学方程式为_______ 。
(4)在25℃, 下,一定质量的无水乙醇完全燃烧生成液态水时放出热量
下,一定质量的无水乙醇完全燃烧生成液态水时放出热量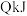 ,其燃烧生成的
,其燃烧生成的 用过量饱和石灰水吸收可得
用过量饱和石灰水吸收可得 沉淀,则乙醇燃烧的热化学方程式为
沉淀,则乙醇燃烧的热化学方程式为_______ 。
(1)图1表示反应
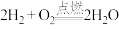 的能量变化。
的能量变化。已知断开
 键、
键、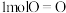 键和
键和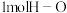 键分别需要消耗
键分别需要消耗 、
、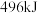 和
和 的能量。则反应过程(Ⅱ)中生成
的能量。则反应过程(Ⅱ)中生成 时放出
时放出 能量。
能量。
(2)由
 和
和 反应生成
反应生成 和
和 的能量变化如图2所示。其正反应的活化能为
的能量变化如图2所示。其正反应的活化能为 ,若反应生成
,若反应生成 ,其
,其
 。
。
(3)已知某温度时,反应Ⅰ:
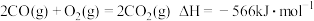 ;
;反应Ⅱ:
 。
。 与
与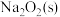 反应生成
反应生成 ,该反应的热化学方程式为
,该反应的热化学方程式为(4)在25℃,
 下,一定质量的无水乙醇完全燃烧生成液态水时放出热量
下,一定质量的无水乙醇完全燃烧生成液态水时放出热量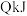 ,其燃烧生成的
,其燃烧生成的 用过量饱和石灰水吸收可得
用过量饱和石灰水吸收可得 沉淀,则乙醇燃烧的热化学方程式为
沉淀,则乙醇燃烧的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】据报道,地暖加热可能会导致室内甲醛的含量升高。地板胶黏剂中含有一定量的甲醛,甲醛对人体有害,但甲醛是一种重要的化工产品,可利用甲醇催化脱氢来制备。甲醛与气态甲醇之间转化的能量关系如图所示。

(1)甲醇催化脱氢转化为甲醛的反应是______ (填“吸热”或“放热”)反应。
(2)过程(Ⅰ)与过程(Ⅱ)的反应热是否相同?_______ (填“相同”或“不相同”),原因是_____________________ 。
(3)写出甲醇催化脱氢转化为甲醛的热化学方程式:______________________________ 。
(4)甲醇催化脱氢转化为甲醛的过程中,如果要使反应温度维持在700 ℃,需向体系中通入空气,则进料甲醇与空气的物质的量的理论比值为____ [假设:H2(g)+  O2(g)
O2(g) H2O(g) ΔH=-a kJ·mol-1,空气中氧气的体积分数为20%]。
H2O(g) ΔH=-a kJ·mol-1,空气中氧气的体积分数为20%]。

(1)甲醇催化脱氢转化为甲醛的反应是
(2)过程(Ⅰ)与过程(Ⅱ)的反应热是否相同?
(3)写出甲醇催化脱氢转化为甲醛的热化学方程式:
(4)甲醇催化脱氢转化为甲醛的过程中,如果要使反应温度维持在700 ℃,需向体系中通入空气,则进料甲醇与空气的物质的量的理论比值为
 O2(g)
O2(g) H2O(g) ΔH=-a kJ·mol-1,空气中氧气的体积分数为20%]。
H2O(g) ΔH=-a kJ·mol-1,空气中氧气的体积分数为20%]。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】已知H2(g)+ O2(g)=H2O(g),如图是1molH2燃烧的反应过程中能量变化示意图。
O2(g)=H2O(g),如图是1molH2燃烧的反应过程中能量变化示意图。

请回答下列问题:
(1)该反应是__ (填“吸热”或“放热”)反应。
(2)氢气在氧气中燃烧,破坏1molH—H键吸收Q1kJ的能量,破坏1molO=O键吸收Q2kJ的能量,形成1molH—O键释放Q3kJ的能量,则下列关系式正确的是___ 。
A.2Q1+Q2>4Q3 B.2Q1+Q2<4Q3
C.Q1+Q2<Q3 D.2Q1+Q2=4Q3
(3)已知1gH2(g)完全燃烧生成水蒸气时放出热量121kJ,且O2(g)中1molO=O键完全断裂时吸收热量496kJ,H2O(g)中1molH—O键形成时放出热量463kJ,则H2(g)中1molH—H键断裂时吸收热量为__ kJ。
 O2(g)=H2O(g),如图是1molH2燃烧的反应过程中能量变化示意图。
O2(g)=H2O(g),如图是1molH2燃烧的反应过程中能量变化示意图。
请回答下列问题:
(1)该反应是
(2)氢气在氧气中燃烧,破坏1molH—H键吸收Q1kJ的能量,破坏1molO=O键吸收Q2kJ的能量,形成1molH—O键释放Q3kJ的能量,则下列关系式正确的是
A.2Q1+Q2>4Q3 B.2Q1+Q2<4Q3
C.Q1+Q2<Q3 D.2Q1+Q2=4Q3
(3)已知1gH2(g)完全燃烧生成水蒸气时放出热量121kJ,且O2(g)中1molO=O键完全断裂时吸收热量496kJ,H2O(g)中1molH—O键形成时放出热量463kJ,则H2(g)中1molH—H键断裂时吸收热量为
您最近一年使用:0次
【推荐2】(1)为探究实验室制氢气反应的热效应,选择如图装置进行实验。
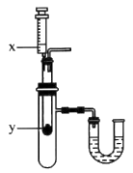
①若x为水,y为生石灰,则实验过程中U形管中可观察到的现象是___________ 。
②若x为稀盐酸,y为锌粒,观察到与①相同的实验现象,则说明锌与稀盐酸制氢气的反应是___________ (填“放热反应”或“吸热反应”)。
(2)太阳能的开发和利用是21世纪的一个重要课题。
①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节。已知下列数据:
其中最适宜作储能介质的是___________ (填字母代号)。
A.CaCl2·6H2O B.Na2SO4·10H2O
C.Na2HPO4·12H2O D.Na2S2O3·5H2O
②如图是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器。根据对水的密度的认识,你估计在阳光照射下水将沿___________ (填“顺”或“逆”)时针方向流动。

(3)反应产生的H2可用于工业合成氨气。已知拆开1mol H-H键、1molN≡N键分别需要吸收的能量为436kJ、946kJ,形成1molN-H键会放出能量391kJ,则在反应N2+3H2 2NH3中,每生成2molNH3
2NH3中,每生成2molNH3___________ (填“吸收”或“放出”)热量___________ kJ。当在相同的条件下向容器中充入1molN2和3molH2时,它们反应对应的热量___________ (填“大于”、“等于”或“小于”)所计算出的值。

①若x为水,y为生石灰,则实验过程中U形管中可观察到的现象是
②若x为稀盐酸,y为锌粒,观察到与①相同的实验现象,则说明锌与稀盐酸制氢气的反应是
(2)太阳能的开发和利用是21世纪的一个重要课题。
①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节。已知下列数据:
| 盐 | 熔点/oC | 熔化吸热/kJ·mol-1 | 参考价格/元·kg-1 |
| CaCl2·6H2O | 29.0 | 37.3 | 780~850 |
| Na2SO4·10H2O | 32.4 | 77.0 | 800~900 |
| Na2HPO4·12H2O | 36.1 | 100.1 | 1 600~2 000 |
| Na2S2O3·5H2O | 48.5 | 49.7 | 1 400~1 800 |
A.CaCl2·6H2O B.Na2SO4·10H2O
C.Na2HPO4·12H2O D.Na2S2O3·5H2O
②如图是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器。根据对水的密度的认识,你估计在阳光照射下水将沿

(3)反应产生的H2可用于工业合成氨气。已知拆开1mol H-H键、1molN≡N键分别需要吸收的能量为436kJ、946kJ,形成1molN-H键会放出能量391kJ,则在反应N2+3H2
 2NH3中,每生成2molNH3
2NH3中,每生成2molNH3
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】化学反应中的能量变化通常表现为热量的变化。回答下列问题:
(1)已知: 、
、 、
、 各
各 分别与足量水反应热量变化依次为
分别与足量水反应热量变化依次为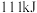 、
、 、
、 。
。
①固态钠与水反应的热化学方程式为_______ 。
②钠、钾与水反应,钠、钾均熔化为球状,而锂与水反应,锂始终为固体,下列可解释这一事实的是_______ (填标号)。
A.锂的密度比钠、钾的大
B.锂的熔点比钠、钾的高得多,实验条件下产生的热量不足以使其熔化
C.锂与水的反应是吸热反应,钠、钾与水的反应是放热反应
D.相同质量时,锂与水反应产生的热量比钠、钾的少
(2) 和
和 在铁催化剂表面合成氨的相关能量与反应历程如图所示(其中吸附在
在铁催化剂表面合成氨的相关能量与反应历程如图所示(其中吸附在 催化剂表面上的物种用
催化剂表面上的物种用 标注):
标注):
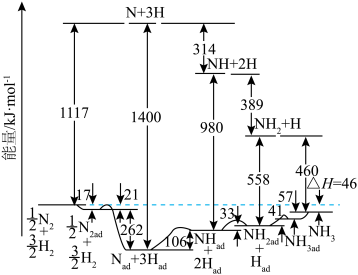
① 和
和 合成
合成 的热化学方程式为
的热化学方程式为_______ 。
②下列反应历程中,吸热的是_______ (填标号)。
A. B.
B.
C.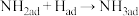 D.
D.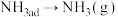
③键能通常是指在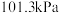 和
和 下,将
下,将 气态分子拆开成气态原子时,每个键所需能量的平均值,
气态分子拆开成气态原子时,每个键所需能量的平均值, 中
中 键的平均键能为
键的平均键能为_______  (保留一位小数)。
(保留一位小数)。
(3)向量热计中加入 盐酸(溶液温度
盐酸(溶液温度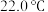 ),再迅速加入相同温度
),再迅速加入相同温度 溶液,盖上杯盖,匀速搅拌,测得最高温度为
溶液,盖上杯盖,匀速搅拌,测得最高温度为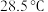 ,设该盐酸和
,设该盐酸和 溶液的密度均为
溶液的密度均为 ,溶液的比热容为
,溶液的比热容为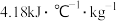 。由实验数据可得出每反应生成
。由实验数据可得出每反应生成 的
的 为
为_______ (保留一位小数)。
(1)已知:
 、
、 、
、 各
各 分别与足量水反应热量变化依次为
分别与足量水反应热量变化依次为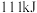 、
、 、
、 。
。①固态钠与水反应的热化学方程式为
②钠、钾与水反应,钠、钾均熔化为球状,而锂与水反应,锂始终为固体,下列可解释这一事实的是
A.锂的密度比钠、钾的大
B.锂的熔点比钠、钾的高得多,实验条件下产生的热量不足以使其熔化
C.锂与水的反应是吸热反应,钠、钾与水的反应是放热反应
D.相同质量时,锂与水反应产生的热量比钠、钾的少
(2)
 和
和 在铁催化剂表面合成氨的相关能量与反应历程如图所示(其中吸附在
在铁催化剂表面合成氨的相关能量与反应历程如图所示(其中吸附在 催化剂表面上的物种用
催化剂表面上的物种用 标注):
标注):
①
 和
和 合成
合成 的热化学方程式为
的热化学方程式为②下列反应历程中,吸热的是
A.
 B.
B.
C.
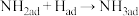 D.
D.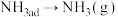
③键能通常是指在
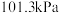 和
和 下,将
下,将 气态分子拆开成气态原子时,每个键所需能量的平均值,
气态分子拆开成气态原子时,每个键所需能量的平均值, 中
中 键的平均键能为
键的平均键能为 (保留一位小数)。
(保留一位小数)。(3)向量热计中加入
 盐酸(溶液温度
盐酸(溶液温度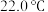 ),再迅速加入相同温度
),再迅速加入相同温度 溶液,盖上杯盖,匀速搅拌,测得最高温度为
溶液,盖上杯盖,匀速搅拌,测得最高温度为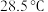 ,设该盐酸和
,设该盐酸和 溶液的密度均为
溶液的密度均为 ,溶液的比热容为
,溶液的比热容为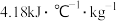 。由实验数据可得出每反应生成
。由实验数据可得出每反应生成 的
的 为
为
您最近一年使用:0次




