为测定某抗胃酸药片中碳酸钙的质量分数(设该药片中的其他成分不与盐酸或氢氧化钠反应):
I.向0.1000 g药片粉末中依次加入20.00 mL蒸馏水、25.00 mL 0.1000 mol/L稀盐酸,使之充分反应。
II.中和过量的盐酸,消耗0.1000 mol/L NaOH溶液13.00 mL。
请计算:
(1)II中消耗NaOH的物质的量为_______ mol。
(2)0.1000 g药片消耗HCl的物质的量为_______ mol。
(3)药片中碳酸钙的质量分数为_______ 。
I.向0.1000 g药片粉末中依次加入20.00 mL蒸馏水、25.00 mL 0.1000 mol/L稀盐酸,使之充分反应。
II.中和过量的盐酸,消耗0.1000 mol/L NaOH溶液13.00 mL。
请计算:
(1)II中消耗NaOH的物质的量为
(2)0.1000 g药片消耗HCl的物质的量为
(3)药片中碳酸钙的质量分数为
更新时间:2022/12/07 20:43:28
|
相似题推荐
【推荐1】钠及其化合物在生产、生活中有着重要的应用。
(1)钠是一种银白色的金属,取2.3g钠块在干燥空气中放置一段时间后,其表面会失去金属光泽生成 ,此时固体质量为2.46g,则原钠块中已被氧化的钠为
,此时固体质量为2.46g,则原钠块中已被氧化的钠为_______ mol;再将该钠块在干燥空气中充分加热,会得到浅黄色的_______ (填化学式)粉末;经过上述两步实验后,最终得到的粉末的质量应为_______ g。
(2)某课外小组为了验证 和
和 的稳定性,设计如下图所示的实验装置
的稳定性,设计如下图所示的实验装置

①为使实验更具有说服力,你认为在试管A中最好放物质_______ (填化学式),在AB试管中能发生的反应的化学方程式为_______ 。
②实验时,C、D两个烧杯中的现象分别是_______ ,可以证明碳酸钠比碳酸氢钠稳定。
(1)钠是一种银白色的金属,取2.3g钠块在干燥空气中放置一段时间后,其表面会失去金属光泽生成
 ,此时固体质量为2.46g,则原钠块中已被氧化的钠为
,此时固体质量为2.46g,则原钠块中已被氧化的钠为(2)某课外小组为了验证
 和
和 的稳定性,设计如下图所示的实验装置
的稳定性,设计如下图所示的实验装置
①为使实验更具有说服力,你认为在试管A中最好放物质
②实验时,C、D两个烧杯中的现象分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铝是一种重要的金属。
(1)铝在元素周期表中的位置是________ 。
(2)生产中曾用铝热反应焊接钢轨,铝与氧化铁发生反应的化学方程式为________________ 。
(3)铝与NaOH溶液反应的离子方程式为:______________ ;
同温同压下,在浓度和体积均为100 mL 2 mol/L的盐酸及NaOH溶液中各加入等质量的Al,产生气体的体积比为5:6,则所加Al的质量为________ 。
(1)铝在元素周期表中的位置是
(2)生产中曾用铝热反应焊接钢轨,铝与氧化铁发生反应的化学方程式为
(3)铝与NaOH溶液反应的离子方程式为:
同温同压下,在浓度和体积均为100 mL 2 mol/L的盐酸及NaOH溶液中各加入等质量的Al,产生气体的体积比为5:6,则所加Al的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】1.74 g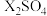 中含X+ 0.02 mol,则
中含X+ 0.02 mol,则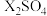 的摩尔质量为
的摩尔质量为_____ ,X的相对原子质量为____ mol• L-1。将质量为17.4 g的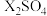 溶于水配制成100 mL溶液,溶质的物质的量浓度为
溶于水配制成100 mL溶液,溶质的物质的量浓度为___ mol •L-1。
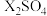 中含X+ 0.02 mol,则
中含X+ 0.02 mol,则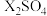 的摩尔质量为
的摩尔质量为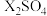 溶于水配制成100 mL溶液,溶质的物质的量浓度为
溶于水配制成100 mL溶液,溶质的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知硫粉和 溶液反应可以生成多硫化钠(
溶液反应可以生成多硫化钠(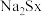 ),离子反应为:
),离子反应为: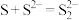 、
、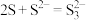 ,现有1.11 mol/L
,现有1.11 mol/L  溶液200mL,往其中加入13.44 g硫粉,控制一定条件使硫粉恰好完全反应,反应后溶液的阴离子有
溶液200mL,往其中加入13.44 g硫粉,控制一定条件使硫粉恰好完全反应,反应后溶液的阴离子有 、
、 、
、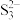 (忽略其他阴离子,假设溶液体积不变),且物质的量之比为1∶10∶100,请计算:
(忽略其他阴离子,假设溶液体积不变),且物质的量之比为1∶10∶100,请计算:
(1)加入硫粉的物质的量: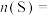
______ mol。
(2)反应后:
______ mol。
(3)反应后:
______ mol/L。
 溶液反应可以生成多硫化钠(
溶液反应可以生成多硫化钠(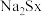 ),离子反应为:
),离子反应为: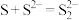 、
、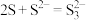 ,现有1.11 mol/L
,现有1.11 mol/L  溶液200mL,往其中加入13.44 g硫粉,控制一定条件使硫粉恰好完全反应,反应后溶液的阴离子有
溶液200mL,往其中加入13.44 g硫粉,控制一定条件使硫粉恰好完全反应,反应后溶液的阴离子有 、
、 、
、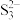 (忽略其他阴离子,假设溶液体积不变),且物质的量之比为1∶10∶100,请计算:
(忽略其他阴离子,假设溶液体积不变),且物质的量之比为1∶10∶100,请计算:(1)加入硫粉的物质的量:
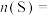
(2)反应后:

(3)反应后:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】判断下列溶液配制的误差(填“大于”“小于”或“等于”):
(1)将6.0g冰醋酸加水配成100mL溶液,所得溶液中H+的浓度_____ 1mol/L
(2)将18.4mol/L浓硫酸加等体积水稀释,所得溶液中 的浓度
的浓度_____ 9.2mol/L
(3)将46mL乙醇(密度0.8g/cm3)溶于500mL水,所得溶液的浓度_____ 1.6mol/L
(4)将某温度下的50mL 2mol/L CuSO4饱和溶液降温结晶,析出8g晶体,则剩余溶液的浓度____ 1mol/L
(1)将6.0g冰醋酸加水配成100mL溶液,所得溶液中H+的浓度
(2)将18.4mol/L浓硫酸加等体积水稀释,所得溶液中
 的浓度
的浓度(3)将46mL乙醇(密度0.8g/cm3)溶于500mL水,所得溶液的浓度
(4)将某温度下的50mL 2mol/L CuSO4饱和溶液降温结晶,析出8g晶体,则剩余溶液的浓度
您最近一年使用:0次



