H2O是生命之源,对于下列涉及H2O的反应,请回答:
(1)下列某同学关于H2O的认识正确的是_____ (填选项序号)。
A.H2O属于非电解质
B.H2O既有氧化性也有还原性
C.水在Al(OH)3胶体中是分散剂,在雾中是分散质
(2)工业上利用反应C+H2O CO+H2制取水煤气,反应中的水作
CO+H2制取水煤气,反应中的水作_____ (选填“氧化剂”、“还原剂”、“氧化剂和还原剂”,下同)。
(3)单质铁可以和水蒸气发生反应,反应的化学方程式为:_____ ,当标况下产生8.96LH2时,消耗的铁的质量为_____ 。
(4)登山运动员常携带氢化钙作为生氢剂,反应方程式:CaH2+2H2O=Ca(OH)2+2H2↑,反应中的CaH2作_____ ,若反应中消耗4molH2O,反应中转移电子的数目为_____ 。
(1)下列某同学关于H2O的认识正确的是
A.H2O属于非电解质
B.H2O既有氧化性也有还原性
C.水在Al(OH)3胶体中是分散剂,在雾中是分散质
(2)工业上利用反应C+H2O
 CO+H2制取水煤气,反应中的水作
CO+H2制取水煤气,反应中的水作(3)单质铁可以和水蒸气发生反应,反应的化学方程式为:
(4)登山运动员常携带氢化钙作为生氢剂,反应方程式:CaH2+2H2O=Ca(OH)2+2H2↑,反应中的CaH2作
更新时间:2022-12-13 22:09:55
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有以下物质:a.NaOH溶液,b.液氨,c.Ba(OH)2固体,d.NaHSO4,e.Fe(OH)3胶体,f.铜,g.CO2,h.CH3COOH。
(1)①以上物质中属于非电解质的是_______ (填序号,下同),属于强电解质的有_______ 。
②写出d在水溶液中电离方程式_______ 。
③在足量d的水溶液中加入少量c的水溶液,发生反应的离子方程式为_______ 。
④在含a的水溶液中缓缓通少量CO2,该过程的离子反应方程式为_______ 。
(2)向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体。
①制取Fe(OH)3胶体的离子方程式为_______ 。
②下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔效应
区分胶体和溶液的方法是_______ (填字母,下同);“卤水点豆腐”,利用的性质是_______ (填字母,下同);工厂采用高压静电除尘,利用的胶体性质是_______ 。
(1)①以上物质中属于非电解质的是
②写出d在水溶液中电离方程式
③在足量d的水溶液中加入少量c的水溶液,发生反应的离子方程式为
④在含a的水溶液中缓缓通少量CO2,该过程的离子反应方程式为
(2)向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体。
①制取Fe(OH)3胶体的离子方程式为
②下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔效应
区分胶体和溶液的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】高铁酸钠( );是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为
);是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为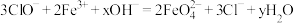 。回答下列问题:
。回答下列问题:
(1)上述反应中的y=___________ 。
(2)上述反应中氧化剂为___________ ;还原产物为___________ 。
(3)由上述反应可知,氧化性强弱:
___________ (填“>”或“<”,下同) ;还原性强弱:
;还原性强弱:
___________  。
。
(4)请用单线桥法表示该反应中电子的转移情况:___________ 。
(5)已知: 在处理饮用水的过程中铁元素会被转化为
在处理饮用水的过程中铁元素会被转化为 ,进而
,进而 在水中产生
在水中产生 月胶体,
月胶体, 胶体具有吸附性。
胶体具有吸附性。
① 在处理饮用水的过程中
在处理饮用水的过程中___________ (填“发生了”或“未发生”)氧化还原反应。
② 胶体为
胶体为___________ 色,写出区分胶体与溶液的操作及现象:___________ 。
 );是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为
);是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为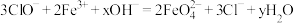 。回答下列问题:
。回答下列问题:(1)上述反应中的y=
(2)上述反应中氧化剂为
(3)由上述反应可知,氧化性强弱:

 ;还原性强弱:
;还原性强弱:
 。
。(4)请用单线桥法表示该反应中电子的转移情况:
(5)已知:
 在处理饮用水的过程中铁元素会被转化为
在处理饮用水的过程中铁元素会被转化为 ,进而
,进而 在水中产生
在水中产生 月胶体,
月胶体, 胶体具有吸附性。
胶体具有吸附性。①
 在处理饮用水的过程中
在处理饮用水的过程中②
 胶体为
胶体为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有以下物质:①NaOH溶液②液氨③BaCO3固体④熔融KHSO4⑤Fe(OH)3胶体⑥铜⑦CO2⑧稀醋酸(CH3COOH)⑨饱和NaHCO3溶液⑩乙醇,请回答下列问题。
(1)物质中属于电解质的是_______ ,非电解质的是_______ ,强电解质的是________ 。(均填序号)
(2)写出⑨和KHSO4溶液反应的离子方程式:_______ 。写出①和⑨反应的离子方程式:________ 。
(3)写出④的电离方程式:________ 。
(4)⑤的实验室制备方案:向沸水中滴加几滴________ 溶液,加热至液体呈红褐色,停止加热;其化学方程式为_________ 。
(5)在足量①的水溶液中通入少量⑦,发生反应的离子方程式为________ 。现有11g⑦发生上述反应,需要消耗①的溶质的物质的量为__________ mol。
(1)物质中属于电解质的是
(2)写出⑨和KHSO4溶液反应的离子方程式:
(3)写出④的电离方程式:
(4)⑤的实验室制备方案:向沸水中滴加几滴
(5)在足量①的水溶液中通入少量⑦,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】阅读下列科普短文并填空。
氢氧燃料电池是一种化学电池,具有能量转化率高、对环境友好等优点。例如,该电池在工作时,从负极连续通入 ,从正极连续通入
,从正极连续通入 ,二者在电池内部(含有
,二者在电池内部(含有 或
或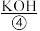 等物质的溶液)发生反应生成
等物质的溶液)发生反应生成 ,同时产生电能。除了
,同时产生电能。除了 ,
, 、
、 等也可以作为燃料电池的燃料。目前已研制成功
等也可以作为燃料电池的燃料。目前已研制成功 燃料电池,它可以代替汽油
燃料电池,它可以代替汽油 为汽车提供动力,也可以用作照明电源等。
为汽车提供动力,也可以用作照明电源等。
(1)在上述短文标有序号的物质中,属于混合物的是___________ (填序号下同);属于氧化物的是___________ ;
(2)属于有机物的是___________ ;属于电解质的是___________ ;
(3)⑧与④的水溶液也能反应生成 和一种气体。写出该反应的化学方程式:
和一种气体。写出该反应的化学方程式:___________ 。
氢氧燃料电池是一种化学电池,具有能量转化率高、对环境友好等优点。例如,该电池在工作时,从负极连续通入
 ,从正极连续通入
,从正极连续通入 ,二者在电池内部(含有
,二者在电池内部(含有 或
或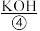 等物质的溶液)发生反应生成
等物质的溶液)发生反应生成 ,同时产生电能。除了
,同时产生电能。除了 ,
, 、
、 等也可以作为燃料电池的燃料。目前已研制成功
等也可以作为燃料电池的燃料。目前已研制成功 燃料电池,它可以代替汽油
燃料电池,它可以代替汽油 为汽车提供动力,也可以用作照明电源等。
为汽车提供动力,也可以用作照明电源等。(1)在上述短文标有序号的物质中,属于混合物的是
(2)属于有机物的是
(3)⑧与④的水溶液也能反应生成
 和一种气体。写出该反应的化学方程式:
和一种气体。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
下列物质:①BaSO4 ②空气 ③铁 ④二氧化碳 ⑤硝酸 ⑥液氨 ⑦熔融NaCl ⑧FeCl3溶液 ⑨油脂 ⑩碳酸氢钠(NaHCO3)
(1)属于电解质的是___________ ,属于非电解质的是_______
(2)铝与氢氧化钠溶液反应的方程式___________ 。等质量Fe、A1分别与足量的稀盐酸反应,生成的气体的体积比为___________ (同温同压)。体积比为2:1,物质的量浓度相同的FeCl3、AlCl3溶液中 的物质的量浓度之比为
的物质的量浓度之比为_____
(3)某元素的一种同位素X原子的质量数为A,含N个中子,它与2H原子组成2HmX分子,在ag2HmX分子中含质子的物质的量是_____
(4)同温同压下,某容器充满氧气重116g,若充满二氧化碳重122g,现充满某气体重114g,则该气体的摩尔质量为_____
(5)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为_____
下列物质:①BaSO4 ②空气 ③铁 ④二氧化碳 ⑤硝酸 ⑥液氨 ⑦熔融NaCl ⑧FeCl3溶液 ⑨油脂 ⑩碳酸氢钠(NaHCO3)
(1)属于电解质的是
(2)铝与氢氧化钠溶液反应的方程式
 的物质的量浓度之比为
的物质的量浓度之比为(3)某元素的一种同位素X原子的质量数为A,含N个中子,它与2H原子组成2HmX分子,在ag2HmX分子中含质子的物质的量是
(4)同温同压下,某容器充满氧气重116g,若充满二氧化碳重122g,现充满某气体重114g,则该气体的摩尔质量为
(5)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)有下列四组物质①水、酒精、煤、石油 ②CaO、SO3、SO2、P2O5 ③HNO3、H2SO4、HCl、NaCl ④KClO3、KCl、KMnO4、HgO各组中均有一种物质所属类别与其他物质不同,这四种物质分别是:
①________ ;②________ ;③________ ;④________ 。
(2)有下列八种物质:
①NaOH溶液 ②铁丝 ③液态HCl ④熔融氯化钠 ⑤硫酸钠固体 ⑥CO2 ⑦酒精 ⑧生石灰
上述物质中,可导电的是________ (填序号,下同),属于非电解质的是________ ,属于电解质但在该状态下不导电的是________ 。
①
(2)有下列八种物质:
①NaOH溶液 ②铁丝 ③液态HCl ④熔融氯化钠 ⑤硫酸钠固体 ⑥CO2 ⑦酒精 ⑧生石灰
上述物质中,可导电的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列各题。
(1)次磷酸钠(NaH2PO2)可用于化学镀镍,即通过化学反应在塑料镀件表面沉积镍磷合金。化学镀镍的溶液中含有Ni2+和 ,在酸性条件下发生以下镀镍反应,请配平此化学方程式:
,在酸性条件下发生以下镀镍反应,请配平此化学方程式:_____ ,Ni2++ +____→Ni+
+____→Ni+ +____,反应中,若生成1mol
+____,反应中,若生成1mol ,转移电子的物质的量为
,转移电子的物质的量为_____ mol。
(2)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请配平该化学方程式:_______ ,FeSO4+KNO3+H2SO4 K2SO4+Fe2(SO4)3+NO↑+H2O,其中氧化剂为
K2SO4+Fe2(SO4)3+NO↑+H2O,其中氧化剂为_______ (填化学式)。
(3)铁红是一种红色颜料,其成分是Fe2O3,将一定量铁红溶于160mL5mol·L-1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况)气体,经检测,溶液中无Fe3+,则参加反应的铁粉的质量为_______ g。
(1)次磷酸钠(NaH2PO2)可用于化学镀镍,即通过化学反应在塑料镀件表面沉积镍磷合金。化学镀镍的溶液中含有Ni2+和
 ,在酸性条件下发生以下镀镍反应,请配平此化学方程式:
,在酸性条件下发生以下镀镍反应,请配平此化学方程式: +____→Ni+
+____→Ni+ +____,反应中,若生成1mol
+____,反应中,若生成1mol ,转移电子的物质的量为
,转移电子的物质的量为(2)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请配平该化学方程式:
 K2SO4+Fe2(SO4)3+NO↑+H2O,其中氧化剂为
K2SO4+Fe2(SO4)3+NO↑+H2O,其中氧化剂为(3)铁红是一种红色颜料,其成分是Fe2O3,将一定量铁红溶于160mL5mol·L-1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况)气体,经检测,溶液中无Fe3+,则参加反应的铁粉的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】科学家也在尝试用 作催化剂,将汽车尾气中NO转化为无毒的N2。其原理如下图所示:
作催化剂,将汽车尾气中NO转化为无毒的N2。其原理如下图所示:

(1)该过程中,还原剂是_______ (用化学式表示)。
(2)某辆汽车的NO排放量为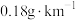 ,则该车行驶100km,完成上述转化时,理论上需消耗乙烯的质量为
,则该车行驶100km,完成上述转化时,理论上需消耗乙烯的质量为_______ g。
 作催化剂,将汽车尾气中NO转化为无毒的N2。其原理如下图所示:
作催化剂,将汽车尾气中NO转化为无毒的N2。其原理如下图所示:
(1)该过程中,还原剂是
(2)某辆汽车的NO排放量为
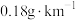 ,则该车行驶100km,完成上述转化时,理论上需消耗乙烯的质量为
,则该车行驶100km,完成上述转化时,理论上需消耗乙烯的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】完成下列各小题。
(1)将NaBiO3固体(黄色,微溶)加入MnSO4和H2SO4的混合溶液里,加热,溶液显紫色(Bi3+无色)。配平该反应的离子方程式:_____ 。
 NaBiO3+
NaBiO3+ Mn2++
Mn2++ ________→
________→ Na++
Na++ Bi3++
Bi3++ ________+
________+ ________。
________。
(2)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:_____ 。
 FeO
FeO +
+ H2O=
H2O= Fe(OH)3(胶体)+
Fe(OH)3(胶体)+ O2↑+
O2↑+ OH-。
OH-。
(3)以亚氯酸钠和稀盐酸为原料制备ClO2,反应原理为5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O。该反应中氧化剂和还原剂的物质的量之比为_____ 。
(4)在含VO2+的溶液中加入KClO3,可使VO2+转化为VO ,则欲使3molVO2+变成VO
,则欲使3molVO2+变成VO ,需要氧化剂KClO3至少为
,需要氧化剂KClO3至少为_____ mol。
(5)已知M2O 可与R2-作用,R2-被氧化为R单质,M2O
可与R2-作用,R2-被氧化为R单质,M2O 的还原产物中M为+3价;又知c(M2O
的还原产物中M为+3价;又知c(M2O )=0.3mol•L-1的溶液100mL可与c(R2-)=0.6mol•L-1的溶液150mL恰好完全反应,则n值为
)=0.3mol•L-1的溶液100mL可与c(R2-)=0.6mol•L-1的溶液150mL恰好完全反应,则n值为_____ 。
(1)将NaBiO3固体(黄色,微溶)加入MnSO4和H2SO4的混合溶液里,加热,溶液显紫色(Bi3+无色)。配平该反应的离子方程式:
 NaBiO3+
NaBiO3+ Mn2++
Mn2++ ________→
________→ Na++
Na++ Bi3++
Bi3++ ________+
________+ ________。
________。(2)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:
 FeO
FeO +
+ H2O=
H2O= Fe(OH)3(胶体)+
Fe(OH)3(胶体)+ O2↑+
O2↑+ OH-。
OH-。(3)以亚氯酸钠和稀盐酸为原料制备ClO2,反应原理为5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O。该反应中氧化剂和还原剂的物质的量之比为
(4)在含VO2+的溶液中加入KClO3,可使VO2+转化为VO
 ,则欲使3molVO2+变成VO
,则欲使3molVO2+变成VO ,需要氧化剂KClO3至少为
,需要氧化剂KClO3至少为(5)已知M2O
 可与R2-作用,R2-被氧化为R单质,M2O
可与R2-作用,R2-被氧化为R单质,M2O 的还原产物中M为+3价;又知c(M2O
的还原产物中M为+3价;又知c(M2O )=0.3mol•L-1的溶液100mL可与c(R2-)=0.6mol•L-1的溶液150mL恰好完全反应,则n值为
)=0.3mol•L-1的溶液100mL可与c(R2-)=0.6mol•L-1的溶液150mL恰好完全反应,则n值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有NH3、CO、Na、Na2O2、Fe、NO、NO2、F2、SO2、SOCl2等中学化学中出现过的物质,根据它们的组成及性质进行如下分类:
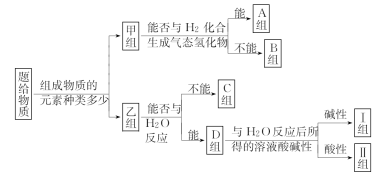
请回答下列问题:
(1)图中所示的分类方法叫_______________________ 。
(2)淡黄色固体最终位于________ 组,它的电子式为______________ 。
(3)C组有一种气体常用作工业上冶炼铁的还原剂,写出高温下它还原Fe2O3的化学方程式:_____________________________________ 。
(4)Ⅱ组某种物质能与水发生氧化还原反应,该反应中被氧化与被还原的元素的质量比为______________________________________ 。
(5)B组中有一种物质在高温下能与水蒸气反应,若该反应过程中有8×6.02× 1023个电子转移,则有________ g该物质参与反应。

请回答下列问题:
(1)图中所示的分类方法叫
(2)淡黄色固体最终位于
(3)C组有一种气体常用作工业上冶炼铁的还原剂,写出高温下它还原Fe2O3的化学方程式:
(4)Ⅱ组某种物质能与水发生氧化还原反应,该反应中被氧化与被还原的元素的质量比为
(5)B组中有一种物质在高温下能与水蒸气反应,若该反应过程中有8×6.02× 1023个电子转移,则有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钾、钠、镁、铁均能与水发生置换H2的反应。
(1)其中反应最剧烈的是____ 。
(2)其中铁与水的反应比较特殊。其特殊性在于:
①_________ ;②产物为氧化物而非氢氧化物。你对②和①的关联性作何解释?__________
(3)证明②的氧化物含Fe3+必需的试剂是______ 。
(1)其中反应最剧烈的是
(2)其中铁与水的反应比较特殊。其特殊性在于:
①
(3)证明②的氧化物含Fe3+必需的试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.(1)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为___________ 。
(2)在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)分别用p(Ne)、p(H2)、p(O2)表示,由大到小的顺序是___________ 。
II.按要求填空:
(1)还原铁粉与高温水蒸气反应的化学方程式:___________ ;
(2)在酸性条件下,向含铬废水中加入FeSO4,可将Cr2O 还原为Cr3+,该过程的离子反应方程式为:
还原为Cr3+,该过程的离子反应方程式为:______
(3)在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为:______
(2)在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)分别用p(Ne)、p(H2)、p(O2)表示,由大到小的顺序是
II.按要求填空:
(1)还原铁粉与高温水蒸气反应的化学方程式:
(2)在酸性条件下,向含铬废水中加入FeSO4,可将Cr2O
 还原为Cr3+,该过程的离子反应方程式为:
还原为Cr3+,该过程的离子反应方程式为:(3)在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为:
您最近一年使用:0次



