SO2是重要的化工原料,回收利用SO2既能减少大气污染,又能充分利用资源。
(1)向食品中添加适量的SO2可以起到防腐、漂白、抗氧化的作用,则葡萄酒中添加适量的SO2的作用是____ 。
(2)SO2性质多变,若将SO2气体通入H2S溶液中,能观察到的现象为______ ,该反应中SO2表现出_______ 性;若将SO2气体通入品红溶液中,能观察到现象为_____ ,该反应中SO2表现出_______ 性。
(3)有学者提出利用Fe3+、Fe2+等离子的作用,在常温下将SO2氧化成 而实现SO2的回收利用。写出Fe3+将SO2氧化成
而实现SO2的回收利用。写出Fe3+将SO2氧化成 反应的离子方程式:
反应的离子方程式:_______ 。
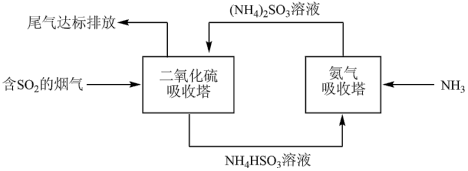
(4)SO2有毒,且能形成酸雨,是大气主要污染物之一。某企业利用下列流程综合处理工厂排放的含SO2的烟气,以减少其对环境造成的污染。“氨气吸收塔”中发生反应的化学方程式为_______ ,该流程中可循环利用的物质为_______ (填化学式)。
(1)向食品中添加适量的SO2可以起到防腐、漂白、抗氧化的作用,则葡萄酒中添加适量的SO2的作用是
(2)SO2性质多变,若将SO2气体通入H2S溶液中,能观察到的现象为
(3)有学者提出利用Fe3+、Fe2+等离子的作用,在常温下将SO2氧化成
 而实现SO2的回收利用。写出Fe3+将SO2氧化成
而实现SO2的回收利用。写出Fe3+将SO2氧化成 反应的离子方程式:
反应的离子方程式:(4)SO2有毒,且能形成酸雨,是大气主要污染物之一。某企业利用下列流程综合处理工厂排放的含SO2的烟气,以减少其对环境造成的污染。“氨气吸收塔”中发生反应的化学方程式为

更新时间:2022-12-16 12:09:09
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求填写:
(1) 我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按照一定比例混合而成的,爆炸时的化学反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。该反应中氧化剂是_____ ,还原剂是______ ,_____ 元素被氧化,每生成6.72LCO2(标准状况下)气体需要__ g硫参加反应,并用双线桥法来表示电子转移的方向和数目:______ 。
(2)铁是人类较早使用的金属之一。
①鉴别 胶体和
胶体和 溶液的常用方法是
溶液的常用方法是_____ ,两者本质区别是_____ 。
②电子工业中用 溶液腐蚀敷在绝缘板上的铜生产氯化亚铁和氯化铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜生产氯化亚铁和氯化铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式______ 。
③ 胶体制备实验:
胶体制备实验:
实验步骤:取一个小烧杯,加入25mL蒸馏水。将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴FeCl3饱和溶液。继续煮沸。
实验现象:烧杯中溶液呈_____ 色;化学方程式:_____ 。
(1) 我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按照一定比例混合而成的,爆炸时的化学反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。该反应中氧化剂是
(2)铁是人类较早使用的金属之一。
①鉴别
 胶体和
胶体和 溶液的常用方法是
溶液的常用方法是②电子工业中用
 溶液腐蚀敷在绝缘板上的铜生产氯化亚铁和氯化铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜生产氯化亚铁和氯化铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式③
 胶体制备实验:
胶体制备实验:实验步骤:取一个小烧杯,加入25mL蒸馏水。将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴FeCl3饱和溶液。继续煮沸。
实验现象:烧杯中溶液呈
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有以下物质:①FeCl3;②稀NaOH溶液;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;⑦稀盐酸;⑧纯醋酸;⑨Na2CO3;
(1)其中能导电的是____________ ;属于非电解质的是______________ ;属于强电解质的是____________ ;属于弱电解质的是______________ 。
(2)写出物质⑥溶于水的电离方程式:___________________ 。
(3)写出物质⑥和⑧在水中反应的离子方程式__________________ 。
(4)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______
(5)现取0.1mol样品⑨,逐滴加入⑦,现象为_________ ,其所发生的离子方程式为___ 。完全反应时生成气体的物质的量为__________ 。
(1)其中能导电的是
(2)写出物质⑥溶于水的电离方程式:
(3)写出物质⑥和⑧在水中反应的离子方程式
(4)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是
(5)现取0.1mol样品⑨,逐滴加入⑦,现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】使用相关化学用语回答下列问题:
(1)用化学方程式表示金属钠的工业制法:___________ ;
(2)用化学方程式表示高炉炼铁的反应原理:___________ ;
(3)实验室使用 和浓盐酸制备氯气的反应离子方程式:
和浓盐酸制备氯气的反应离子方程式:___________ ;
(4)通过氯碱工业制备氯气的离子方程式:___________ ;
(5)用化学方程式表示氨气实验室制法的反应原理:___________ ;
(6)实验室制乙烯的化学反应方程式:___________ ;
(7)实验室制乙炔的化学反应方程式:___________ ;
(8)泡沫灭火器反应原理的离子方程式:___________ 。
(1)用化学方程式表示金属钠的工业制法:
(2)用化学方程式表示高炉炼铁的反应原理:
(3)实验室使用
 和浓盐酸制备氯气的反应离子方程式:
和浓盐酸制备氯气的反应离子方程式:(4)通过氯碱工业制备氯气的离子方程式:
(5)用化学方程式表示氨气实验室制法的反应原理:
(6)实验室制乙烯的化学反应方程式:
(7)实验室制乙炔的化学反应方程式:
(8)泡沫灭火器反应原理的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】
(1)某建筑材料,主要成分铝硅酸盐,化学式MgAl2H4Si4O14,化学式改写成氧化物形式为_____________ 。则材料该与足量的氢氧化钠反应后过滤,滤渣主要是______ .写出该过程中发生的离子方程式_______________________________ 、_______________________________________ 。
(2)检验CO2中是否混有SO2可将气体通过盛有______ 的洗气瓶.
(3)鉴别Na2CO3和NaHCO3溶液可选用______ (填序号).
①NaOH ②Ca(OH)2 ③BaCl2 ④K2SO4 ⑤Ca(NO3)2
(4)某溶液中有NH4+,Mg2+,Fe2+,Al3+四种离子,若向其中加入过量的氢氧化钠溶液,加热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是______ .
A.NH B.Mg2+ C.Fe2+ D.Al3+
B.Mg2+ C.Fe2+ D.Al3+
(5)6.4gCu与过量硝酸(60mL 8mol/L)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中所含H+为n mol,NO、NO2混合气体的物质的量为________________ 。
(1)某建筑材料,主要成分铝硅酸盐,化学式MgAl2H4Si4O14,化学式改写成氧化物形式为
(2)检验CO2中是否混有SO2可将气体通过盛有
(3)鉴别Na2CO3和NaHCO3溶液可选用
①NaOH ②Ca(OH)2 ③BaCl2 ④K2SO4 ⑤Ca(NO3)2
(4)某溶液中有NH4+,Mg2+,Fe2+,Al3+四种离子,若向其中加入过量的氢氧化钠溶液,加热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
A.NH
 B.Mg2+ C.Fe2+ D.Al3+
B.Mg2+ C.Fe2+ D.Al3+(5)6.4gCu与过量硝酸(60mL 8mol/L)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中所含H+为n mol,NO、NO2混合气体的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】为了达到下表的实验目的,请选择合适的试剂及实验方法,并将其标号填入对应的空格。
A.加热升华
B.向溶液中加入足量CO2气体
C.分别加入品红溶液中,观察现象
D.分别加入紫色石蕊试剂中,观察现象
E.加入硫酸铜固体观察现象
| 序号 | 实验目的 | 试剂及方法 |
| (1) | 鉴别CO2和SO2气体 | |
| (2) | 除去食盐中混有的少量碘 | |
| (3) | 检验无水乙醇中是否含有水 | |
| (4) | 除去NaHCO3溶液中混有的Na2CO3 |
B.向溶液中加入足量CO2气体
C.分别加入品红溶液中,观察现象
D.分别加入紫色石蕊试剂中,观察现象
E.加入硫酸铜固体观察现象
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求写出反应的化学方程式:
(1)木炭加入到热的浓硝酸中有无色和红棕色气体生成_______
(2)加热条件下铜加入到浓硫酸中_______
(3)氯化铵固体和氢氧化钠固体混合加热______
(4)二氧化硫与硫化氢混合有黄色物质生成_______
(1)木炭加入到热的浓硝酸中有无色和红棕色气体生成
(2)加热条件下铜加入到浓硫酸中
(3)氯化铵固体和氢氧化钠固体混合加热
(4)二氧化硫与硫化氢混合有黄色物质生成
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硫、氮、氯其化合物在生产生活中应用广泛。请回答:
(1)将SO2通入品红溶液中,现象为品红溶液___________ ,加热后溶液颜色___________ 。将Cl2和SO2以1:1通入品红中,不能增强漂白性,用化学用语解释原因___________
(2)工业生产漂白粉有关反应的化学方程式:___________
(3)在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式___________ 。
(4)0.3mol的钠镁铝分别投入100mL 1mol/L的硫酸中,相同条件下产生H2的体积比是___________
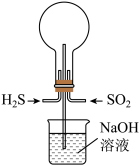
(5)用如图所示装置做实验:常温下将H2S和SO2以物质的量之比为1∶1充满烧瓶,不久烧瓶中能观察到的现象是___________ 。
(1)将SO2通入品红溶液中,现象为品红溶液
(2)工业生产漂白粉有关反应的化学方程式:
(3)在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式
(4)0.3mol的钠镁铝分别投入100mL 1mol/L的硫酸中,相同条件下产生H2的体积比是
(5)用如图所示装置做实验:常温下将H2S和SO2以物质的量之比为1∶1充满烧瓶,不久烧瓶中能观察到的现象是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某实验小组在探究SO2性质的时候,发现若将SO2气体通入足量的Ba(OH)2溶液中,有白色沉淀生成,再滴入稀硝酸,沉淀无明显变化,但有无色气体生成,遇空气无色气体变为红棕色。
回答下列问题:
(1)写出上述实验中通入SO2生成白色沉淀的离子方程式:___________ 。请用离子方程式表示加入稀硝酸后生成无色气体的原因:___________ 。
(2)若将SO2气体通入足量的BaCl2溶液中,则无明显现象产生。
①同时向BaCl2溶液中通入NH3和SO2有白色沉淀产生,产生沉淀的化学式___________ 。
②同时向BaCl2溶液中通入SO2和Cl2有白色沉淀产生,产生沉淀的化学式___________ 。
③同时向BaCl2溶液中通入SO2和NO2是否有白色沉淀生成,请判断并说明原因___________ 。
(3)若将SO2通入H2S溶液中,有淡黄色沉淀生成,请写出反应的化学方程式:___________ ,该反应中体现了SO2的___________ (填"还原性"或"氧化性")。
回答下列问题:
(1)写出上述实验中通入SO2生成白色沉淀的离子方程式:
(2)若将SO2气体通入足量的BaCl2溶液中,则无明显现象产生。
①同时向BaCl2溶液中通入NH3和SO2有白色沉淀产生,产生沉淀的化学式
②同时向BaCl2溶液中通入SO2和Cl2有白色沉淀产生,产生沉淀的化学式
③同时向BaCl2溶液中通入SO2和NO2是否有白色沉淀生成,请判断并说明原因
(3)若将SO2通入H2S溶液中,有淡黄色沉淀生成,请写出反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据信息书写指定反应的方程式。
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂: 溶液、
溶液、 溶液、
溶液、 溶液、浓
溶液、浓 、氯水、KI溶液
、氯水、KI溶液
① 的离子方程式:
的离子方程式:_______ ;
② (两性氧化物)
(两性氧化物)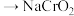 的化学方程式:
的化学方程式:_______ ;
(2)一种以 溶液为原料先制取
溶液为原料先制取 ,再制取
,再制取 (铁红)的流程如下:
(铁红)的流程如下:

反应Ⅰ中向 溶液中同时加入
溶液中同时加入 和
和 ,过滤所得滤液中只含一种溶质,写出该反应的化学方程式:
,过滤所得滤液中只含一种溶质,写出该反应的化学方程式:_______ 。
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂:
 溶液、
溶液、 溶液、
溶液、 溶液、浓
溶液、浓 、氯水、KI溶液
、氯水、KI溶液①
 的离子方程式:
的离子方程式:②
 (两性氧化物)
(两性氧化物)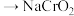 的化学方程式:
的化学方程式:(2)一种以
 溶液为原料先制取
溶液为原料先制取 ,再制取
,再制取 (铁红)的流程如下:
(铁红)的流程如下:
反应Ⅰ中向
 溶液中同时加入
溶液中同时加入 和
和 ,过滤所得滤液中只含一种溶质,写出该反应的化学方程式:
,过滤所得滤液中只含一种溶质,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有下列9种物质:①甲烷;②乙烷;③SO2;④聚乙烯;⑤聚乙炔;⑥己烯;⑦2-丁炔;⑧聚1,3-丁二烯;⑨乙醇 既能使酸性高锰酸钾溶液褪色,又能与溴水反应使溴水褪色的是___________________ (写序号)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】硫、氮、氯其化合物在生产生活中应用广泛。请回答:
(1)将SO2通入品红溶液中,现象为品红溶液________ ,加热后溶液颜色________ 。
(2)已知反应:SO2+Cl2+2H2O ═ 2HCl+H2SO4,该反应中的氧化产物是__________ 。
(3)木炭与浓硫酸共热的化学反应方程式为:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是
CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是_________ mol。
(4)汽车尾气常含有NO、NO2、CO等,会污染空气。在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式___________ 。
(5)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是___________ (用离子方程式表示)。利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式:____________
(1)将SO2通入品红溶液中,现象为品红溶液
(2)已知反应:SO2+Cl2+2H2O ═ 2HCl+H2SO4,该反应中的氧化产物是
(3)木炭与浓硫酸共热的化学反应方程式为:C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是
CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是(4)汽车尾气常含有NO、NO2、CO等,会污染空气。在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式
(5)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是
您最近一年使用:0次




