完成下列表格(操作—现象—结论型判断解释)
| 序号 | 实验操作及现象 | 结论 | 判断 | 解释 |
| (1) | 用铂丝蘸取某溶液进行焰色反应,火焰呈黄色 | 一定是钠盐溶液,该溶液中一定不含 | ||
| (2) | 向乙醇中加入浓硫酸,加热,溶液变黑,将产生的气体通入酸性 溶液中,溶液褪色 溶液中,溶液褪色 | 该气体是乙烯 | ||
| (3) | 向溶液X中滴加稀 溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 溶液X中无 | ||
| (4) | 用湿润的淀粉碘化钾试纸检验气体Y,试纸变蓝 | Y是 | ||
| (5) | 将某气体通入品红溶液中,溶液褪色 | 该气体一定是 | ||
| (6) | 向溶液Y中滴加稀硝酸,再滴加 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | Y中一定含有 | ||
| (7) | 往 中滴入酸性 中滴入酸性 溶液,溶液褪色 溶液,溶液褪色 | 该有机物中含有碳碳双键 | ||
| (8) | 蘸有浓氨水的玻璃棒靠近溶液X有白烟产生 | X一定是浓盐酸 | ||
| (9) | 向某溶液中滴加 溶液,溶液不变色,滴加氯水后溶液显红色 溶液,溶液不变色,滴加氯水后溶液显红色 | 该溶液中一定含 | ||
| (10) | 将 气体通入 气体通入 溶液中,生成白色沉淀 溶液中,生成白色沉淀 | 该沉淀一定是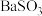 | ||
| (11) | 将 气体通入 气体通入 溶液中,无明显现象 溶液中,无明显现象 |  和 和 不反应 不反应 | ||
| (12) | 将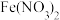 样品溶于稀硫酸,滴加 样品溶于稀硫酸,滴加 溶液,溶液变红 溶液,溶液变红 | 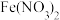 样品已氧化变质 样品已氧化变质 |
2023高三·全国·专题练习 查看更多[1]
(已下线)第一部分 二轮专题突破 专题18 物质检验、鉴别简单实验方案的设计及评价
更新时间:2023-02-03 21:56:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】电解质溶于水时会发生电离产生自由移动的离子,电导率变化一定程度上可以反映溶液中自由移动的离子浓度变化。在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。回答下列问题。
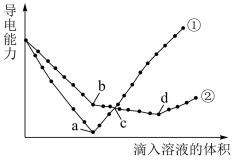
(1)NaHSO4在水溶液中的电离方程式是_______ ;NaHSO4属于“酸”、“碱”、“盐”中的_______ ;图中代表滴加NaHSO4溶液的变化曲线是_______ (填“①”或“②”)。
(2)曲线①中a点导电能力最弱的原因是_______ ;(用离子方程式表示),b点溶液中大量存在的离子是_______ 。
(3)c点两溶液中H+浓度:①_______ ②(填“>”、“<”或“=”,下同);d点对应的溶液显_______ (填“酸性”、“中性”、“碱性”)。
(4)曲线②中的b、d两点对应所加溶液的体积比为_______ 。

(1)NaHSO4在水溶液中的电离方程式是
(2)曲线①中a点导电能力最弱的原因是
(3)c点两溶液中H+浓度:①
(4)曲线②中的b、d两点对应所加溶液的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有一包白色固体粉末,其中可能含有CaCO3、Na2CO3、Na2SO4、NaCl、CuSO4进行如下实验: ①溶于水得无色溶液, ②向溶液中加入BaCl2溶液时生成白色沉淀,再加盐酸时沉淀全部消失.根据以上实验现象推断:一定不存在的物质是________________________________ ; 一定存在的物质是__________ ;可能存在 _____________ 。(写化学式)如想对上述固体粉末中可能存在的物质做进一步检验,所选用的试剂是:____________________________________ 有关的离子方程式______________________________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某无色透明溶液中可能大量存在 、
、 、
、 、
、 、
、 和
和 中的几种,请填写:
中的几种,请填写:
(1)通过观察溶液颜色可知溶液中不存在的离子是_______ 。
(2)取少量原溶液,加入过量氯化钡溶液,有白色沉淀A生成,再加入足量硝酸,沉淀部分溶解,则A为_______ (填化学式)。
(3)取(2)反应后的上层清液,加入硝酸银溶液,出现白色沉淀B,该反应的离子方程式为_______ 。
(4)综上所述,原溶液中一定存在的离子是_______ ,一定不存在的离子是_______ ,可能存在的离子是_______ 。
 、
、 、
、 、
、 、
、 和
和 中的几种,请填写:
中的几种,请填写:(1)通过观察溶液颜色可知溶液中不存在的离子是
(2)取少量原溶液,加入过量氯化钡溶液,有白色沉淀A生成,再加入足量硝酸,沉淀部分溶解,则A为
(3)取(2)反应后的上层清液,加入硝酸银溶液,出现白色沉淀B,该反应的离子方程式为
(4)综上所述,原溶液中一定存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】尽管氮元素在地壳中的丰度较低(主要以硝酸盐的形式存在),在所有元素中仅排31位,但是大气中有丰富的氮气,这为氨和硝酸的广泛应用提供了可能。
(1)氮气的电子式为_______ ,雷电作用能进行氮的固定,写出反应方程式______________ 。
(2)食物蕴含的营养物质中,含氮的高分子化合物是______________ (填名称),其水解的最终产物为______________ 。
(3)土壤中的NH4+在硝化细菌的催化作用下可转化为NO3﹣,写出其离子方程式:______________ 。
(4)某铜铝合金用足量稀硝酸完全溶解,得到标准状况下NO 11.2 L,再向溶液中加入过量氨水,充分反应后过滤。①滤液显深蓝色是因为含有的离子(填化学式).______________ 。②若沉淀质量为7.8g,则合金的质量为______________ g。
(1)氮气的电子式为
(2)食物蕴含的营养物质中,含氮的高分子化合物是
(3)土壤中的NH4+在硝化细菌的催化作用下可转化为NO3﹣,写出其离子方程式:
(4)某铜铝合金用足量稀硝酸完全溶解,得到标准状况下NO 11.2 L,再向溶液中加入过量氨水,充分反应后过滤。①滤液显深蓝色是因为含有的离子(填化学式).
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化工生产中采用硝酸为原料生产亚硝酸钠,工艺流程如下。
其生产原理是:NO+NO2+2NaOH=2NaNO2+H2O。
可能副反应为:2NO2+ 2NaOH=NaNO2+ NaNO3+H2O。

(1)分解塔加料时采用气-液逆流方式,其目的是:___________ 。
(2)按一定计量比在反应塔中通SO2和喷入硝酸,若反应后生成的NO与NO2物质的量之比恰好1:1,则分解塔中发生反应的化学方程式为:___________ 。
(3)该流程中硝酸的浓度不宜过大或过小的原因是___________ 。
(4)结晶过程中溶液需保持弱碱性,在酸性溶液中NaNaO2会发生分解,产物之一是NO,其反应的离子方程式为___________ 。
其生产原理是:NO+NO2+2NaOH=2NaNO2+H2O。
可能副反应为:2NO2+ 2NaOH=NaNO2+ NaNO3+H2O。

(1)分解塔加料时采用气-液逆流方式,其目的是:
(2)按一定计量比在反应塔中通SO2和喷入硝酸,若反应后生成的NO与NO2物质的量之比恰好1:1,则分解塔中发生反应的化学方程式为:
(3)该流程中硝酸的浓度不宜过大或过小的原因是
(4)结晶过程中溶液需保持弱碱性,在酸性溶液中NaNaO2会发生分解,产物之一是NO,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学性质

(1)不稳定性
反应:___________ 。
(2)强氧化性
硝酸无论浓、稀都具有强氧化性,而且浓度越大,氧化性越强。
按要求完成下列反应的方程式:
①与金属反应
稀硝酸与铜反应:___________ ;
浓硝酸与铜反应:___________ 。
②与非金属反应
浓硝酸与C反应:___________ 。
③与还原性化合物反应
硝酸可氧化H2S、SO2、Na2SO3、HI、Fe2+等还原性物质。
稀硝酸与FeSO4溶液反应的离子方程式:3Fe2++4H++NO =3Fe3++NO↑+2H2O。
=3Fe3++NO↑+2H2O。

(1)不稳定性
反应:
(2)强氧化性
硝酸无论浓、稀都具有强氧化性,而且浓度越大,氧化性越强。
按要求完成下列反应的方程式:
①与金属反应
稀硝酸与铜反应:
浓硝酸与铜反应:
②与非金属反应
浓硝酸与C反应:
③与还原性化合物反应
硝酸可氧化H2S、SO2、Na2SO3、HI、Fe2+等还原性物质。
稀硝酸与FeSO4溶液反应的离子方程式:3Fe2++4H++NO
 =3Fe3++NO↑+2H2O。
=3Fe3++NO↑+2H2O。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请根据钠及其化合物性质按要求完成各题。
(1)金属钠的密度比水小,在钠与水反应的实验中,能得出“该反应是放热反应”这一结论的实验现象是_______ ,反应的离子方程式是_______ 。
(2)钠的焰色反应的焰色为_______ 色,金属焰色反应是_______ 变化(填“物理”或“化学”)。
(3)写出过氧化钠和二氧化碳反应的化学方程式,并用双线桥表示电子转移方向和数目_______ 。
(1)金属钠的密度比水小,在钠与水反应的实验中,能得出“该反应是放热反应”这一结论的实验现象是
(2)钠的焰色反应的焰色为
(3)写出过氧化钠和二氧化碳反应的化学方程式,并用双线桥表示电子转移方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某学习小组欲确定某混合溶液中是否含有以下离子Al3+、Fe3+、Cl-、Na+,采取如下方法,请回答问题:
(1)取少量溶液于试管中,滴加KSCN溶液,溶液变为红色,说明溶液中存在______ ,向该溶液中加入铁粉,写出发生反应的离子方程式___________________ 。
(2)另取少量溶液于试管中,逐滴滴加NaOH溶液,实验发现产生的沉淀先增加后略有减少,说明溶液中存在_________ ,写出沉淀减少的化学方程式___________ 。
(3)请用简要的文字,结合离子方程式说明检验Cl-的实验方法____________________ ,离子方程式为______________ 。
(4)在焰色反应实验中,若观察到火焰的颜色为黄色,则证明该溶液中存在__________ 。
(1)取少量溶液于试管中,滴加KSCN溶液,溶液变为红色,说明溶液中存在
(2)另取少量溶液于试管中,逐滴滴加NaOH溶液,实验发现产生的沉淀先增加后略有减少,说明溶液中存在
(3)请用简要的文字,结合离子方程式说明检验Cl-的实验方法
(4)在焰色反应实验中,若观察到火焰的颜色为黄色,则证明该溶液中存在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有一透明溶液,可能含有大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO 、CO
、CO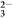 中的一种或几种,取此溶液做下列实验:
中的一种或几种,取此溶液做下列实验:
①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。试推断:
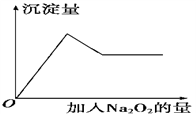
(1)溶液中一定含有的离子是______________ 。
(2)溶液中肯定不含有的离子是________________ 。
(3)可能含有的离子是____________ ,若要确定该离子的存在需要用到的实验方法是____________
 、CO
、CO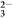 中的一种或几种,取此溶液做下列实验:
中的一种或几种,取此溶液做下列实验:①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。试推断:

(1)溶液中一定含有的离子是
(2)溶液中肯定不含有的离子是
(3)可能含有的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.下面A~F是几种常见的烃的分子球棍模型,根据这些模型回答下列问题:
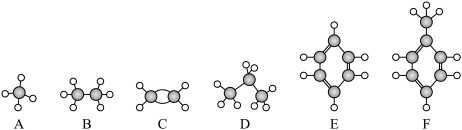
(1)写出以上各分子模型的结构简式: B:_______ 、C:_______ 、D:_______ 、E:_______ 。
(2)能够使酸性高锰酸钾溶液褪色的链烃是_______ (填写结构简式)。
(3)A的二氯代物有_______ 种结构。
(4)写出由C制备高聚物的化学方程式为_______ 。
(5)有人设计下列实验以确认某混合气体中有C2H4和SO2。

装置①、②、③、④可盛放的试剂是①_______ ;②_______ ;③品红;④_______ 。(填字母)
a.品红溶液 b.NaOH溶液 c.浓H2SO4 d. KMnO4(H+)
(6)实验(5)中确认含有C的现象是_______ 。
II.合成聚丙烯腈纤维的方法很多,如以乙炔为原料,其合成过程如下:
CH≡CH+HCN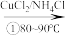 CH2=CHCN
CH2=CHCN 聚丙烯腈
聚丙烯腈
(7)反应①的反应类型为_______ 。
(8)CH2=CHCN在一定条件下可与苯乙烯( )发生共同加成聚合反应,得到一种优良的塑料,该塑料的结构简式为
)发生共同加成聚合反应,得到一种优良的塑料,该塑料的结构简式为_______ 。(写一种即可)
(9)聚苯乙烯的结构为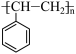 ,则聚苯乙烯的链节是
,则聚苯乙烯的链节是_______ ,单体是_______ 。

(1)写出以上各分子模型的结构简式: B:
(2)能够使酸性高锰酸钾溶液褪色的链烃是
(3)A的二氯代物有
(4)写出由C制备高聚物的化学方程式为
(5)有人设计下列实验以确认某混合气体中有C2H4和SO2。

装置①、②、③、④可盛放的试剂是①
a.品红溶液 b.NaOH溶液 c.浓H2SO4 d. KMnO4(H+)
(6)实验(5)中确认含有C的现象是
II.合成聚丙烯腈纤维的方法很多,如以乙炔为原料,其合成过程如下:
CH≡CH+HCN
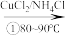 CH2=CHCN
CH2=CHCN 聚丙烯腈
聚丙烯腈(7)反应①的反应类型为
(8)CH2=CHCN在一定条件下可与苯乙烯(
 )发生共同加成聚合反应,得到一种优良的塑料,该塑料的结构简式为
)发生共同加成聚合反应,得到一种优良的塑料,该塑料的结构简式为(9)聚苯乙烯的结构为
 ,则聚苯乙烯的链节是
,则聚苯乙烯的链节是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求回答下列问题:
(1)已知拆开 键、
键、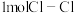 键、
键、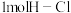 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、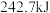 、
、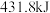 。则由
。则由 和
和 反应生成1molHCl需要
反应生成1molHCl需要________  填“放出”或“吸收”
填“放出”或“吸收”
_______  的热量。
的热量。
(2)已知:某物质的产量可以用来衡量一个国家的石油化工发展水平。请回答:
①该物质的结构式为________ 。
②若将该物质通入溴的四氯化碳溶液中,反应的化学方程式为________ 。
③在一定条件下,该物质能与水反应生成有机物A.A的结构简式是________ 。
④下列化学反应原理相同的是________ (填序号)。
A.乙烯使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色
B.SO2使溴水和酸性高锰酸钾溶液褪色
C.SO2使品红溶液和滴有酚酞的NaOH溶液褪色
(1)已知拆开
 键、
键、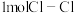 键、
键、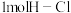 键分别需要吸收的能量为
键分别需要吸收的能量为 、
、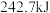 、
、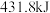 。则由
。则由 和
和 反应生成1molHCl需要
反应生成1molHCl需要 填“放出”或“吸收”
填“放出”或“吸收”
 的热量。
的热量。(2)已知:某物质的产量可以用来衡量一个国家的石油化工发展水平。请回答:
①该物质的结构式为
②若将该物质通入溴的四氯化碳溶液中,反应的化学方程式为
③在一定条件下,该物质能与水反应生成有机物A.A的结构简式是
④下列化学反应原理相同的是
A.乙烯使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色
B.SO2使溴水和酸性高锰酸钾溶液褪色
C.SO2使品红溶液和滴有酚酞的NaOH溶液褪色
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】完成下列表格
(1)常见物质的除杂(括号中的物质为杂质)
(2)常见混合气体的除杂
混合气体(括号内为杂质)除杂试剂分离方法
(1)常见物质的除杂(括号中的物质为杂质)
| 除杂试剂 | 分离方法(或操作) | |
 溶液( 溶液( 溶液) 溶液) | 加酸转化法 | |
 | 过量 | |
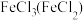 | 加氧化剂转化法 | |
 | 过量 | |
 | 适量 | |
 | 水 | 蒸发浓缩、 |
 | 水 | 蒸发结晶、 |
炭粉( ) ) | ||
 粉( 粉( 粉) 粉) | 过量 | |
| 乙醇(水) |  | |
| 乙酸乙酯(乙酸) | 饱和 | 分液 |
(2)常见混合气体的除杂
混合气体(括号内为杂质)除杂试剂分离方法
| 混合气体(括号内为杂质) | 除杂试剂 | 分离方法 |
 | 洗气 | |
 | 洗气 | |
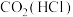 | 洗气 | |
 | 洗气 | |
 | ||
 | 洗气 | |
 | 洗气 | |
 | ||
 | 洗气 | |
您最近一年使用:0次



