铁合金有下列数据:
取15g某碳素钢样品,按下列实验流程进行操作;
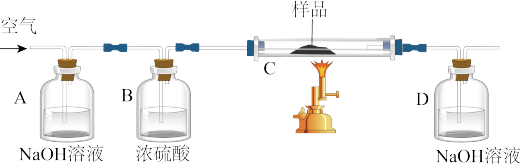
请回答:
(1)A、B的作用分别为_______ ,_______ 。
(2)D中的发生反应的离子方程式为_______ 。
(3)充分加热完全反应后,D装置质量增加0.022g,该样品含碳量为_______ ,属于_______ 碳铜。(填“低”、“中”、“高”)
(4)没有A装置,实验结果_______ (填“偏高”、“偏低”成“不影响”)
| 碳素钢(Fe、C、Mn、Si) | ||
| 低碳钢 | 中碳钢 | 高碳钢 |
| 含碳量<0.3% | 含碳量0.3%-0.6% | 含碳量>0.6% |

请回答:
(1)A、B的作用分别为
(2)D中的发生反应的离子方程式为
(3)充分加热完全反应后,D装置质量增加0.022g,该样品含碳量为
(4)没有A装置,实验结果
更新时间:2023-02-10 09:46:12
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】 是一种安全稳定、高效低毒的广谱型消毒剂,它易溶于水、难溶于有机溶剂,高浓度的
是一种安全稳定、高效低毒的广谱型消毒剂,它易溶于水、难溶于有机溶剂,高浓度的 气体易爆炸。常见制备
气体易爆炸。常见制备 的方法如下:
的方法如下:
Ⅰ.利用 与纯净的
与纯净的 反应可制得
反应可制得 和NaCl,实验装置如图所示(夹持装置略)。
和NaCl,实验装置如图所示(夹持装置略)。_______ 。
(2)装置E中所盛试剂是 ,其作用为
,其作用为_______ 。
Ⅱ.草酸( )、氯酸钾和适当浓度的
)、氯酸钾和适当浓度的 溶液反应制取
溶液反应制取 ,反应中有
,反应中有 气体生成。
气体生成。
(3)该方法制备 的优点是
的优点是_______ 。
Ⅲ.以黄铁矿( )、氯酸钠和硫酸溶液混合反应制备
)、氯酸钠和硫酸溶液混合反应制备 ,再用水吸收获得
,再用水吸收获得 溶液。在
溶液。在 的制备和吸收过程中均需要控制适宜的温度,如图所示为温度对
的制备和吸收过程中均需要控制适宜的温度,如图所示为温度对 纯度、吸收率的影响。
纯度、吸收率的影响。 氧化成
氧化成 ,写出该法制备
,写出该法制备 气体的离子方程式:
气体的离子方程式:_______ ,由图可知,反应时采取的适宜措施是_______ 。
(5)某校化学学习小组拟以“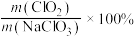 ”作为衡量
”作为衡量 产率的指标。取
产率的指标。取 样品质量6.000g,通过反应和吸收可得
样品质量6.000g,通过反应和吸收可得 溶液,取出20.00mL,加入
溶液,取出20.00mL,加入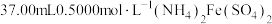 溶液充分反应,过量
溶液充分反应,过量 再用
再用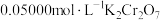 标准溶液滴定至终点,消耗20.00mL。反应原理如下(未配平):
标准溶液滴定至终点,消耗20.00mL。反应原理如下(未配平):
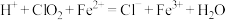 ;
;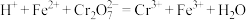 ,试计算
,试计算 的产率
的产率_______ (写出计算过程)。
 是一种安全稳定、高效低毒的广谱型消毒剂,它易溶于水、难溶于有机溶剂,高浓度的
是一种安全稳定、高效低毒的广谱型消毒剂,它易溶于水、难溶于有机溶剂,高浓度的 气体易爆炸。常见制备
气体易爆炸。常见制备 的方法如下:
的方法如下:Ⅰ.利用
 与纯净的
与纯净的 反应可制得
反应可制得 和NaCl,实验装置如图所示(夹持装置略)。
和NaCl,实验装置如图所示(夹持装置略)。
(2)装置E中所盛试剂是
 ,其作用为
,其作用为Ⅱ.草酸(
 )、氯酸钾和适当浓度的
)、氯酸钾和适当浓度的 溶液反应制取
溶液反应制取 ,反应中有
,反应中有 气体生成。
气体生成。(3)该方法制备
 的优点是
的优点是Ⅲ.以黄铁矿(
 )、氯酸钠和硫酸溶液混合反应制备
)、氯酸钠和硫酸溶液混合反应制备 ,再用水吸收获得
,再用水吸收获得 溶液。在
溶液。在 的制备和吸收过程中均需要控制适宜的温度,如图所示为温度对
的制备和吸收过程中均需要控制适宜的温度,如图所示为温度对 纯度、吸收率的影响。
纯度、吸收率的影响。
 氧化成
氧化成 ,写出该法制备
,写出该法制备 气体的离子方程式:
气体的离子方程式:(5)某校化学学习小组拟以“
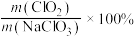 ”作为衡量
”作为衡量 产率的指标。取
产率的指标。取 样品质量6.000g,通过反应和吸收可得
样品质量6.000g,通过反应和吸收可得 溶液,取出20.00mL,加入
溶液,取出20.00mL,加入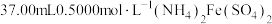 溶液充分反应,过量
溶液充分反应,过量 再用
再用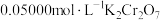 标准溶液滴定至终点,消耗20.00mL。反应原理如下(未配平):
标准溶液滴定至终点,消耗20.00mL。反应原理如下(未配平):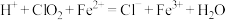 ;
;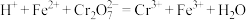 ,试计算
,试计算 的产率
的产率
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】草酸锰能作漂白催化剂,特别用于增强过氧化物在漂白有色污渍时的漂白效果。工业上,常用废锰料(主要成分为Mn,含有一定量的Al2O3、FeO、CaO、SiO2)为原料制备纯净草酸锰晶体,其工业流程如图所示。

已知:①草酸锰晶体(MnC2O4∙2H2O)难溶于水。
②相关金属离子生成氢氧化物沉淀的pH见表中数据。
(1)能提高“酸浸”速率的方法有______ (写出一点即可)。
(2)“氧化”步骤中,试剂a常选双氧水,反应的离子方程式为______ 。
(3)“加入氨水调节pH”时,应控制pH的范围是______ ,滤渣2的主要成分是______ (写化学式)。
(4)“沉钙”后得到的滤渣3的电子式为______ 。
(5)“沉锰”时,反应的离子方程式为______ 。
(6)“操作a”是指______ 。
(7)氨水是常用于废水处理的pH调节剂,如对于含锰废水中的Fe3+,用氨水调节pH值,以除去Fe3+,若使c(Fe3+)小于2.6×10−9 mol∙L−1,而保留c(Mn2+)=0.0548 mol∙L−1,则需控制pH的大致范围为______ 。[已知常温下,Fe(OH)3的Ksp=2.6×10−39,Mg(OH)2的Ksp=5.48×10−16]

已知:①草酸锰晶体(MnC2O4∙2H2O)难溶于水。
②相关金属离子生成氢氧化物沉淀的pH见表中数据。
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
| 开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀pH | 3.2 | 9.0 | 4.7 | 10.1 |
(1)能提高“酸浸”速率的方法有
(2)“氧化”步骤中,试剂a常选双氧水,反应的离子方程式为
(3)“加入氨水调节pH”时,应控制pH的范围是
(4)“沉钙”后得到的滤渣3的电子式为
(5)“沉锰”时,反应的离子方程式为
(6)“操作a”是指
(7)氨水是常用于废水处理的pH调节剂,如对于含锰废水中的Fe3+,用氨水调节pH值,以除去Fe3+,若使c(Fe3+)小于2.6×10−9 mol∙L−1,而保留c(Mn2+)=0.0548 mol∙L−1,则需控制pH的大致范围为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某化学兴趣小组用下列装置制取纯净干燥的氯气,并进行氯气性质的探究(提示:氯气几乎不溶于饱和食盐水).

回答下列问题:
(1)装置B中试剂是____________________ ,作用为____________________ .
(2)装置C中浓硫酸的作用是_____________________________ .
(3)一段时间后装置B内不再产生气泡,请你分析产生这种现象的原因是___________________ .
(4)D中导管长进短出的原因是_____________________________ .
(5)装置E中现象为__________ ,说明氯气_________ (填“有”或“无”)漂白性.
(6)装置F中现象为___________ ,用离子方程式解释原因__________________ .

回答下列问题:
(1)装置B中试剂是
(2)装置C中浓硫酸的作用是
(3)一段时间后装置B内不再产生气泡,请你分析产生这种现象的原因是
(4)D中导管长进短出的原因是
(5)装置E中现象为
(6)装置F中现象为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】固体矿物X由三种元素组成。某学习小组为了探究它的组成和性质,进行了如下实验:

请回答:
(1)溶液F的溶质为__________ (写化学式)。溶液D中的阳离子有__________ 。
(2)X的化学式是__________ 。
(3)写出气体A与溶液D反应的离子方程式__________ 。
(4)设计检验气体A的实验方案:__________ 。

请回答:
(1)溶液F的溶质为
(2)X的化学式是
(3)写出气体A与溶液D反应的离子方程式
(4)设计检验气体A的实验方案:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】“侯氏制碱法”促进了我国纯碱工业的发展。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备碳酸钠的实验流程如图。

回答下列问题:
(1)下列关于碳酸氢铵的说法中错误的是___________(填序号)。
(2)“加热搅拌”中发生反应的化学方程式是___________ ,该反应属于___________ (填基本反应类型)。
(3)“300℃加热”需用到的仪器除酒精灯、坩埚、坩埚钳、三角架外,还有___________ 。
(4)除去 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是___________ 。
(5)检验 中阳离子的实验方法是
中阳离子的实验方法是___________ 。
(6)现将 和
和 的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少
的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少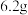 ;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体
;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体 。则混合物中
。则混合物中 和
和 的物质的量之比为
的物质的量之比为___________ 。

回答下列问题:
(1)下列关于碳酸氢铵的说法中错误的是___________(填序号)。
| A.属于铵盐 | B.属于碳酸氢盐 | C.属于酸式盐 | D.属于复合肥料 |
(3)“300℃加热”需用到的仪器除酒精灯、坩埚、坩埚钳、三角架外,还有
(4)除去
 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是(5)检验
 中阳离子的实验方法是
中阳离子的实验方法是(6)现将
 和
和 的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少
的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少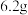 ;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体
;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体 。则混合物中
。则混合物中 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】Ⅰ.焦亚硫酸钠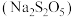 是常用的食品抗氧化剂之一,带有强烈的
是常用的食品抗氧化剂之一,带有强烈的 气味,久置于空气中易被氧化,其溶于水生成的
气味,久置于空气中易被氧化,其溶于水生成的 溶液呈酸性。某研究小组采用如图所示装置(实验前已除尽装置内的空气)制取
溶液呈酸性。某研究小组采用如图所示装置(实验前已除尽装置内的空气)制取 。
。

(1)装置Ⅰ中的盛装浓硫酸的仪器名称__________ 。
(2)请写出 溶液中的离子浓度由大到小的顺序
溶液中的离子浓度由大到小的顺序____________________________ 。
Ⅱ. 溶液可用于测定溶液中
溶液可用于测定溶液中 的含量,实验方案如下。
的含量,实验方案如下。
步骤1:准确量取 溶液
溶液 ,稀释至
,稀释至 。
。
步骤2:量取 稀释后的
稀释后的 溶液于锥形瓶中,调节溶液的
溶液于锥形瓶中,调节溶液的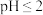 ,加入足量的
,加入足量的 晶体,摇匀,在暗处静置30分钟。(已知:
晶体,摇匀,在暗处静置30分钟。(已知: )
)
步骤3:以淀粉溶液作指示剂,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。(已知:
。(已知: )
)
(3)准确量取 溶液的玻璃仪器是
溶液的玻璃仪器是______________ 。
(4)确定滴定终点的现象为_________________ 。
(5)根据上述步骤计算出原 溶液的物质的量浓度为
溶液的物质的量浓度为________  (用含字母的代数式表示)。
(用含字母的代数式表示)。
(6)下列操作会导致测定结果偏低的是_________(填字母)。
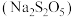 是常用的食品抗氧化剂之一,带有强烈的
是常用的食品抗氧化剂之一,带有强烈的 气味,久置于空气中易被氧化,其溶于水生成的
气味,久置于空气中易被氧化,其溶于水生成的 溶液呈酸性。某研究小组采用如图所示装置(实验前已除尽装置内的空气)制取
溶液呈酸性。某研究小组采用如图所示装置(实验前已除尽装置内的空气)制取 。
。
(1)装置Ⅰ中的盛装浓硫酸的仪器名称
(2)请写出
 溶液中的离子浓度由大到小的顺序
溶液中的离子浓度由大到小的顺序Ⅱ.
 溶液可用于测定溶液中
溶液可用于测定溶液中 的含量,实验方案如下。
的含量,实验方案如下。步骤1:准确量取
 溶液
溶液 ,稀释至
,稀释至 。
。步骤2:量取
 稀释后的
稀释后的 溶液于锥形瓶中,调节溶液的
溶液于锥形瓶中,调节溶液的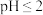 ,加入足量的
,加入足量的 晶体,摇匀,在暗处静置30分钟。(已知:
晶体,摇匀,在暗处静置30分钟。(已知: )
)步骤3:以淀粉溶液作指示剂,用
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。(已知:
。(已知: )
)(3)准确量取
 溶液的玻璃仪器是
溶液的玻璃仪器是(4)确定滴定终点的现象为
(5)根据上述步骤计算出原
 溶液的物质的量浓度为
溶液的物质的量浓度为 (用含字母的代数式表示)。
(用含字母的代数式表示)。(6)下列操作会导致测定结果偏低的是_________(填字母)。
A.未用标准浓度的 溶液润洗滴定管 溶液润洗滴定管 |
| B.滴定前锥形瓶中有少量水 |
| C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失 |
| D.读数时,滴定前仰视,滴定后俯视 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】辽宁号航空母舰,是中国人民解放军第一艘可以搭载固定翼飞机的航空母舰,它的主体材料是各种合金。
(1)航母升降机可由铝合金制造。
①铝原子结构示意图为_______ 。工业炼铝的原料由铝土矿提取而得,铝土矿的主要成分中含有氧化铝、氧化铁和二氧化硅,工业上经过下列工艺可以冶炼金属铝(过滤、洗涤、干燥过程已略去):

则在步骤III中加入的最佳的物质是(填化学式)_______ ;步骤IV的化学反应方程式是:_______ 。
②Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为_______ 。
(2)航母舰体材料为合金钢。
①工业上冶炼铁原料主要选择赤铁矿,其主要成分是_______ (填化学式)。
②不锈钢是最常见的一种合金钢,它的合金元素主要是_______ 。
(3)航母螺旋桨主要用铜合金制造。
①青铜是我国古代使用最早的一种合金,中国古代用火烧孔雀石[主要成分为碱式碳酸铜- ]和焦炭的混合物冶炼铜,请写出冶炼铜过程中发生的两个主要反应方程式:
]和焦炭的混合物冶炼铜,请写出冶炼铜过程中发生的两个主要反应方程式:_______ ,_______ 。
②80.0gCu-Al合金用稀盐酸充分反应后,向滤液中加入过量氨水,过滤得沉淀39.0g,则合金中Cu的质量分数为_______ %(小数点后保留一位有效数字)。
(1)航母升降机可由铝合金制造。
①铝原子结构示意图为

则在步骤III中加入的最佳的物质是(填化学式)
②Al-Mg合金焊接前用NaOH溶液处理Al2O3膜,其化学方程式为
(2)航母舰体材料为合金钢。
①工业上冶炼铁原料主要选择赤铁矿,其主要成分是
②不锈钢是最常见的一种合金钢,它的合金元素主要是
(3)航母螺旋桨主要用铜合金制造。
①青铜是我国古代使用最早的一种合金,中国古代用火烧孔雀石[主要成分为碱式碳酸铜-
 ]和焦炭的混合物冶炼铜,请写出冶炼铜过程中发生的两个主要反应方程式:
]和焦炭的混合物冶炼铜,请写出冶炼铜过程中发生的两个主要反应方程式:②80.0gCu-Al合金用稀盐酸充分反应后,向滤液中加入过量氨水,过滤得沉淀39.0g,则合金中Cu的质量分数为
您最近一年使用:0次



