在用惰性电极电解时,由于阴阳两极附近的电势不等,电解质溶液中的___ (填“阴”或“阳”)离子向阳极移动,并最终在阳极上放电发生___ (填“氧化”或“还原”,下同),反应得到___ 产物。在一定温度下,用惰性电极电解饱和CuSO4溶液,一段时间后CuSO4溶液的pH___ (填“变大”、“变小”或“不变”);阴极反应式是___ ,阳极反应式是___ 。
更新时间:2019-11-15 18:51:20
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】某高二化学学习小组设计了如图所示的实验方案来制取次氯酸钠和探究氯水的性质。

图中:①为实验室制氯气发生装置;②试管里盛有15 mL 8% 的NaOH溶液,并置于冰水浴中;③试管里是滴有酚酞的NaOH溶液④为尾气吸收装置。请填写下列空白:
(1)实验前首先必须对整套装置进行的操作是__________ ;
①装置中所进行反应氧化剂与还原剂的物质的量之比为___________ 。
(2)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过____ (填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_____ (填写下列编号字母)的净化装置。
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(3)写出②装置中发生的离子反应方程式________________________________ ;
(4)实验中可观察到③试管的实验现象是溶液褪色。某同学提出两种猜想:
猜想一:氯气与NaOH溶液发生反应使溶液褪色 猜想二:__________________ 。
(5)实验所用NaOH工业上的制备,以电解精制饱和食盐水的方法制取氯气、氢气、烧碱。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
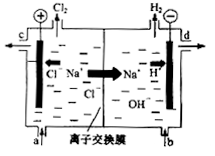
写出电解饱和食盐水的离子方程式________________________________ 。
精制饱和食盐水从图中________ 位置补充(选填“a”、“b”、“c”或“d”)。
(6)含NaCN的污水危害很大,0.01mol/L的NaCN溶液pH=9,请判断该溶液中:c(CN-)_____ c(OH-)(填“>”、“<”或“=”),处理含NaCN污水时,可用制取的次氯酸钠溶液将CN-在酸性条件下氧化生成N2与CO2,该反应的离子方程式为________ 。

图中:①为实验室制氯气发生装置;②试管里盛有15 mL 8% 的NaOH溶液,并置于冰水浴中;③试管里是滴有酚酞的NaOH溶液④为尾气吸收装置。请填写下列空白:
(1)实验前首先必须对整套装置进行的操作是
①装置中所进行反应氧化剂与还原剂的物质的量之比为
(2)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(3)写出②装置中发生的离子反应方程式
(4)实验中可观察到③试管的实验现象是溶液褪色。某同学提出两种猜想:
猜想一:氯气与NaOH溶液发生反应使溶液褪色 猜想二:
(5)实验所用NaOH工业上的制备,以电解精制饱和食盐水的方法制取氯气、氢气、烧碱。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。

写出电解饱和食盐水的离子方程式
精制饱和食盐水从图中
(6)含NaCN的污水危害很大,0.01mol/L的NaCN溶液pH=9,请判断该溶液中:c(CN-)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】阳离子交换膜电解槽运用到氯碱工业,使产品的纯度大大提高,主要归功于阳离子交换膜的严格把关,它只允许阳离子自由通过,其工作原理如图所示。
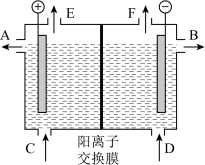
(1)在氯碱工业中电解饱和食盐水制备氢气、氯气和氢氧化钠溶液时,饱和食盐水的入口应该是______ (填“C”或“D”)。
(2)该装置也可用于物质的提纯,工业品氢氧化钾的溶液中含有某些含氧酸根杂质(如SO42-),可以用阳离子交换膜电解槽电解提纯。除去杂质后氢氧化钾溶液从液体出口_________ (填“A”或“B”)导出。
(3)阳离子交换膜的诞生极大促进了电解工业的发展,我们不妨大胆设想,假设阴离子交换膜也已经诞生,同时使用阳离子交换膜和阴离子交换膜电解硫酸钠溶液,可以同时制备产品氢气、氧气、氢氧化钠溶液和硫酸溶液四种物质。某同学设计了如图所示的装置,请你指出硫酸钠溶液的入口是_______ (填“C”“G”或“D”)。


(1)在氯碱工业中电解饱和食盐水制备氢气、氯气和氢氧化钠溶液时,饱和食盐水的入口应该是
(2)该装置也可用于物质的提纯,工业品氢氧化钾的溶液中含有某些含氧酸根杂质(如SO42-),可以用阳离子交换膜电解槽电解提纯。除去杂质后氢氧化钾溶液从液体出口
(3)阳离子交换膜的诞生极大促进了电解工业的发展,我们不妨大胆设想,假设阴离子交换膜也已经诞生,同时使用阳离子交换膜和阴离子交换膜电解硫酸钠溶液,可以同时制备产品氢气、氧气、氢氧化钠溶液和硫酸溶液四种物质。某同学设计了如图所示的装置,请你指出硫酸钠溶液的入口是

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】用石墨作电极电解下列溶液①稀H2SO4②K2SO4溶液 ③NaCl溶液 ④CuSO4溶液 ⑤KOH溶液
(1)阴极、阳极都有气体产生,且体积比(相同条件下)为2:1的是(填序号)__ ,
(2)阴极、阳极都有气体产生,且体积比(相同条件下)为1:1的是(填序号)__ 其阳极的电极反应式是__ ,电解的总方程式是__ .
(3)阴极、阳极都有气体产生,其中溶液pH变小的是__ ,pH变大的是__ .(填序号)
(4)一个电极析出金属,一个电极逸出气体,且溶液pH明显减小的是__ (填序号),其总反应的化学方程式是__ .
(1)阴极、阳极都有气体产生,且体积比(相同条件下)为2:1的是(填序号)
(2)阴极、阳极都有气体产生,且体积比(相同条件下)为1:1的是(填序号)
(3)阴极、阳极都有气体产生,其中溶液pH变小的是
(4)一个电极析出金属,一个电极逸出气体,且溶液pH明显减小的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】如下图所示的装置,C、D、E、F都是惰性电极。将电源接通后,向乙中滴入酚酞液,在F极附近显红色。试回答以下问题:
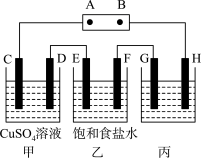
(1)电源的A极是_______ ;
(2)写出甲装置中电解反应的总方程式:__________________ ;
(3)如果收集乙装置中产生的气体,EF两电极产生的气体的体积比是______________ ;
(4)欲用丙装置给铜镀银,G应该是______ ,电镀液的主要成分是______ (填化学式)。

(1)电源的A极是
(2)写出甲装置中电解反应的总方程式:
(3)如果收集乙装置中产生的气体,EF两电极产生的气体的体积比是
(4)欲用丙装置给铜镀银,G应该是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】如图所示为在直流电源的作用下电解CuSO4溶液的装置,其中A、B为石墨电极,a、b为电源的两极,当接通电源,通电一段时间后,将B电极取出,洗干净并干燥后称量,其质量增加了3.2g,则:
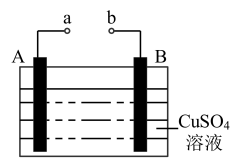
(1)a电极为电源的___ 极。
(2)写出电极反应式:A极___ ,B极__ 。
(3)若要使反应后的溶液恢复到原来状态,则应该加入__ ,加入__ g。

(1)a电极为电源的
(2)写出电极反应式:A极
(3)若要使反应后的溶液恢复到原来状态,则应该加入
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】金属铝在现代生产和日常生活中应用广泛。工业上用电解熔融氧化铝的方法来制取金属铝,纯净氧化铝的熔点很高(约2045℃),在实际生产中,通过加入助熔剂冰晶石(Na3AlF6)在1000℃左右就可以得到熔融体。反应方程式为2Al2O3 4Al+3O2↑。
4Al+3O2↑。
(1)在电解时阴极的电极反应式_________________ ,阳极的电极反应式_____________________ 。
(2)对金属制品进行抗腐蚀处理,可延长其使用寿命,以铝材为阳极,在H2SO4溶液中电解,可使铝材表面形成氧化膜,阳极电极反应式为________________________ 。在电解过程中,阴极附近溶液的pH________ (填“增大,减小或不变”)
(3) “863”计划和中科院“百人计划”支持的环境友好型铝碘电池已研制成功,电解质为AlI3溶液,已知电池总反应为2Al+3I2=2AlI3,该电池负极的电极反应为:_____________________________ ,当负极质量减少27g时,在导线有________ 个电子通过。
 4Al+3O2↑。
4Al+3O2↑。(1)在电解时阴极的电极反应式
(2)对金属制品进行抗腐蚀处理,可延长其使用寿命,以铝材为阳极,在H2SO4溶液中电解,可使铝材表面形成氧化膜,阳极电极反应式为
(3) “863”计划和中科院“百人计划”支持的环境友好型铝碘电池已研制成功,电解质为AlI3溶液,已知电池总反应为2Al+3I2=2AlI3,该电池负极的电极反应为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】电解饱和食盐水的工作原理
(1)电解过程中,阳极室_______ 离子浓度减小,_______ 离子通过阳离子交换膜进入阴极室,NaCl溶液浓度变小;阴极室_______ 离子浓度增大,形成NaOH浓溶液。
(2)阳极产物为_______ ,阴极产物为:_______ 。
(3)阳离子交换膜的作用
①防止阴极区的OH-进入阳极区,OH-与Cl2的反应方程式为_______ 。
②防止H2与Cl2混合发生_______ 。
(1)电解过程中,阳极室
(2)阳极产物为
(3)阳离子交换膜的作用
①防止阴极区的OH-进入阳极区,OH-与Cl2的反应方程式为
②防止H2与Cl2混合发生
您最近一年使用:0次
【推荐2】如图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题。

(1)打开K2,合并K1,B为_______ 极,A的电极反应式为:_______ ,
(2)打开K1,合并K2,E为_______ 极,F极的电极反应式为:_______ ;检验F极产生气体的方法是_______ 。

(1)打开K2,合并K1,B为
(2)打开K1,合并K2,E为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为_____________ 溶液(填化学式),阳极电极反应式为_______________ ,电解过程中Li+向________ 电极迁移(填“A”或“B”)。


您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】请设计一个能使反应:Cu+2H+═Cu2++H2↑发生的电化学装置,并画出装置图.
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】电解原理在化学工业中有广泛的应用。如图所示为一电解池装置,U形管内装有电解液c,A、B是两块电极板,通过导线与直流电源相连。

(1)若A、B都是惰性电极,电解质溶液c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试剂,试判断:
①a电极是______ 极(填“正”或“负”),B电极是______ 极(填“阴”或“阳”);
②A电极上的电极反应式为_______ ,B电极上的电极反应式为________ ;
③检验A电极上产物的方法是______ 。
(2)若图示装置为用惰性电极电解CuSO4溶液的装置,其中阴极上析出Cu的质量为3.2 g,则阳极上产生的气体在标准状况下的体积为_______ 。

(1)若A、B都是惰性电极,电解质溶液c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试剂,试判断:
①a电极是
②A电极上的电极反应式为
③检验A电极上产物的方法是
(2)若图示装置为用惰性电极电解CuSO4溶液的装置,其中阴极上析出Cu的质量为3.2 g,则阳极上产生的气体在标准状况下的体积为
您最近一年使用:0次



