下列依据热化学方程式得出的结论正确的是
A.已知 ,则氢气的燃烧热为 ,则氢气的燃烧热为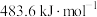 |
B.在一定温度和压强下,将 和 和 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 ,放出热量19.3kJ,则其热化学方程式为 ,放出热量19.3kJ,则其热化学方程式为 |
| C.已知酸和碱发生中和反应生成1mol水,这时的反应热叫中和热 |
D.已知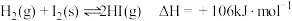 ,虽然该反应为可逆反应,但该反应的焓变仍可通过一定的实验方法直接测得 ,虽然该反应为可逆反应,但该反应的焓变仍可通过一定的实验方法直接测得 |
更新时间:2023/02/24 20:19:39
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) ΔH=-226kJ/mol
O2(g) ΔH=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是
Na2O2(s)+CO2(g)=Na2CO3(s)+
 O2(g) ΔH=-226kJ/mol
O2(g) ΔH=-226kJ/mol根据以上热化学方程式判断,下列说法正确的是
| A.CO的燃烧热为283kJ |
B.如图可表示由CO生成CO2的反应过程和能量关系 |
| C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH=-452kJ/mol |
| D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】反应N2(g)+3H2(g)⇌2NH3(g)的能量变化如图所示,a、b均为正值,单位是kJ,下列说法正确的是
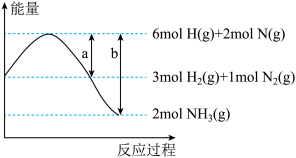

| A.N2(g)+3H2(g)⇌2NH3(g) △H=(a-b)kJ·mol-1 |
B.NH3(g)⇌ N2(g)+ N2(g)+ H2(g) △H=(b-a)kJ·mol-1 H2(g) △H=(b-a)kJ·mol-1 |
| C.NH3中氮氢键键能为bkJ·mol-1 |
| D.压强越大,该反应的△H越小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】有关热化学方程式书写与对应表述均正确的是
| A.稀硫酸与0.1 mol/L NaOH溶液反应:H+(aq)+OH-(aq)= H2O(l) △H = +57.3 kJ·mol1 |
| B.已知2C(s)+O2(g)=2CO(g) △H=—221 kJ·mol-1, 则可知C的燃烧热为110.5 kJ·mol1 |
| C.密闭容器中,0.3mol硫粉与0.2mol铁粉混合加热生成硫化亚铁0.2mol时,放出19.12 kJ热量。则Fe(s)+S(s)=FeS(s) △H= - 95.6 kJ·mol1 |
D.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)  2NH3(g) △H= —38.6kJ·mol1 2NH3(g) △H= —38.6kJ·mol1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列反应方程式表达正确的是
A.用饱和Na2CO3溶液除去乙酸乙酯中的少量乙酸:2CH3COOH+CO =2CH3COO-+CO2↑+H2O =2CH3COO-+CO2↑+H2O |
B.明矾溶液与过量氨水混合:Al3++4NH3+2H2O=AlO +4NH +4NH |
| C.稀硫酸与稀氢氧化钾溶液发生反应:H2SO4(l)+2KOH(1)=K2SO4(l)+2H2O(l) △H=-57.3kJ•mol-1 |
D.将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1:2混合:Ba2++2OH-+2H++SO =BaSO4↓+2H2O =BaSO4↓+2H2O |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】宏观辨识和微观探析是化学学科的核心素养之一,下列相关描述中正确的是
A. (白磷,s) (白磷,s) (红磷,s) (红磷,s)  kJ⋅mol kJ⋅mol ,则白磷比红磷稳定 ,则白磷比红磷稳定 |
B.表示 燃烧热的热化学方程式 燃烧热的热化学方程式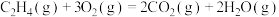 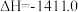 kJ⋅mol kJ⋅mol |
C.已知稀溶液中  kJ⋅mol kJ⋅mol ,则稀硫酸与稀氢氧化钡溶液反应生成1 mol水时放出57.3 kJ的热量 ,则稀硫酸与稀氢氧化钡溶液反应生成1 mol水时放出57.3 kJ的热量 |
D.已知500℃、30 MPa下, 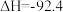 kJ⋅mol kJ⋅mol ,则相同条件下1 mol ,则相同条件下1 mol  和3 moI 和3 moI  充分反应,放出热量小于92.4 kJ 充分反应,放出热量小于92.4 kJ |
您最近半年使用:0次
【推荐1】已知:25℃,101kPa时,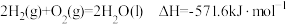 ,请结合水的聚集状态变化时的焓变示意图分析,下列说法
,请结合水的聚集状态变化时的焓变示意图分析,下列说法不正确 的是

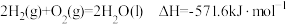 ,请结合水的聚集状态变化时的焓变示意图分析,下列说法
,请结合水的聚集状态变化时的焓变示意图分析,下列说法
| A.A过程为熔化,B过程焓增大 |
B. 的燃烧热: 的燃烧热: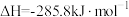 |
C. 冰经过A和B两个过程后化学键数目和氢键数目均不变 冰经过A和B两个过程后化学键数目和氢键数目均不变 |
D. 的单位中“ 的单位中“ ”指每摩尔反应 ”指每摩尔反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述正确的是
| A.甲烷的燃烧热为ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)= CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| B.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则稀H2SO4溶液和稀Ba(OH)2 溶液反应的反应热ΔH ==2×(-57.3) kJ·mol-1 |
| C.Mg在CO2中燃烧生成MgO和C,该反应中化学能全部转化为热能 |
| D.常温下,反应C(s)+CO2(g)===2CO(g)不能自发进行,则该反应的ΔH > 0 |
您最近半年使用:0次

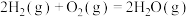
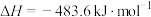 ,则氢气的燃烧热为
,则氢气的燃烧热为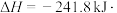
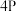 (s,红磷)
(s,红磷)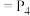 (s,白磷)
(s,白磷) ,则白磷比红磷稳定
,则白磷比红磷稳定
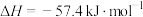

 ,
,
 ,则
,则
 燃烧的热化学方程式为:
燃烧的热化学方程式为: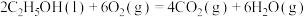


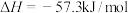 ,则稀醋酸与稀氢氧化钠溶液反应生成1mol水放出57.3kJ热量
,则稀醋酸与稀氢氧化钠溶液反应生成1mol水放出57.3kJ热量
 ,则
,则 生成
生成 的反应热的
的反应热的


