在25℃,101kPa,1gCH4气体完全燃烧生成液态水和CO2 ,放出的热量为55.6kJ,CH4燃烧热___________
更新时间:2023-03-28 21:59:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
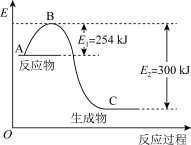
(1)如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量的变化示意图,请问该化学反应属于___________ (放热或吸热)反应,请写出该反应的热化学方程式:___________ 。
(2)上述反应用到的氢气是一种清洁燃料,已知氢气的燃烧热为285.8kJ·mol-1,又已知1molH2O(l)转化成1molH2O(g)吸收44kJ的热量,___________ molH2完全燃烧生成气态水可以放出120.9kJ的热量(不考虑热量损失)。
(3)肼(N2H4)是一种用于火箭或燃料电池的原料,已知:
①2H2O(g)+O2(g)=2H2O2(l) ΔH1=+108.0kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.0kJ·mol-1
则③N2H4(l)+2H2O2(l)=N2(g)+4H2O(l) ΔH3=___________ kJ·mol-1
(1)如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量的变化示意图,请问该化学反应属于

(2)上述反应用到的氢气是一种清洁燃料,已知氢气的燃烧热为285.8kJ·mol-1,又已知1molH2O(l)转化成1molH2O(g)吸收44kJ的热量,
(3)肼(N2H4)是一种用于火箭或燃料电池的原料,已知:
①2H2O(g)+O2(g)=2H2O2(l) ΔH1=+108.0kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.0kJ·mol-1
则③N2H4(l)+2H2O2(l)=N2(g)+4H2O(l) ΔH3=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】填空
(1)在25℃、101kPa下,1mol气态H2与0.5mol气态O2反应生成1mol气态H2O,放出241.8kJ的热量:_____________
(2)在25℃、101kPa下,1mol气态H2与足量气态O2反应生成1mol液态H2O,放出285.8kJ的热量:____________________
(1)在25℃、101kPa下,1mol气态H2与0.5mol气态O2反应生成1mol气态H2O,放出241.8kJ的热量:
(2)在25℃、101kPa下,1mol气态H2与足量气态O2反应生成1mol液态H2O,放出285.8kJ的热量:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)已知乙醇的燃烧热为-1366.8kJ/mol,写出相应的热化学方程式__ 。
(2)已知强酸强碱的中和热为-57.3kJ/mol,写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式:__ 。
(3)已知16g硫固体完全燃烧时放出148.4kJ的热量,则硫的燃烧热的热化学方程式:__ 。
(4)已知:101kPa时,2C(s)+O2(g)=2CO(g)ΔH=-221kJ/mol,则碳的燃烧热数值___ 110.5kJ/mol(填>,<,=)。
(5)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应生成1mol水,放出的热量___ 57.3kJ(填>,<,=)。
(6)已知一定条件下合成氨反应:N2(g)+3H2(g) 2NH3(g)ΔH=-92.0kJ·mol-1,相同条件下将1molN2和3molH2放在一密闭容器中充分反应,测得反应放出的热量
2NH3(g)ΔH=-92.0kJ·mol-1,相同条件下将1molN2和3molH2放在一密闭容器中充分反应,测得反应放出的热量___ (假定热量无损失)92.0kJ(填>,<,=)。
(7)相同条件下2mol氢原子所具有的能量___ 1mol氢分子所具有的能量(填>,<,=)
(2)已知强酸强碱的中和热为-57.3kJ/mol,写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式:
(3)已知16g硫固体完全燃烧时放出148.4kJ的热量,则硫的燃烧热的热化学方程式:
(4)已知:101kPa时,2C(s)+O2(g)=2CO(g)ΔH=-221kJ/mol,则碳的燃烧热数值
(5)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应生成1mol水,放出的热量
(6)已知一定条件下合成氨反应:N2(g)+3H2(g)
 2NH3(g)ΔH=-92.0kJ·mol-1,相同条件下将1molN2和3molH2放在一密闭容器中充分反应,测得反应放出的热量
2NH3(g)ΔH=-92.0kJ·mol-1,相同条件下将1molN2和3molH2放在一密闭容器中充分反应,测得反应放出的热量(7)相同条件下2mol氢原子所具有的能量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】以甲醇为原料,以KOH为电解质的手机充电电池,充一次电可以连续使用一个月。已知该电池的总反应式为2CH3OH+ 3O2+ 4KOH  2K2CO3+ 6H2O。请填空:
2K2CO3+ 6H2O。请填空:
(1)放电时:负极的电极反应式为_______ 。
(2)通入甲醇一端的电极是_______ 极,电池在放电过程中溶液的碱性将_______ (填“增强”“减弱”或“不变”)。
(3)若在常温、常压下,1 g液态CH3OH燃烧生成CO2和液态水时放出22. 68 kJ的热量,表示该反应的热化学方程式为_______ 。
 2K2CO3+ 6H2O。请填空:
2K2CO3+ 6H2O。请填空:(1)放电时:负极的电极反应式为
(2)通入甲醇一端的电极是
(3)若在常温、常压下,1 g液态CH3OH燃烧生成CO2和液态水时放出22. 68 kJ的热量,表示该反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知下列反应的反应热:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H=-870.3kJ∕mol
②C(s)+O2(g)=CO2(g) △H=-393.5kJ∕mol
③2C(s)+2H2(g)+O2(g)=CH3COOH(l) △H=-488.3kJ∕mol
请写出H2燃烧热的热化学方程式_______________________ 。
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H=-870.3kJ∕mol
②C(s)+O2(g)=CO2(g) △H=-393.5kJ∕mol
③2C(s)+2H2(g)+O2(g)=CH3COOH(l) △H=-488.3kJ∕mol
请写出H2燃烧热的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
(1)把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)=CO2(g) △H1<0 ①
途径II:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) △H2>0 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g) △H3<0 ③
2H2(g)+O2(g)=2H2O(g) △H4<0 ④
则途径I放出的热量_______ (填“大于”“等于”或“小于”)途径II放出的热量;△H1、△H2、△H3、△H4的数学关系式是_______ 。
(2)在25℃、101kPa下,1克甲醇完全燃料放热22.68kJ,写出甲醇燃烧热的热化学方程式_______ 。
(3)已知①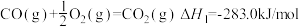
②H2(g)+ O2(g)=H2O(l) ΔH2=-285.8kJ/mol
O2(g)=H2O(l) ΔH2=-285.8kJ/mol
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH3=-1370kJ/mol
试计算④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的ΔH=_______ 。
(1)把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)=CO2(g) △H1<0 ①
途径II:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) △H2>0 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g) △H3<0 ③
2H2(g)+O2(g)=2H2O(g) △H4<0 ④
则途径I放出的热量
(2)在25℃、101kPa下,1克甲醇完全燃料放热22.68kJ,写出甲醇燃烧热的热化学方程式
(3)已知①
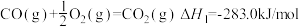
②H2(g)+
 O2(g)=H2O(l) ΔH2=-285.8kJ/mol
O2(g)=H2O(l) ΔH2=-285.8kJ/mol③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH3=-1370kJ/mol
试计算④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l)的ΔH=
您最近一年使用:0次



