甲同学通过查询资料知道,一定浓度的硝酸与镁反应时,可得到二氧化氮、一氧化氮、氮气三种气体。该同学用下列仪器组装装置来直接验证有二氧化氮,一氧化氮生成并制取氮化镁(假设实验中每步转化均是完全的)。
查阅文献得知:①二氧化氮沸点为21.1℃、熔点为-11℃,一氧化氮沸点为-151℃、熔点为-164℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。
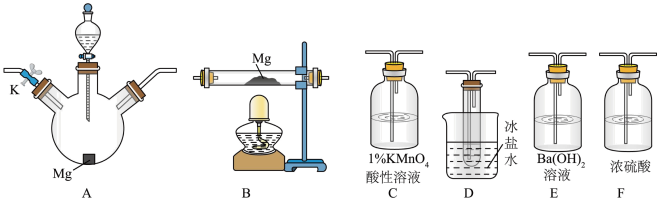
(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是___________ 。
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→___________ →E,确定还原产物中有二氧化氮的现象是___________ ,实验中要多次使用装置F,第二次使用F的目的是___________ 。
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:___________ 。
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是___________ 。
(5)取少量氮化镁于试管中,加入足量稀硝酸,没有气体逸出。取少量反应后的溶液于试管中,加入足量NaOH浓溶液,加热,用镊子夹一块湿润的红色石蕊试纸接近试管口,试纸变蓝色。则氮化镁溶于足量稀硝酸中发生反应的化学方程式为___________ 。
查阅文献得知:①二氧化氮沸点为21.1℃、熔点为-11℃,一氧化氮沸点为-151℃、熔点为-164℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。

(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是
(5)取少量氮化镁于试管中,加入足量稀硝酸,没有气体逸出。取少量反应后的溶液于试管中,加入足量NaOH浓溶液,加热,用镊子夹一块湿润的红色石蕊试纸接近试管口,试纸变蓝色。则氮化镁溶于足量稀硝酸中发生反应的化学方程式为
更新时间:2023-04-16 18:03:24
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】将浓度均为0.02mol•L-1的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学再室温下对该“碘钟实验”的原理进行探究。
资料:该“碘钟实验”的总反应为H2O2+2S2O +2H+=S4O
+2H+=S4O +2H2O,反应分两步进行,反应A:……;反应B:I2+2S2O
+2H2O,反应分两步进行,反应A:……;反应B:I2+2S2O =2I-+S4O
=2I-+S4O 。
。
(1)反应A的离子方程式是_____ ;对于总反应,I-的作用相当于_____ 。
(2)为证明反应A、B的存在,进行实验I.
实验I:
a.向酸化的H2O2溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入Na2S2O3溶液,溶液的蓝色褪去。
试剂X是_____
(3)为探究硫酸浓度对溶液变蓝快慢的影响,进行实验Ⅱ、实验Ⅲ.
(各溶液浓度均为0.02mol•L-1)
溶液从混合时的无色变为蓝色的时间:实验Ⅱ是15min,实验Ⅲ是20min。
①实验Ⅲ中,x、y、z所对应的数值分别是_____ 。
②对比试验Ⅱ、实验Ⅲ,可得出的实验结论是_____ 。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验Ⅳ.(各溶液浓度均为0.02mol•L-1)
实验过程中,溶液始终未出现变蓝的现象。试结合该“碘钟实验”总反应方程式,推测反应A与反应B速率的相对快慢关系:_____ 。
资料:该“碘钟实验”的总反应为H2O2+2S2O
 +2H+=S4O
+2H+=S4O +2H2O,反应分两步进行,反应A:……;反应B:I2+2S2O
+2H2O,反应分两步进行,反应A:……;反应B:I2+2S2O =2I-+S4O
=2I-+S4O 。
。(1)反应A的离子方程式是
(2)为证明反应A、B的存在,进行实验I.
实验I:
a.向酸化的H2O2溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入Na2S2O3溶液,溶液的蓝色褪去。
试剂X是
(3)为探究硫酸浓度对溶液变蓝快慢的影响,进行实验Ⅱ、实验Ⅲ.
(各溶液浓度均为0.02mol•L-1)
| 用量/mL | H2O2溶液 | H2SO4溶液 | Na2S2O3溶液 | 试剂X溶液 | H2O |
| 实验Ⅱ | 5 | 4 | 8 | 3 | 0 |
| 实验Ⅲ | 5 | 2 | x | y | z |
①实验Ⅲ中,x、y、z所对应的数值分别是
②对比试验Ⅱ、实验Ⅲ,可得出的实验结论是
(4)为探究其他因素对该“碘钟实验”的影响,进行实验Ⅳ.(各溶液浓度均为0.02mol•L-1)
| 用量/mL | H2O2溶液 | H2SO4溶液 | Na2S2O3溶液 | 试剂X溶液 | H2O |
| 实验Ⅳ | 4 | 4 | 9 | 3 | 0 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】某小组同学探究 与
与 溶液的反应,实验如下。
溶液的反应,实验如下。
资料:i.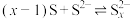 (黄色)
(黄色)
ii. 呈绿色(酸性条件下不稳定)、低浓度
呈绿色(酸性条件下不稳定)、低浓度 呈无色、MnS为肉色沉淀。
呈无色、MnS为肉色沉淀。
iii.
实验Ⅰ:
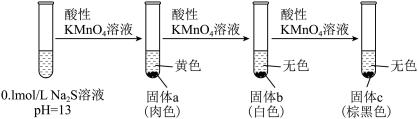
(1)用离子方程式表示 溶液显碱性的原因:
溶液显碱性的原因:_______ 。
(2)将固体a过滤、洗涤,放置在空气中,固体变为棕黑色。
①甲同学认为固体a中除了MnS外,还有 ,依据的现象是
,依据的现象是_______ 。
②乙同学认为根据上述现象不能得出固体a中含有 ,应补充对比实验:
,应补充对比实验:_______ (填实验方案)。实验证实固体a中含有 。
。
(3)固体b的主要成分是S。分析产生S的可能原因:_______ 。
经检验,固体c的主要成分是 。
。
①分析产生 的可能原因:酸性条件下,
的可能原因:酸性条件下, 将
将 氧化。
氧化。
②继续滴加酸性 溶液,溶液变为紫红色,仍有棕黑色固体。
溶液,溶液变为紫红色,仍有棕黑色固体。
实验Ⅱ:改用未经酸化的 溶液重复实验Ⅰ,产生棕黑色固体时溶液呈绿色。
溶液重复实验Ⅰ,产生棕黑色固体时溶液呈绿色。
(4)分析实验Ⅰ未见绿色的原因:取少量实验Ⅱ的绿色溶液,滴加硫酸,溶液变为紫红色,产生棕黑色固体。该反应的离子方程式是_______ 。
实验Ⅲ:向未经酸化的 溶液中滴加少量,产生棕黑色沉淀并检测到。
溶液中滴加少量,产生棕黑色沉淀并检测到。
(5)综合上述实验, 与
与 溶液反应的产物与
溶液反应的产物与_______ 等因素有关(答出两点即可)。
 与
与 溶液的反应,实验如下。
溶液的反应,实验如下。资料:i.
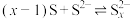 (黄色)
(黄色)ii.
 呈绿色(酸性条件下不稳定)、低浓度
呈绿色(酸性条件下不稳定)、低浓度 呈无色、MnS为肉色沉淀。
呈无色、MnS为肉色沉淀。iii.

实验Ⅰ:

(1)用离子方程式表示
 溶液显碱性的原因:
溶液显碱性的原因:(2)将固体a过滤、洗涤,放置在空气中,固体变为棕黑色。
①甲同学认为固体a中除了MnS外,还有
 ,依据的现象是
,依据的现象是②乙同学认为根据上述现象不能得出固体a中含有
 ,应补充对比实验:
,应补充对比实验: 。
。(3)固体b的主要成分是S。分析产生S的可能原因:
经检验,固体c的主要成分是
 。
。①分析产生
 的可能原因:酸性条件下,
的可能原因:酸性条件下, 将
将 氧化。
氧化。②继续滴加酸性
 溶液,溶液变为紫红色,仍有棕黑色固体。
溶液,溶液变为紫红色,仍有棕黑色固体。实验Ⅱ:改用未经酸化的
 溶液重复实验Ⅰ,产生棕黑色固体时溶液呈绿色。
溶液重复实验Ⅰ,产生棕黑色固体时溶液呈绿色。(4)分析实验Ⅰ未见绿色的原因:取少量实验Ⅱ的绿色溶液,滴加硫酸,溶液变为紫红色,产生棕黑色固体。该反应的离子方程式是
实验Ⅲ:向未经酸化的
 溶液中滴加少量,产生棕黑色沉淀并检测到。
溶液中滴加少量,产生棕黑色沉淀并检测到。(5)综合上述实验,
 与
与 溶液反应的产物与
溶液反应的产物与
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
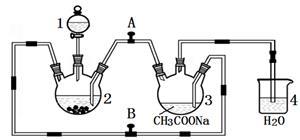
【推荐3】二价铬不稳定, 极易被氧气氧化。醋酸亚铬水合物{ [Cr(CH3COO)2]2·2H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水和醚,易溶于盐酸,是常用的氧气吸收剂。实验室中以锌粒、CrCl3溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如下图所示:
制备过程中发生的反应如下:
Zn(s) + 2HCl(aq) = ZnCl2(aq) + H2(g);
2CrCl3(aq) + Zn(s)= 2CrCl2 (aq) + ZnCl2(aq)
2Cr2+(aq) + 4CH3COO-(aq) + 2H2O(l) = [Cr(CH3COO)2]2·2H2O (s)
请回答下列问题:
(1)仪器1的名称是____________ , 所盛装的试剂是________________________ 。
(2)本实验中所用的溶液,配制用的蒸馏水都需事先煮沸,原因是__________________ 。
(3)实验开始生成H2气后, 为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应________ 阀门A、__________ 阀门B (填“打开”或“关闭”)。
(4)本实验中锌粒须过量,其原因是______________ ,_________________________ 。
(5)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质6.34 g,实验后得干燥纯净的[Cr(CH3COO)2]2·2H2O 5.64 g,请计算该实验所得产品的产率_____________ 。
(6)若使用该装置制备Fe(OH)2,且能较长时间看到Fe(OH)2白色沉淀现象。则在1、2、3中应装入的试剂依次为_________ 、___________ 、__________ 。(写化学式

制备过程中发生的反应如下:
Zn(s) + 2HCl(aq) = ZnCl2(aq) + H2(g);
2CrCl3(aq) + Zn(s)= 2CrCl2 (aq) + ZnCl2(aq)
2Cr2+(aq) + 4CH3COO-(aq) + 2H2O(l) = [Cr(CH3COO)2]2·2H2O (s)
请回答下列问题:
(1)仪器1的名称是
(2)本实验中所用的溶液,配制用的蒸馏水都需事先煮沸,原因是
(3)实验开始生成H2气后, 为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应
(4)本实验中锌粒须过量,其原因是
(5)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质6.34 g,实验后得干燥纯净的[Cr(CH3COO)2]2·2H2O 5.64 g,请计算该实验所得产品的产率
(6)若使用该装置制备Fe(OH)2,且能较长时间看到Fe(OH)2白色沉淀现象。则在1、2、3中应装入的试剂依次为
您最近一年使用:0次



