写出下列正确的化学方程式
(1)乙烯制聚乙烯:_______ ;
(2)乙醇与钠:_______ ;
(3)乙醇的燃烧:_______ ;
(4)乙烯与水:_______ ;
(5)淀粉水解:_______ ;
(6)冶炼金属镁:_______ ;
(7)冶炼金属铝:_______ ;
(8)铝热法炼铁:_______ 。
(1)乙烯制聚乙烯:
(2)乙醇与钠:
(3)乙醇的燃烧:
(4)乙烯与水:
(5)淀粉水解:
(6)冶炼金属镁:
(7)冶炼金属铝:
(8)铝热法炼铁:
更新时间:2023-07-10 10:19:29
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1) 2016中国首艘国产航母即将竣工,8艘052D驱逐舰下水,加快了我国海军迈向“蓝水海军”的步伐。

①舰艇底部涂有含Cu2O的防腐蚀涂料。Cu2O属于________ (填字母)。
a. 复合材料
b. 无机非金属材料
c. 有机高分子材料
②核动力航母中,钠钾合金(常温下呈液态)可用于快中子反应堆导热剂,是利用了钠钾合金性质的________ (填字母)。
a. 熔点低、沸点高 b. 导电性好 c. 在空气中性质不稳定
③航母中供水管道多采用PE(聚乙烯)材料,聚乙烯的化学式为________________ 。
(2)西兰花营养丰富,含蛋白质、淀粉、油脂、叶酸、维生素C和叶绿素,营养成分位居同类蔬菜之首,被誉为“蔬菜皇冠”。

①维生素C俗名为________ 。在一支盛有2 mL 2%淀粉溶液的试管中滴入2滴碘 水,溶液呈蓝色,再滴入维生素C的水溶液,溶液颜色变为________ ,该实验说明维生素C具有________ 性。
②油脂在人体内水解的最终产物是________ (写名称)和甘油。
③西兰花成分中可做天然着色剂的是________ ,属于糖类的是________ 。
(3) 2016年9月4日,G20峰会召开,扬州天空呈现出干净的蓝色,云彩随意地铺散在天空,纯净透明,出现了持续的“水晶天”。
①目前我国空气质量检测体系包括:PM2.5、SO2、NO2、O3、CO等指标。其中________ 被认为是引起雾霾天气的元凶;会引起硫酸型酸雨的气体为________ 。
②NH3催化还原氮氧化合物转化为无污染物质是目前应用最广泛的烟气氮氧化合物脱除技术,写出NH3催化还原NO2反应的化学方程式________________ 。
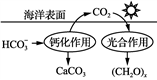
③减少CO2的排放对于环境保护具有重要意义。在海洋碳循环中,可通 过如图所示的途径固碳。写出钙化作用的离子方程式:________________ 。

①舰艇底部涂有含Cu2O的防腐蚀涂料。Cu2O属于
a. 复合材料
b. 无机非金属材料
c. 有机高分子材料
②核动力航母中,钠钾合金(常温下呈液态)可用于快中子反应堆导热剂,是利用了钠钾合金性质的
a. 熔点低、沸点高 b. 导电性好 c. 在空气中性质不稳定
③航母中供水管道多采用PE(聚乙烯)材料,聚乙烯的化学式为
(2)西兰花营养丰富,含蛋白质、淀粉、油脂、叶酸、维生素C和叶绿素,营养成分位居同类蔬菜之首,被誉为“蔬菜皇冠”。

①维生素C俗名为
②油脂在人体内水解的最终产物是
③西兰花成分中可做天然着色剂的是
(3) 2016年9月4日,G20峰会召开,扬州天空呈现出干净的蓝色,云彩随意地铺散在天空,纯净透明,出现了持续的“水晶天”。
①目前我国空气质量检测体系包括:PM2.5、SO2、NO2、O3、CO等指标。其中
②NH3催化还原氮氧化合物转化为无污染物质是目前应用最广泛的烟气氮氧化合物脱除技术,写出NH3催化还原NO2反应的化学方程式
③减少CO2的排放对于环境保护具有重要意义。在海洋碳循环中,可通 过如图所示的途径固碳。写出钙化作用的离子方程式:

您最近一年使用:0次
【推荐2】已知乙烯在一定条件下能发生下列转化;(反应条件未写出)
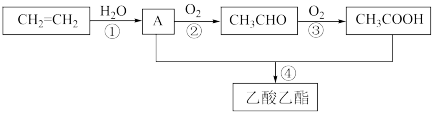
(1) 所含官能团的名称是
所含官能团的名称是______ ,实验室鉴别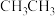 和
和 可选择下列哪些试剂?
可选择下列哪些试剂?______ (填字母)
A.溴的四氯化碳溶液 B.酸性高锰酸钾溶液 C.碳酸钠溶液
(2)写出A的结构简式:______ 。
(3) 的化学名称是
的化学名称是______ 。
(4)反应①的反应类型是______ 。
(5)写出反应④的化学反应方程式:______ 。

(1)
 所含官能团的名称是
所含官能团的名称是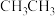 和
和 可选择下列哪些试剂?
可选择下列哪些试剂?A.溴的四氯化碳溶液 B.酸性高锰酸钾溶液 C.碳酸钠溶液
(2)写出A的结构简式:
(3)
 的化学名称是
的化学名称是(4)反应①的反应类型是
(5)写出反应④的化学反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)下列各组物质中,互为同位素的是_____________________ (填序号,下同);互为同素异形体的是_________________ ;互为同系物的是_____________________ ;互为同分异构体的是_____________________ ;属于同一种物质的是_____________________ 。_____________ 反应(填反应类型)。反应的方程式:_____________________________________________________________________________ 。
(1)下列各组物质中,互为同位素的是
① 和
和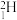 ;②
;② 和
和 ;③
;③ 和
和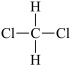 ;④石墨和金刚石;⑤正丁烷
;④石墨和金刚石;⑤正丁烷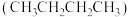 和异丁烷(
和异丁烷(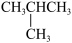 )⑥乙醇
)⑥乙醇 与二甲醚
与二甲醚
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】研究有机化合物中的典型代表物,对于有机合成的研究有重要意义。
(1)乙醇是醇类物质的典型代表物,乙醇分子结构中的各种化学键如图所示:___________ (填序号),该反应的类型属于___________ 。
②乙醇氧化可转化为乙醛,该反应断键位置是___________ (填序号)。
(2)乙酸乙酯是酯类物质的典型代表物,广泛用于药物、染料、香料等工业。实验室用无水乙醇、冰醋酸和浓硫酸反应可制备乙酸乙酯,常用装置如图所示。___________ 。
②试管X中的试剂为___________ ,作用是___________ 。
③为提高反应速率或限度,实验中采取的措施及对应理由不正确 的是___________ (填字母)。
a.浓硫酸可做催化剂,提高化学反应速率
b.浓硫酸可做吸水剂,促进反应向生成乙酸乙酯的反应移动
c.已知该反应为放热反应,升高温度可同时提高化学反应速率和反应限度
(3)三种常见羧酸的pKa数值如下表。(pKa数值越小,酸性越强)乙酸中的-CH3具有推电子作用,使羧基中羟基的极性减小,从而难以电离出H+,故乙酸的酸性比甲酸的酸性弱。
请比较乙酸与三氯乙酸的酸性强弱并解释原因___________ 。
(1)乙醇是醇类物质的典型代表物,乙醇分子结构中的各种化学键如图所示:

②乙醇氧化可转化为乙醛,该反应断键位置是
(2)乙酸乙酯是酯类物质的典型代表物,广泛用于药物、染料、香料等工业。实验室用无水乙醇、冰醋酸和浓硫酸反应可制备乙酸乙酯,常用装置如图所示。
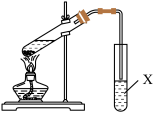
②试管X中的试剂为
③为提高反应速率或限度,实验中采取的措施及对应理由
a.浓硫酸可做催化剂,提高化学反应速率
b.浓硫酸可做吸水剂,促进反应向生成乙酸乙酯的反应移动
c.已知该反应为放热反应,升高温度可同时提高化学反应速率和反应限度
(3)三种常见羧酸的pKa数值如下表。(pKa数值越小,酸性越强)乙酸中的-CH3具有推电子作用,使羧基中羟基的极性减小,从而难以电离出H+,故乙酸的酸性比甲酸的酸性弱。
| 羧酸 | 甲酸(HCOOH) | 乙酸(CH3COOH) | 三氯乙酸(CCl3COOH) |
| pKa | 3.75 | 4.76 | 0.65 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】写出下对反应的化学方程式,并注明反应类型:
(1)乙醇制乙烯:_________________ ,反应类型:_________________ 。
(2)乙醇与浓氢溴酸反应:_________________ ,反应类型_________________ 。
(3)苯酚与浓溴水反应:_________________ ,反应类型_________________ 。
(4)乙醛与银氨溶液反应:_________________ ,反应类型_________________ 。
(5)乙醛与新制氢氧化铜悬浊液反应:_________________ ,反应类型_________________ 。
(6)乙酸乙酯与氢氧化钠溶液反应:_________________ ,反应类型_________________ 。
(1)乙醇制乙烯:
(2)乙醇与浓氢溴酸反应:
(3)苯酚与浓溴水反应:
(4)乙醛与银氨溶液反应:
(5)乙醛与新制氢氧化铜悬浊液反应:
(6)乙酸乙酯与氢氧化钠溶液反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下列物质都能发生水解反应,请说明水解的条件和生成物的类别:
(1)淀粉:___________
(2)油脂:___________
(3)蛋白质:___________
(1)淀粉:
(2)油脂:
(3)蛋白质:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)按表左边的实验操作,可观察到表中右边的实验现象。请从“实验现象”栏中选择正确选项的字母代号填入“答案”栏中。
(2)①糖类、油脂、蛋白质都是人体必需的营养物质。油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和_______ (写名称)。
②氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(-NH2)和_______ (写名称)。人体中共有二十多种氨基酸,其中人体自身_______ (填“能”或“不能”)合成的氨基酸称为人体必需氨基酸。
③淀粉在淀粉酶的作用下最终水解为_______ (写化学式),部分该产物在体内被氧化放出能量,供人体活动需要。
| 实验操作 | 答案 | 实验现象 |
| ①向鸡蛋清溶液中滴加少许浓硝酸,微热 | A.橙红色褪去 B.变为黄色 C.出现白色沉淀 D.液体不再分层,形成均一溶液 | |
| ②将植物油滴入少量溴的四氯化碳溶液中 | ||
| ③向鸡蛋清溶液中滴入少量醋酸铅溶液 | ||
| ④向花生油中加入足量浓NaOH溶液,加热,搅拌,静止 |
②氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(-NH2)和
③淀粉在淀粉酶的作用下最终水解为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】我国古代人民学会了利用含淀粉丰富的谷类物质发酵酿酒的方法,其过程可粗略表示如下:
过程Ⅰ:(C6H10O5)n+nH2O nC6H12O6
nC6H12O6
过程Ⅱ:C6H12O6 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑
请回答下列问题:
(1)C6H12O6的名称为__________ 。
(2)为检验过程Ⅰ是否反应完全,可向反应混合液中滴入______ ,观察溶液是否变______ 。
(3)“酒是陈的香”是因为酒在窖藏过程中生成的乙酸与乙醇反应生成具有香味的乙酸乙酯的结果。请写出该反应的化学方程式______ 。
(4)下列有关酶的说法不正确的是________ 。
A.酶是一类有机物,绝大多数是蛋白质
B.温度为30~50℃时,酶的活性最强
C.上述过程Ⅰ可以用蛋白酶作催化剂
D.生物体内的化学反应都离不开酶的催化
过程Ⅰ:(C6H10O5)n+nH2O
 nC6H12O6
nC6H12O6过程Ⅱ:C6H12O6
 2C2H5OH+2CO2↑
2C2H5OH+2CO2↑请回答下列问题:
(1)C6H12O6的名称为
(2)为检验过程Ⅰ是否反应完全,可向反应混合液中滴入
(3)“酒是陈的香”是因为酒在窖藏过程中生成的乙酸与乙醇反应生成具有香味的乙酸乙酯的结果。请写出该反应的化学方程式
(4)下列有关酶的说法不正确的是
A.酶是一类有机物,绝大多数是蛋白质
B.温度为30~50℃时,酶的活性最强
C.上述过程Ⅰ可以用蛋白酶作催化剂
D.生物体内的化学反应都离不开酶的催化
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据要求写出方程式:
(1)酸性高锰酸钾与草酸反应的化学方程式___ ;
(2)硫代硫酸钠(Na2S2O3)与稀硫酸反应的化学方程式___ ;
(3)工业上冶炼铝的化学方程式___ ;
(4)惰性电极电解氯化铝溶液的离子方程式___ ;
(5)酸性条件下铬酸钾与重铬酸钾转化的离子方程式___ ;
(6)已知某反应的化学平衡常数的表达式为K=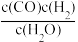 ,写出该反应的化学方程式
,写出该反应的化学方程式___ ;
(7)铅蓄电池的电池总反应化学方程式___ 。
(1)酸性高锰酸钾与草酸反应的化学方程式
(2)硫代硫酸钠(Na2S2O3)与稀硫酸反应的化学方程式
(3)工业上冶炼铝的化学方程式
(4)惰性电极电解氯化铝溶液的离子方程式
(5)酸性条件下铬酸钾与重铬酸钾转化的离子方程式
(6)已知某反应的化学平衡常数的表达式为K=
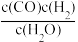 ,写出该反应的化学方程式
,写出该反应的化学方程式(7)铅蓄电池的电池总反应化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】钠及其化合物具有独特的性质和广泛的用途。
I.
(1)下图为钠与水反应的实验示意图。
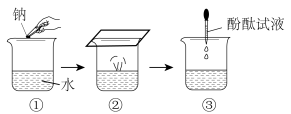
i.②中现象说明钠的密度比水___________ (“大”或“小”)。
ii.实验中观察到钠融成小球,下列能量变化示意图中能解释该现象的是___________ 。
a.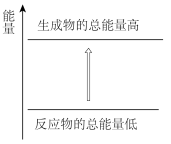 B.
B.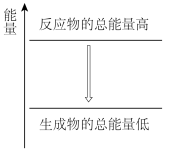
iii.③中加入酚酞试液后的现象是___________ 。
(2)用化学方程式表示由氯化钠制取金属钠的原理。___________
(3)将一定量的 通入
通入 溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入
溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入 盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
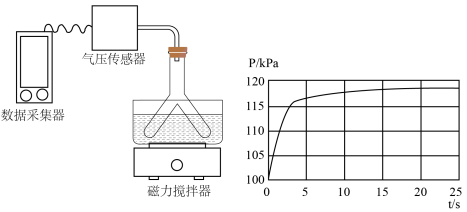
其中0~5s发生反应的离子方程式为___________ 。20s时溶液中的溶质是___________ (不考虑气体在水中的溶解)。
II.过碳酸钠( ),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:
),俗名固态双氧水,具有去污杀菌等功效。其制备原理为: (反应放热)
(反应放热)
(4)结合 和
和 的性质,推测制备过碳酸钠的原料中,
的性质,推测制备过碳酸钠的原料中, 与
与 的物质的量之比应
的物质的量之比应___________  。
。
A.大于 B.等于 C.小于
向 中加入
中加入 溶液的速度不能过快,原因是
溶液的速度不能过快,原因是___________ 。
(5)在过碳酸钠的生产过程中需要加入稳定剂,以得到稳定性好的过碳酸钠产品,保证其在一定贮存期内仍具有高活性的氧含量。以不同种类的稳定剂制备过碳酸钠产品,测得其活性氧质量分数随时间的变化如图所示:
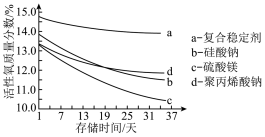
由图可知,制备过碳酸钠时应选择的稳定剂是___________ ,理由是___________ 。
A.a B.b C.c D.d
I.
(1)下图为钠与水反应的实验示意图。

i.②中现象说明钠的密度比水
ii.实验中观察到钠融成小球,下列能量变化示意图中能解释该现象的是
a.
 B.
B.
iii.③中加入酚酞试液后的现象是
(2)用化学方程式表示由氯化钠制取金属钠的原理。
(3)将一定量的
 通入
通入 溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入
溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入 盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
其中0~5s发生反应的离子方程式为
II.过碳酸钠(
 ),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:
),俗名固态双氧水,具有去污杀菌等功效。其制备原理为: (反应放热)
(反应放热)(4)结合
 和
和 的性质,推测制备过碳酸钠的原料中,
的性质,推测制备过碳酸钠的原料中, 与
与 的物质的量之比应
的物质的量之比应 。
。A.大于 B.等于 C.小于
向
 中加入
中加入 溶液的速度不能过快,原因是
溶液的速度不能过快,原因是(5)在过碳酸钠的生产过程中需要加入稳定剂,以得到稳定性好的过碳酸钠产品,保证其在一定贮存期内仍具有高活性的氧含量。以不同种类的稳定剂制备过碳酸钠产品,测得其活性氧质量分数随时间的变化如图所示:

由图可知,制备过碳酸钠时应选择的稳定剂是
A.a B.b C.c D.d
您最近一年使用:0次



