钠及其化合物具有独特的性质和广泛的用途。
I.
(1)下图为钠与水反应的实验示意图。
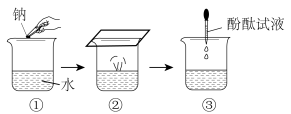
i.②中现象说明钠的密度比水___________ (“大”或“小”)。
ii.实验中观察到钠融成小球,下列能量变化示意图中能解释该现象的是___________ 。
a.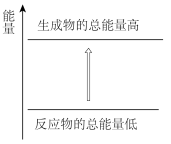 B.
B.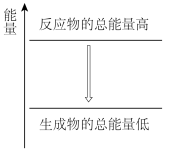
iii.③中加入酚酞试液后的现象是___________ 。
(2)用化学方程式表示由氯化钠制取金属钠的原理。___________
(3)将一定量的 通入
通入 溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入
溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入 盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
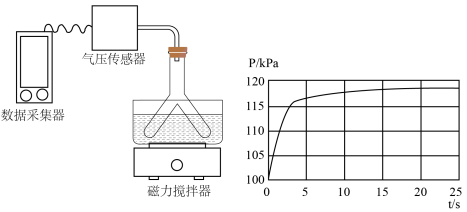
其中0~5s发生反应的离子方程式为___________ 。20s时溶液中的溶质是___________ (不考虑气体在水中的溶解)。
II.过碳酸钠( ),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:
),俗名固态双氧水,具有去污杀菌等功效。其制备原理为: (反应放热)
(反应放热)
(4)结合 和
和 的性质,推测制备过碳酸钠的原料中,
的性质,推测制备过碳酸钠的原料中, 与
与 的物质的量之比应
的物质的量之比应___________  。
。
A.大于 B.等于 C.小于
向 中加入
中加入 溶液的速度不能过快,原因是
溶液的速度不能过快,原因是___________ 。
(5)在过碳酸钠的生产过程中需要加入稳定剂,以得到稳定性好的过碳酸钠产品,保证其在一定贮存期内仍具有高活性的氧含量。以不同种类的稳定剂制备过碳酸钠产品,测得其活性氧质量分数随时间的变化如图所示:
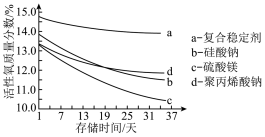
由图可知,制备过碳酸钠时应选择的稳定剂是___________ ,理由是___________ 。
A.a B.b C.c D.d
I.
(1)下图为钠与水反应的实验示意图。

i.②中现象说明钠的密度比水
ii.实验中观察到钠融成小球,下列能量变化示意图中能解释该现象的是
a.
 B.
B.
iii.③中加入酚酞试液后的现象是
(2)用化学方程式表示由氯化钠制取金属钠的原理。
(3)将一定量的
 通入
通入 溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入
溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入 盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
其中0~5s发生反应的离子方程式为
II.过碳酸钠(
 ),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:
),俗名固态双氧水,具有去污杀菌等功效。其制备原理为: (反应放热)
(反应放热)(4)结合
 和
和 的性质,推测制备过碳酸钠的原料中,
的性质,推测制备过碳酸钠的原料中, 与
与 的物质的量之比应
的物质的量之比应 。
。A.大于 B.等于 C.小于
向
 中加入
中加入 溶液的速度不能过快,原因是
溶液的速度不能过快,原因是(5)在过碳酸钠的生产过程中需要加入稳定剂,以得到稳定性好的过碳酸钠产品,保证其在一定贮存期内仍具有高活性的氧含量。以不同种类的稳定剂制备过碳酸钠产品,测得其活性氧质量分数随时间的变化如图所示:

由图可知,制备过碳酸钠时应选择的稳定剂是
A.a B.b C.c D.d
更新时间:2023/05/18 18:39:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】写出下列反应的离子方程式。
(1) 和
和 的反应
的反应_______ ;
(2)Cl2与 的反应
的反应_______ ;
(3) 和
和 的反应
的反应_______ ;
(4)Ba(OH)2与NaHSO4反应后溶液呈中性_______ ;
(5)稀的NH4HSO4溶液与足量稀的NaOH溶液混合_______ ;
(6)将 溶液与少量澄清石灰水混合
溶液与少量澄清石灰水混合_______ 。
(1)
 和
和 的反应
的反应(2)Cl2与
 的反应
的反应(3)
 和
和 的反应
的反应(4)Ba(OH)2与NaHSO4反应后溶液呈中性
(5)稀的NH4HSO4溶液与足量稀的NaOH溶液混合
(6)将
 溶液与少量澄清石灰水混合
溶液与少量澄清石灰水混合
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A是一种金属单质,B是一种淡黄色固体。相关物质的转化关系如图所示,回答下列问题:

(1)B的化学式为_______ ;
(2)A也能与水反应生成C,写出相应的化学方程式:_______ ;C中含有的化学键类型为_______ ;
(3)D是84消毒液的有效成分,该物质的名称是_______ ,与空气中的水和二氧化碳反应后具有_______ 作用。

(1)B的化学式为
(2)A也能与水反应生成C,写出相应的化学方程式:
(3)D是84消毒液的有效成分,该物质的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)钠与氧气的反应会因条件不同而导致现象不同,产物不同,反应的实质也不同。据此回答下列问题:
①常温下,在空气中切开金属钠,钠的断面由银白色逐渐变暗而失去金属光泽,请用化学方程式解释这种现象产生的原因:__________________ 。
②钠在空气中受热所发生反应的化学方程式是__________________ 。
③将4.6克钠投入足量水中,标况下生成气体的体积是__________ 。
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为____________ 。
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为___________________________________ 。
③实验室制备Al(OH)3的常用方法是向Al2(SO4)3溶液中逐滴滴加氨水至过量,请写出对应的化学方程式:___________________________________ 。
(3)铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
①中国古代四大发明之一的指南针是由天然磁石制成的,其主要成分是_______ 。
②写出磁石的主要成分和盐酸反应的离子方程式______________ 。
①常温下,在空气中切开金属钠,钠的断面由银白色逐渐变暗而失去金属光泽,请用化学方程式解释这种现象产生的原因:
②钠在空气中受热所发生反应的化学方程式是
③将4.6克钠投入足量水中,标况下生成气体的体积是
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
③实验室制备Al(OH)3的常用方法是向Al2(SO4)3溶液中逐滴滴加氨水至过量,请写出对应的化学方程式:
(3)铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
①中国古代四大发明之一的指南针是由天然磁石制成的,其主要成分是
②写出磁石的主要成分和盐酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.化学科学在药物的开发、合成和使用中具有至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可疗胃酸过多,硫胶亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:________________________ 。
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾、过氧化氢),__________ (填写实验操作、现象和结论)
(3)氢氧化亚铁在空气中极不稳定,易被空气中氧气氧化。这一过程中观察到的现象是__________ ,反应的化学方程式是______________ 。
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(4)镁铝合金的硬度比金属铝的硬度______ (选填:大、小)。使用该合金前用NaOH溶液处理Al2O3,其离子方程式为_________ 。取一定量的镁铝合金均分为两份,分别与足量的盐酸、NaOH溶液充分反应,产生气体的物质的量之比为5:3。合金与NaOH溶液反应的化学方程式为__________ 。合金中镁铝的物质的量之比为_____________ 。
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
(2)利用提供试剂设计实验证明补铁剂中只含亚铁盐(可选试剂:氯水、硫氰化钾、过氧化氢),
(3)氢氧化亚铁在空气中极不稳定,易被空气中氧气氧化。这一过程中观察到的现象是
Ⅱ.镁铝合金是建造航空母舰的主体材料。
(4)镁铝合金的硬度比金属铝的硬度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了 C2H5OH、CO2、Fe2O3、FeCl3、KOH五种物质,图中相连的物质均可归为一类,相交部分 A、B、C、D 为相应的分类标准代号:
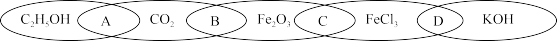
①相连的两种物质都是电解质的是_____ (填分类标准代号,下同)。
②图中相连的两种物质能够相互反应的是_____ ,所属基本反应类型的是_____ 反应。
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的化学方程式为_____
④用洁净的烧杯取 25mL 蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热至液体呈红褐色,证明该分散系生成的实验原理是_____ 。
(2)分类方法应用比较广泛,属于同一类的物质具有相似性,在生活和学习中使用分类的方法处理问题,可以做到举一反三,还可以做到由此及彼。如:
①CO2、SiO2、SO2、SO3都属于酸性氧化物,由 CO2+Ca(OH)2=CaCO3↓+H2O,可完成 SO3与NaOH反应的方程式为_____ 。
②NaHCO3、NaHSO3、NaHS 都属于弱酸形成的酸式盐,由 NaHCO3+HCl=NaCl+H2O+CO2↑及NaHCO3+NaOH=Na2CO3+H2O,可完成 NaHS 分别与 HCl、NaOH 反应的方程式为___________ 。
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了 C2H5OH、CO2、Fe2O3、FeCl3、KOH五种物质,图中相连的物质均可归为一类,相交部分 A、B、C、D 为相应的分类标准代号:
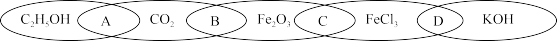
①相连的两种物质都是电解质的是
②图中相连的两种物质能够相互反应的是
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应的化学方程式为
④用洁净的烧杯取 25mL 蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热至液体呈红褐色,证明该分散系生成的实验原理是
(2)分类方法应用比较广泛,属于同一类的物质具有相似性,在生活和学习中使用分类的方法处理问题,可以做到举一反三,还可以做到由此及彼。如:
①CO2、SiO2、SO2、SO3都属于酸性氧化物,由 CO2+Ca(OH)2=CaCO3↓+H2O,可完成 SO3与NaOH反应的方程式为
②NaHCO3、NaHSO3、NaHS 都属于弱酸形成的酸式盐,由 NaHCO3+HCl=NaCl+H2O+CO2↑及NaHCO3+NaOH=Na2CO3+H2O,可完成 NaHS 分别与 HCl、NaOH 反应的方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。已知将1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知将1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
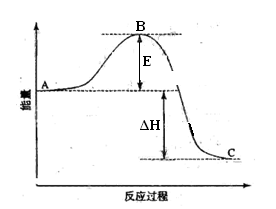
(1)图中A、C分别表示________ 、_________ ,E的大小对该反应的反应热有无影响?_______ 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?_________ 。
(2)图中△H=____________ kJ·mol-1。
 2SO3(g)反应过程的能量变化如图所示。已知将1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知将1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
(1)图中A、C分别表示
(2)图中△H=
您最近一年使用:0次
【推荐2】已知H-H 键、N-H 键、N≡N 键的键能分别为 436kJ/mol、391kJ/mol、946 kJ/mol,关于工业合成氨的反应,请根据键能的数据判断下列问题:
若有 1 mol NH3生成 ,可________ (填“吸收”或“放出”)热量________ kJ;该反应的能量变化可用图__________ 表示。(填“甲“或“乙”)

若有 1 mol NH3生成 ,可

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某实验小组设计了下图所示的5组实验,探究化学能与热能的转化。_______ ,反应的化学方程式是_______ 。
(2)实验②中反应的能量变化可用下图中的_______ (填序号A或B)表示_______ (填序号)
(4)从微观角度分析实验⑤化学反应中能量变化的原因:_______ 、_______ (填“吸收”或“释放”)。氢气与氧气反应生成1mol水蒸气时,释放_______ kJ能量。

(2)实验②中反应的能量变化可用下图中的

(4)从微观角度分析实验⑤化学反应中能量变化的原因:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】门捷列夫在研究周期表时预言了包括“类铝”、“类硅”在内的11种元素。回答下列问题:
Ⅰ. “类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
(1)铝是一种活泼金属,工业上采用电解熔融Al2O3制备金属Al。电解反应方程式为2Al2O3 4Al+3O2↑,加入冰晶石的目的是
4Al+3O2↑,加入冰晶石的目的是_______ 。Al可以与NaOH溶液反应生成Na[Al(OH)4]与H2,该反应的离子方程式为_______ 。
(2)镓与铝同主族,且位于铝的下一周期,则镓的原子结构示意图为_______ 。
(3)废弃的含GaAs的材料可以用浓硝酸溶解,放出红棕色气体,同时生成H3AsO4和Ga(NO3)3,该反应的化学方程式为_______ 。
Ⅱ.门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(Ge)。
(4)硅是应用最为广泛的半导体材料,写出高纯硅的两种用途:_______ 、_______ 。
(5)写出SiCl4的电子式:_______
(6)硅和锗单质分别与H2反应时,反应较难进行的是_______ (填“硅”或“锗”)。
Ⅰ. “类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
(1)铝是一种活泼金属,工业上采用电解熔融Al2O3制备金属Al。电解反应方程式为2Al2O3
 4Al+3O2↑,加入冰晶石的目的是
4Al+3O2↑,加入冰晶石的目的是(2)镓与铝同主族,且位于铝的下一周期,则镓的原子结构示意图为
(3)废弃的含GaAs的材料可以用浓硝酸溶解,放出红棕色气体,同时生成H3AsO4和Ga(NO3)3,该反应的化学方程式为
Ⅱ.门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(Ge)。
(4)硅是应用最为广泛的半导体材料,写出高纯硅的两种用途:
(5)写出SiCl4的电子式:
(6)硅和锗单质分别与H2反应时,反应较难进行的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)铝热反应可用于定向爆破,写出铝和四氧化三铁反应的化学方程式___________________ ;
(2)利用金属活泼性的不同,可采用不同的冶炼方法,写出工业制铝的化学方程式___________________ 。
(2)利用金属活泼性的不同,可采用不同的冶炼方法,写出工业制铝的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)根据A~E几种烃分子的结构填空。
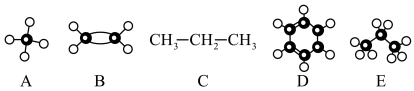
上述分子中属于C的同系物的是_____________ (填字母序号)。
(2)随着工业的发展和社会的进步,人们日益关注环境问题。
①下列物质属于室内空气污染物的是__________________ (填字母序号,下同);
A CO2 B 甲醛 C N2
②按照垃圾分类的方法,易拉罐瓶属于________________________ ;
A 可回收物 B 可堆肥垃圾
③工业废水需处理达标后才能排放。下列废水处理的方法合理的是__________ 。
A 用氯气除去废水中的悬浮物 B 用中和法除去废水中的酸
C 用明矾除去废水中的重金属离子
(3)化学是材料科学发展的基础,合理使用材料有利于人类的生产和生活。
①在一定条件下,将某种单体进行加聚反应得到一种如下图所示的导电性塑料:
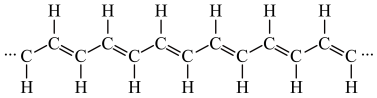
则合成该塑料的单体为___________ (填字母序号,下同);
A 乙炔 B 乙烯 C 乙烷 D 甲烷
②工业炼铁通常采用的方法是__________ ;
A 加热分解法 B 电解法 C 高温还原法
③某同学欲探究铁在NaCl溶液、蒸馏水和空气中锈蚀的快慢,设计了如下实验。
一周后,试管中铁钉锈蚀程度最大的是__________ ;
④将质量相同的铁片、铜片用导线连接后浸入硫酸铜溶液中,构成原电池,工作一段时间后铜片质量与铁片质量相差12 g,则理论上导线中通过______ mol电子。
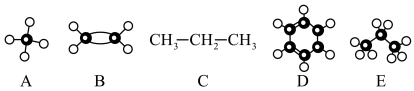
上述分子中属于C的同系物的是
(2)随着工业的发展和社会的进步,人们日益关注环境问题。
①下列物质属于室内空气污染物的是
A CO2 B 甲醛 C N2
②按照垃圾分类的方法,易拉罐瓶属于
A 可回收物 B 可堆肥垃圾
③工业废水需处理达标后才能排放。下列废水处理的方法合理的是
A 用氯气除去废水中的悬浮物 B 用中和法除去废水中的酸
C 用明矾除去废水中的重金属离子
(3)化学是材料科学发展的基础,合理使用材料有利于人类的生产和生活。
①在一定条件下,将某种单体进行加聚反应得到一种如下图所示的导电性塑料:

则合成该塑料的单体为
A 乙炔 B 乙烯 C 乙烷 D 甲烷
②工业炼铁通常采用的方法是
A 加热分解法 B 电解法 C 高温还原法
③某同学欲探究铁在NaCl溶液、蒸馏水和空气中锈蚀的快慢,设计了如下实验。
| 实验序号 | A | B | C |
| 实验 内容 | 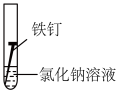 | 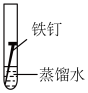 | 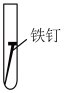 |
一周后,试管中铁钉锈蚀程度最大的是
④将质量相同的铁片、铜片用导线连接后浸入硫酸铜溶液中,构成原电池,工作一段时间后铜片质量与铁片质量相差12 g,则理论上导线中通过
您最近一年使用:0次



