门捷列夫在研究周期表时预言了包括“类铝”、“类硅”在内的11种元素。回答下列问题:
Ⅰ. “类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
(1)铝是一种活泼金属,工业上采用电解熔融Al2O3制备金属Al。电解反应方程式为2Al2O3 4Al+3O2↑,加入冰晶石的目的是
4Al+3O2↑,加入冰晶石的目的是_______ 。Al可以与NaOH溶液反应生成Na[Al(OH)4]与H2,该反应的离子方程式为_______ 。
(2)镓与铝同主族,且位于铝的下一周期,则镓的原子结构示意图为_______ 。
(3)废弃的含GaAs的材料可以用浓硝酸溶解,放出红棕色气体,同时生成H3AsO4和Ga(NO3)3,该反应的化学方程式为_______ 。
Ⅱ.门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(Ge)。
(4)硅是应用最为广泛的半导体材料,写出高纯硅的两种用途:_______ 、_______ 。
(5)写出SiCl4的电子式:_______
(6)硅和锗单质分别与H2反应时,反应较难进行的是_______ (填“硅”或“锗”)。
Ⅰ. “类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。
(1)铝是一种活泼金属,工业上采用电解熔融Al2O3制备金属Al。电解反应方程式为2Al2O3
 4Al+3O2↑,加入冰晶石的目的是
4Al+3O2↑,加入冰晶石的目的是(2)镓与铝同主族,且位于铝的下一周期,则镓的原子结构示意图为
(3)废弃的含GaAs的材料可以用浓硝酸溶解,放出红棕色气体,同时生成H3AsO4和Ga(NO3)3,该反应的化学方程式为
Ⅱ.门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现,命名为锗(Ge)。
(4)硅是应用最为广泛的半导体材料,写出高纯硅的两种用途:
(5)写出SiCl4的电子式:
(6)硅和锗单质分别与H2反应时,反应较难进行的是
更新时间:2023-11-14 14:13:07
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】有以下物质:①FeCl3;②稀NaOH溶液;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;⑦稀盐酸;⑧纯醋酸;⑨Na2CO3;
(1)其中能导电的是____________ ;属于非电解质的是______________ ;属于强电解质的是____________ ;属于弱电解质的是______________ 。
(2)写出物质⑥溶于水的电离方程式:___________________ 。
(3)写出物质⑥和⑧在水中反应的离子方程式__________________ 。
(4)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______
(5)现取0.1mol样品⑨,逐滴加入⑦,现象为_________ ,其所发生的离子方程式为___ 。完全反应时生成气体的物质的量为__________ 。
(1)其中能导电的是
(2)写出物质⑥溶于水的电离方程式:
(3)写出物质⑥和⑧在水中反应的离子方程式
(4)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是
(5)现取0.1mol样品⑨,逐滴加入⑦,现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)如图所示是在一定温度下向不同电解质溶液中加入新物质时其电流强度(I)随新物质加入量(m)的变化曲线。以下a、b、c三个导电性实验,其中与A图变化趋势一致的是_________________ ,与B图变化趋势一致的是______________ ,与 C图变化趋势一致的是_________________ 。
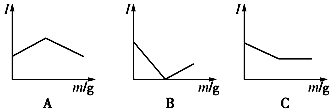
a.向Ba(OH)2溶液中逐滴加入等浓度的H2SO4溶液至过量
b.向醋酸溶液中逐滴加入等浓度的氨水至过量
c.向盐酸中逐滴加入等浓度的NaOH溶液至过量
(2)写出第(1)中,选项b所描述的离子反应方程式____________________ 。
(3)写出制备氢氧化铁胶体的化学反应方程式:_______________________ 。
在氢氧化铁胶体中加入足量的盐酸,能观察到的现象是:____________________ 。

a.向Ba(OH)2溶液中逐滴加入等浓度的H2SO4溶液至过量
b.向醋酸溶液中逐滴加入等浓度的氨水至过量
c.向盐酸中逐滴加入等浓度的NaOH溶液至过量
(2)写出第(1)中,选项b所描述的离子反应方程式
(3)写出制备氢氧化铁胶体的化学反应方程式:
在氢氧化铁胶体中加入足量的盐酸,能观察到的现象是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)我国是世界上最早使用湿法炼铜的国家。湿法炼铜的原理是Fe+CuSO4=FeSO4+Cu,其中CuSO4被_______ (填“氧化”或“还原”),铁作_______ (填“氧化剂”或“还原剂”)。在该反应中,若生成了32 g Cu,消耗Fe的物质的量是_______ 。
(2)某学习小组设计下图所示装置观察氧化还原反应中电子的转移。
①实验Ⅰ中,Fe与CuSO4溶液反应的离子方程式是_______ 。
②根据实验Ⅰ的原理,推测实验Ⅱ中:锌片上发生_______ (填“氧化反应”或“还原反应”);铜片上的实验现象是_______ 。
(1)我国是世界上最早使用湿法炼铜的国家。湿法炼铜的原理是Fe+CuSO4=FeSO4+Cu,其中CuSO4被
(2)某学习小组设计下图所示装置观察氧化还原反应中电子的转移。
| 实验I | 实验II | |
| 装置 | 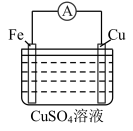 | 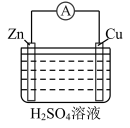 |
| 现象 | 电流计指针向右偏转;铁片溶解;铜片上有红色物质(铜)析出,铜片质量增加 | 电流计指针向右偏转;…… |
②根据实验Ⅰ的原理,推测实验Ⅱ中:锌片上发生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)配平下列化学方程式或离子方程式:
 ______MnO2 + ______HCl(浓)Δ_ ____MnCl2 +_____
______MnO2 + ______HCl(浓)Δ_ ____MnCl2 +_____ ______
______
_________
 _____
_____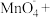 ____
____ ____H2O -----_____
____H2O -----_____ ____
____ __ _____
__ _____ _________
(2)用双线桥表示出下列反应中电子转移方向和数目
①3S + 6KOH = 2K2S + K2SO3 + 3H2O___________
②KClO3 + 6HCl = KCl + 3Cl2↑ + 3H2O_________
 ______MnO2 + ______HCl(浓)Δ_ ____MnCl2 +_____
______MnO2 + ______HCl(浓)Δ_ ____MnCl2 +_____ ______
______
 _____
_____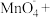 ____
____ ____H2O -----_____
____H2O -----_____ ____
____ __ _____
__ _____ (2)用双线桥表示出下列反应中电子转移方向和数目
①3S + 6KOH = 2K2S + K2SO3 + 3H2O
②KClO3 + 6HCl = KCl + 3Cl2↑ + 3H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】碘是人体必需的微量元素,也可用于工业、医药等领域。大量的碘富集于海藻灰〔主要成分是NaI)中,因此从海藻灰中提取碘,可有效利用海洋资源。
(1)某兴趣小组以海藻灰为原料进行I2的制备实验。具体步骤如下:将海藻灰加热浸泡后,得到了NaI溶液,将适量Na2SO3固体溶于NaI溶液,再将CuSO4饱和溶液滴入上述溶液中,生成白色CuI沉淀,该反应的离子方程式为______ 。
(2)待I-沉淀完全后,过滤,将沉淀物置于小烧杯中,在搅拌下逐滴加入适量浓HNO3,观察到______ (颜色)气体放出,______ (颜色)晶体析出。出于安全和环保考虑,该实验操作需在______ (条件)下进行。该反应的化学方程式为______ 。
(1)某兴趣小组以海藻灰为原料进行I2的制备实验。具体步骤如下:将海藻灰加热浸泡后,得到了NaI溶液,将适量Na2SO3固体溶于NaI溶液,再将CuSO4饱和溶液滴入上述溶液中,生成白色CuI沉淀,该反应的离子方程式为
(2)待I-沉淀完全后,过滤,将沉淀物置于小烧杯中,在搅拌下逐滴加入适量浓HNO3,观察到
您最近一年使用:0次
【推荐3】近来,《饮用天然矿泉水》新标准引起热议,其中备受争议的溴酸盐是一种致癌物,新标准中溴酸盐限值为0.01mg/L。已知在酸性条件下有以下反应:
①2BrO3-+I2→2IO3-+Br2;
②2IO3-+10Br-+12H+→I2+5Br2+6H2O;
③5Br-+BrO3-+6H+→3Br2+3H2O。
请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由___ 。
(2)反应②中:IO3-→I2发生的是___ 反应(选填“氧化”、“还原”)。
现向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图所示关系:
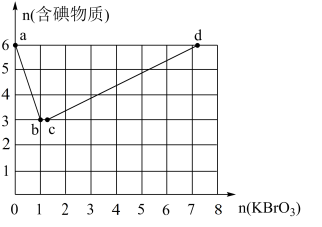
(3)a→b阶段的反应为(写出产物并配平)I-+BrO3-+H+→___ 。
(4)b→c阶段为反应③,其中氧化产物和还原产物的物质的量之比为___ 。
①2BrO3-+I2→2IO3-+Br2;
②2IO3-+10Br-+12H+→I2+5Br2+6H2O;
③5Br-+BrO3-+6H+→3Br2+3H2O。
请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由
(2)反应②中:IO3-→I2发生的是
现向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图所示关系:

(3)a→b阶段的反应为(写出产物并配平)I-+BrO3-+H+→
(4)b→c阶段为反应③,其中氧化产物和还原产物的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)第三周期元素的原子所形成的简单离子中:半径最大的阴离子是__ ;氧化性最强的阳离子是__ .
(2)下列事实可以作为S和Cl非金属性强弱的判断依据的是__ (选填序号)
a.Cl的最高正价比S高 b.可用浓H2SO4制HCl
c.HCl的酸性比H2S强 d.Cl2与H2S反应生成S.
(3)硅元素最外层有__ 种能量不同的电子;SiCl4的空间构型和CH4相同,写出SiCl4的电子式:__ .
(4)PH3和NH3的某些化学性质相似.下列对晶体PH4I性质的推测,错误的是__ (选填序号)
a.PH4I是一种共价化合物 b.PH4I能与烧碱溶液反应
c.PH4I加热后会发生升华 d.PH4I溶液能与溴水反应.
(5)二氯化二硫(S2C12)可用作橡胶工业的硫化剂,它的分子结构与H2O2相似.下列有关说法不正确的是__ (选填序号)
a.S2C12分子中有4对共用电子对
b.S2C12分子中没有非极性键
c.S2C12分子中,S为+1价,Cl为﹣1价
d.S2C12分子中各原子均为8电子稳定结构.
(1)第三周期元素的原子所形成的简单离子中:半径最大的阴离子是
(2)下列事实可以作为S和Cl非金属性强弱的判断依据的是
a.Cl的最高正价比S高 b.可用浓H2SO4制HCl
c.HCl的酸性比H2S强 d.Cl2与H2S反应生成S.
(3)硅元素最外层有
(4)PH3和NH3的某些化学性质相似.下列对晶体PH4I性质的推测,错误的是
a.PH4I是一种共价化合物 b.PH4I能与烧碱溶液反应
c.PH4I加热后会发生升华 d.PH4I溶液能与溴水反应.
(5)二氯化二硫(S2C12)可用作橡胶工业的硫化剂,它的分子结构与H2O2相似.下列有关说法不正确的是
a.S2C12分子中有4对共用电子对
b.S2C12分子中没有非极性键
c.S2C12分子中,S为+1价,Cl为﹣1价
d.S2C12分子中各原子均为8电子稳定结构.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图是元素周期表的一部分:
(1)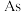 元素在周期表中的位置是
元素在周期表中的位置是___________ 。比较酸性:H3AsO4___________ H2SeO4(选填“>”或“<”)。用离子符号表示元素③、④、⑤的简单离子半径由大到小排序为___________ 。
(2)元素②的最简气态氢化物分子的空间构型为___________ ,用一个化学方程式表示元素①、②非金属性的强弱。___________ 从原子结构的角度解释元素⑤、⑥非金属性的强弱___________ 。
| ① | ② | ③ | ||
| ④ | P | ⑤ | ⑥ | |
| Ga | Ge | As | Se | Br |
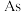 元素在周期表中的位置是
元素在周期表中的位置是(2)元素②的最简气态氢化物分子的空间构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,针对表中的①〜⑩种元素,填写下列空白:
(1)上述元素中,形成化合物种类最多的是_____________ (填元素符号)。
(2)元素①、④和⑤形成的化合物的电子式是_______ ,该化合物中存在的化学键类型是_______ 。
(3)②、③、⑧三种元素原子半径由大到小的顺序是___________ (用元素符号表示)。
(4)⑤、⑥、⑦三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是______________ 。(用对应物质的化学式表示)
(5)元素⑦和⑨最高价氧化物对应的水化物相互反应的离子方程式为___________________ 。
(6)能比较元素⑨和⑩非金属性强弱的实验事实是_________ (填字母序号)。
a.⑨的氢化物的酸性比⑩的氢化物的酸性弱
b.⑩的单质R2与H2化合比⑨的单质Q与H2化合容易,且HR的稳定性比H2Q强
c.在⑨的氢化物H2Q的水溶液中通少量⑩的单质R2气体可置换出单质Q
族 周期 | IA | IIA | ⅢA | IVA | VA | VIA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)上述元素中,形成化合物种类最多的是
(2)元素①、④和⑤形成的化合物的电子式是
(3)②、③、⑧三种元素原子半径由大到小的顺序是
(4)⑤、⑥、⑦三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是
(5)元素⑦和⑨最高价氧化物对应的水化物相互反应的离子方程式为
(6)能比较元素⑨和⑩非金属性强弱的实验事实是
a.⑨的氢化物的酸性比⑩的氢化物的酸性弱
b.⑩的单质R2与H2化合比⑨的单质Q与H2化合容易,且HR的稳定性比H2Q强
c.在⑨的氢化物H2Q的水溶液中通少量⑩的单质R2气体可置换出单质Q
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na,电解反应方程式如下: 。加入
。加入 的目的是
的目的是___________ 。
 。加入
。加入 的目的是
的目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】冶炼金属常用以下几种方法:
①热分解法 ②以活泼金属Na、Mg等还原 ③以C、CO或H2做还原剂
④电解法 ⑤利用铝热反应原理还原
请将下列金属所采用的最佳冶炼方法填写在相应空白处(填写序号,每项只填写一种方法)。
(1)Fe、Zn、Cu等中等活泼金属________________________________ 。
(2)Na、Mg、Al等活泼或较活泼金属____________________________ 。
(3)Hg、Ag等不活泼金属______________________________________ 。
(4)V、Cr、Mn、W等高熔点金属_______________________________ 。
①热分解法 ②以活泼金属Na、Mg等还原 ③以C、CO或H2做还原剂
④电解法 ⑤利用铝热反应原理还原
请将下列金属所采用的最佳冶炼方法填写在相应空白处(填写序号,每项只填写一种方法)。
(1)Fe、Zn、Cu等中等活泼金属
(2)Na、Mg、Al等活泼或较活泼金属
(3)Hg、Ag等不活泼金属
(4)V、Cr、Mn、W等高熔点金属
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】钠及其化合物具有独特的性质和广泛的用途。
I.
(1)下图为钠与水反应的实验示意图。
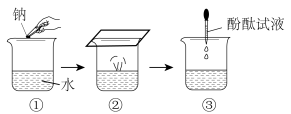
i.②中现象说明钠的密度比水___________ (“大”或“小”)。
ii.实验中观察到钠融成小球,下列能量变化示意图中能解释该现象的是___________ 。
a.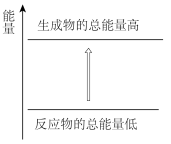 B.
B.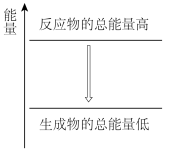
iii.③中加入酚酞试液后的现象是___________ 。
(2)用化学方程式表示由氯化钠制取金属钠的原理。___________
(3)将一定量的 通入
通入 溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入
溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入 盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
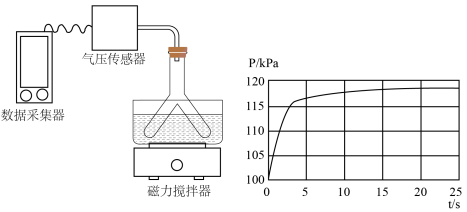
其中0~5s发生反应的离子方程式为___________ 。20s时溶液中的溶质是___________ (不考虑气体在水中的溶解)。
II.过碳酸钠( ),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:
),俗名固态双氧水,具有去污杀菌等功效。其制备原理为: (反应放热)
(反应放热)
(4)结合 和
和 的性质,推测制备过碳酸钠的原料中,
的性质,推测制备过碳酸钠的原料中, 与
与 的物质的量之比应
的物质的量之比应___________  。
。
A.大于 B.等于 C.小于
向 中加入
中加入 溶液的速度不能过快,原因是
溶液的速度不能过快,原因是___________ 。
(5)在过碳酸钠的生产过程中需要加入稳定剂,以得到稳定性好的过碳酸钠产品,保证其在一定贮存期内仍具有高活性的氧含量。以不同种类的稳定剂制备过碳酸钠产品,测得其活性氧质量分数随时间的变化如图所示:
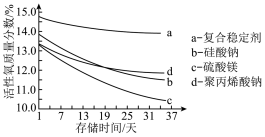
由图可知,制备过碳酸钠时应选择的稳定剂是___________ ,理由是___________ 。
A.a B.b C.c D.d
I.
(1)下图为钠与水反应的实验示意图。

i.②中现象说明钠的密度比水
ii.实验中观察到钠融成小球,下列能量变化示意图中能解释该现象的是
a.
 B.
B.
iii.③中加入酚酞试液后的现象是
(2)用化学方程式表示由氯化钠制取金属钠的原理。
(3)将一定量的
 通入
通入 溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入
溶液中。所得溶液转移至Y形管的一侧,并放入小磁子;向Y形管另一侧支管中加入 盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
盐酸,Y形管上端连接压强传感器。将Y形管倾斜,使两支管中的溶液混合,启动磁力搅拌器,采集压强数据。当数据变化平缓时,停止采集数据,得到如图所示的实验结果:
其中0~5s发生反应的离子方程式为
II.过碳酸钠(
 ),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:
),俗名固态双氧水,具有去污杀菌等功效。其制备原理为: (反应放热)
(反应放热)(4)结合
 和
和 的性质,推测制备过碳酸钠的原料中,
的性质,推测制备过碳酸钠的原料中, 与
与 的物质的量之比应
的物质的量之比应 。
。A.大于 B.等于 C.小于
向
 中加入
中加入 溶液的速度不能过快,原因是
溶液的速度不能过快,原因是(5)在过碳酸钠的生产过程中需要加入稳定剂,以得到稳定性好的过碳酸钠产品,保证其在一定贮存期内仍具有高活性的氧含量。以不同种类的稳定剂制备过碳酸钠产品,测得其活性氧质量分数随时间的变化如图所示:

由图可知,制备过碳酸钠时应选择的稳定剂是
A.a B.b C.c D.d
您最近一年使用:0次



