填空
(1)下列物质中:①铜②融化态NaCl③ 固体;④盐酸⑤
固体;④盐酸⑤ 。其中属于电解质的是
。其中属于电解质的是___________ (填写代号),能导电的是___________ (填写代号)。
(2) 溶于水电离方程式是
溶于水电离方程式是___________ 。
(3)某工业废水中含有 、
、 、
、 ,要求加入三种试剂,每次只沉淀一种离子,写出加入第一种试剂时,所发生反应的离子方程式
,要求加入三种试剂,每次只沉淀一种离子,写出加入第一种试剂时,所发生反应的离子方程式___________ ;
(4)某化学兴趣小组通过实验对硫酸的化学性质进行了验证和总结,如图4所示“——”表示物质两两之间能发生化学反应,请据图回答问题。

请补充一个实验,完善硫酸的化学性质,X可以是___________ (用化学式表示);发生中和反应的化学方程式为___________ 。
(1)下列物质中:①铜②融化态NaCl③
 固体;④盐酸⑤
固体;④盐酸⑤ 。其中属于电解质的是
。其中属于电解质的是(2)
 溶于水电离方程式是
溶于水电离方程式是(3)某工业废水中含有
 、
、 、
、 ,要求加入三种试剂,每次只沉淀一种离子,写出加入第一种试剂时,所发生反应的离子方程式
,要求加入三种试剂,每次只沉淀一种离子,写出加入第一种试剂时,所发生反应的离子方程式(4)某化学兴趣小组通过实验对硫酸的化学性质进行了验证和总结,如图4所示“——”表示物质两两之间能发生化学反应,请据图回答问题。

请补充一个实验,完善硫酸的化学性质,X可以是
更新时间:2023-08-03 18:37:18
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】甘肃马家窑遗址出土的青铜刀,是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,其化学式为Cu2(OH)2CO3,“铜绿”能跟酸反应生成铜盐、CO2和H2O。
(1)CO2属于____ 氧化物。(填“酸性”或“碱性”)
(2)从物质分类标准看,“铜绿”属于哪类物质____ (填选项)。
(3)铜器表面有时会生成“铜绿”,这层“铜绿”可用化学方法除去,写出盐酸去除“铜绿”的化学方程式:____ 。
(4)古代人们高温灼烧孔雀石[Cu(OH)2•CuCO3]和木炭的混合物得到一种紫红色的金属铜,其化学反应方程式为2CuO+C 2Cu+CO2↑,该反应属于
2Cu+CO2↑,该反应属于____ 。
(5)现代工业以黄铜矿为原料,在炼铜的过程中发生了多个反应,其中有如下两个反应:
反应Ⅰ:2Cu2S+3O2 2Cu2O+2SO2,反应Ⅱ:Cu2S+2Cu2O
2Cu2O+2SO2,反应Ⅱ:Cu2S+2Cu2O 6Cu+SO2↑
6Cu+SO2↑
请回答下列问题:
①反应Ⅰ中,氧化产物是____ ,用双线桥标出反应Ⅰ中电子转移的方向和数目____ 。
②反应Ⅱ中,Cu2O的作用是____ 。(填“氧化剂”“还原剂”或“氧化剂和还原剂”)
(1)CO2属于
(2)从物质分类标准看,“铜绿”属于哪类物质
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(4)古代人们高温灼烧孔雀石[Cu(OH)2•CuCO3]和木炭的混合物得到一种紫红色的金属铜,其化学反应方程式为2CuO+C
 2Cu+CO2↑,该反应属于
2Cu+CO2↑,该反应属于| A.置换反应 | B.复分解反应 | C.氧化还原反应 | D.离子反应 |
反应Ⅰ:2Cu2S+3O2
 2Cu2O+2SO2,反应Ⅱ:Cu2S+2Cu2O
2Cu2O+2SO2,反应Ⅱ:Cu2S+2Cu2O 6Cu+SO2↑
6Cu+SO2↑请回答下列问题:
①反应Ⅰ中,氧化产物是
②反应Ⅱ中,Cu2O的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】阅读下列科普短文并填空。
氢氧燃料电池是一种化学电池,具有能量转化率高、对环境友好等优点。例如,该电池在工作时,从负极连续通入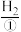 ,从正极连续通入
,从正极连续通入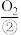 ,二者在电池内部(含有
,二者在电池内部(含有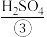 或
或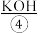 等物质的溶液)发生反应生成
等物质的溶液)发生反应生成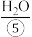 ,同时产生电能。除了H2,
,同时产生电能。除了H2,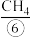 、
、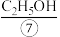 等也可以作为燃料电池的燃料。目前已研制成功
等也可以作为燃料电池的燃料。目前已研制成功 -
- 燃料电池,它可以代替汽油
燃料电池,它可以代替汽油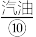 为汽车提供动力,也可以用作照明电源等。
为汽车提供动力,也可以用作照明电源等。
(1)在上述短文标有序号的物质中,属于混合物的是___________ (填序号下同);属于酸的是___________ ;属于有机物的是___________ ;属于碱的是___________ ;
(2)请写出与O2互为同素异形体的物质的化学式:___________ 。
(3)请写出下列反应的离子方程式:
a)③与④___________ 。
b)③与⑧___________ 。
(4)④与⑧的水溶液也能反应生成KAlO2和一种气体。写出该反应的化学方程式:___________
氢氧燃料电池是一种化学电池,具有能量转化率高、对环境友好等优点。例如,该电池在工作时,从负极连续通入
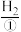 ,从正极连续通入
,从正极连续通入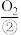 ,二者在电池内部(含有
,二者在电池内部(含有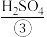 或
或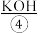 等物质的溶液)发生反应生成
等物质的溶液)发生反应生成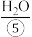 ,同时产生电能。除了H2,
,同时产生电能。除了H2,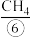 、
、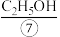 等也可以作为燃料电池的燃料。目前已研制成功
等也可以作为燃料电池的燃料。目前已研制成功 -
- 燃料电池,它可以代替汽油
燃料电池,它可以代替汽油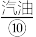 为汽车提供动力,也可以用作照明电源等。
为汽车提供动力,也可以用作照明电源等。(1)在上述短文标有序号的物质中,属于混合物的是
(2)请写出与O2互为同素异形体的物质的化学式:
(3)请写出下列反应的离子方程式:
a)③与④
b)③与⑧
(4)④与⑧的水溶液也能反应生成KAlO2和一种气体。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】关注物质的宏观组成和微观构成,是研究物质性质及其转化的基本出发点。
(1)从物质分类看, 均属于
均属于___________ (选填序号), 的电离方程式
的电离方程式___________ 。
A.氧化物 B.酸 C.碱 D.盐
(2)利用 制备为
制备为
资料i:
资料ii:氨气( )可与水发生反应,生成一水合氨(
)可与水发生反应,生成一水合氨( ),一水合氨属于一种碱。
),一水合氨属于一种碱。
①向饱和 溶液中通入足量
溶液中通入足量 ,无
,无 生成,原因是
生成,原因是___________ 。
②向饱和 溶液中先通入
溶液中先通入 ,再通入
,再通入 ,在溶液中可析出
,在溶液中可析出 晶体,该反应的化学方程式:
晶体,该反应的化学方程式:___________ ,通入 的作用是
的作用是___________ 。
(3)灼烧 制取
制取 化学方程式为
化学方程式为___________ 。若灼烧的时间较短,NaHCO3将分解不完全,现在取不完全灼烧后的59.2g样品分成两等份进行了以下探究。
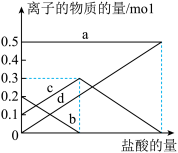
①将其中一份溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如图所示。则曲线c对应的溶液中的离子是___________ ;该样品中 和
和 的物质的量之比是
的物质的量之比是___________ 。
②标准状况下,将另一份样品与足量硫酸反应,放出的气体经过浓硫酸干燥后通入足量 中,能收集到
中,能收集到
___________ L。
(1)从物质分类看,
 均属于
均属于 的电离方程式
的电离方程式A.氧化物 B.酸 C.碱 D.盐
(2)利用
 制备为
制备为
资料i:
| 物质 |  |  |  |  |
20℃时的溶解度(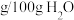 ) ) | 36.0 | 9.6 | 21.7 | 37.2 |
 )可与水发生反应,生成一水合氨(
)可与水发生反应,生成一水合氨( ),一水合氨属于一种碱。
),一水合氨属于一种碱。①向饱和
 溶液中通入足量
溶液中通入足量 ,无
,无 生成,原因是
生成,原因是②向饱和
 溶液中先通入
溶液中先通入 ,再通入
,再通入 ,在溶液中可析出
,在溶液中可析出 晶体,该反应的化学方程式:
晶体,该反应的化学方程式: 的作用是
的作用是(3)灼烧
 制取
制取 化学方程式为
化学方程式为①将其中一份溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如图所示。则曲线c对应的溶液中的离子是
 和
和 的物质的量之比是
的物质的量之比是
②标准状况下,将另一份样品与足量硫酸反应,放出的气体经过浓硫酸干燥后通入足量
 中,能收集到
中,能收集到
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下列物质中:①AlCl3溶液,②液氨,③液态CH3COOH,④铜,⑤NaHSO4固体,⑥蔗糖,⑦胆矾晶体,⑧SO2的水溶液,⑨无水乙醇,⑩熔融态的NaOH。
(1)能导电的是___________ (填序号);
(2)属于电解质的是:___________ (填序号);
(3)属于非电解质的是:___________ (填序号);
(4)属于强电解质的是:___________ (填序号);
(5)属于弱电解质的是:___________ (填序号);
(6)请分别写出上述物质中的③、⑤、⑦在水溶液中的电离方程式:___________ 、___________ 、___________ 。
(1)能导电的是
(2)属于电解质的是:
(3)属于非电解质的是:
(4)属于强电解质的是:
(5)属于弱电解质的是:
(6)请分别写出上述物质中的③、⑤、⑦在水溶液中的电离方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】有以下10种物质,请回答下列问题:
①干冰②氢氧化钡溶液③铜④稀硫酸⑤Na2SO4溶液⑥熔融碳酸氢钠固体⑦氢氧化钠固体⑧二氧化硫⑨氯化氢⑩NH3⑪Na2CO3
(1)其中能导电的是________ (填写符号,下同);属于电解质的是________ ;属于非电解质的是________ .
(2)写出物质⑪在水中的电离方程式:________________ .
(3)写出物质①和足量⑦在水中发生反应的离子方程式:________________ .
(4)写出②和⑤发生反应的离子方程式:________________ .
(5)写出物质④和⑦反应的离子方程式:________________ .
①干冰②氢氧化钡溶液③铜④稀硫酸⑤Na2SO4溶液⑥熔融碳酸氢钠固体⑦氢氧化钠固体⑧二氧化硫⑨氯化氢⑩NH3⑪Na2CO3
(1)其中能导电的是
(2)写出物质⑪在水中的电离方程式:
(3)写出物质①和足量⑦在水中发生反应的离子方程式:
(4)写出②和⑤发生反应的离子方程式:
(5)写出物质④和⑦反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】高铁酸钠( )是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为:
)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为: 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便,净水效果更好。请回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便,净水效果更好。请回答下列问题:
(1)高铁酸钠( )属于
)属于___________ (“酸”、“碱”、“盐”或“氧化物”),其中铁的化合价为___________ 价
(2)光束通过 胶体时,在垂直于光线的方向可以看到一条光亮的通路,这种现象称为
胶体时,在垂直于光线的方向可以看到一条光亮的通路,这种现象称为___________ , 胶体的胶粒具有
胶体的胶粒具有___________ 性,能使水中的悬浮颗粒物沉降,因而能够净水。
(3)该反应中有NaOH生成,NaOH属于___________ 。(填“电解质”或“非电解质”)
(4)当该反应生成48g 时,转移电子数目为
时,转移电子数目为___________ 。
 )是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为:
)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为: 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便,净水效果更好。请回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便,净水效果更好。请回答下列问题:(1)高铁酸钠(
 )属于
)属于(2)光束通过
 胶体时,在垂直于光线的方向可以看到一条光亮的通路,这种现象称为
胶体时,在垂直于光线的方向可以看到一条光亮的通路,这种现象称为 胶体的胶粒具有
胶体的胶粒具有(3)该反应中有NaOH生成,NaOH属于
(4)当该反应生成48g
 时,转移电子数目为
时,转移电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在图1所示的装置中,烧杯中盛放的是Ba(OH)2溶液,当从滴定管中逐滴加入某种溶液A时,溶液的导电性的变化趋势如图2所示。

(1)滴加液体至图2中曲线最低点时,灯泡可能熄灭,可能的原因是_______ 。
(2)试根据离子反应的特点分析,溶液A中含有的溶质可能是______ (填序号)。
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
(3)①写出NaHSO4在熔融状态下的电离方程式_______ 。
②NaHSO4属于______ 。(填“酸”“碱”或“盐”)。
(4)有以下物质:①石墨;②氯化氢气体;③酒精;④铝;⑤二氧化碳;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧液态醋酸;⑨氯化银固体;⑩氨气。其中能导电的是:_______ ;属于非电解质的是:______ 。(填序号)

(1)滴加液体至图2中曲线最低点时,灯泡可能熄灭,可能的原因是
(2)试根据离子反应的特点分析,溶液A中含有的溶质可能是
①HCl ②H2SO4 ③NaHSO4 ④NaHCO3
(3)①写出NaHSO4在熔融状态下的电离方程式
②NaHSO4属于
(4)有以下物质:①石墨;②氯化氢气体;③酒精;④铝;⑤二氧化碳;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧液态醋酸;⑨氯化银固体;⑩氨气。其中能导电的是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.现有下列七种物质:①胆矾 ②铝 ③Al2(SO4)3 ④干冰 ⑤稀硝酸 ⑥Ba(OH)2 ⑦N2O5 ⑧熔融的KNO3 ⑨NO
(1)以上物质属于电解质的是_______ ,以上物质能导电的是_______ 。
(2)上述物质中有两种易溶于水的物质之间可发生酸碱中和反应,该反应对应的化学方程式为_______ 。
(3)Al2(SO4)3 在水中的电离方程式为_______ ;
(4)写出向Ba(OH)2溶液中通入过量CO2反应的离子方程式_______ 。
Ⅱ.甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
铜 铜绿
铜绿 A
A Cu(OH)2
Cu(OH)2 B
B Cu
Cu
(5)从物质分类标准看,“铜绿”属于_______(填字母)。
(6)写出B的化学式:_______ 。
(7)请写出铜绿与盐酸反应的化学方程式:_______ 。
(1)以上物质属于电解质的是
(2)上述物质中有两种易溶于水的物质之间可发生酸碱中和反应,该反应对应的化学方程式为
(3)Al2(SO4)3 在水中的电离方程式为
(4)写出向Ba(OH)2溶液中通入过量CO2反应的离子方程式
Ⅱ.甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
铜
 铜绿
铜绿 A
A Cu(OH)2
Cu(OH)2 B
B Cu
Cu(5)从物质分类标准看,“铜绿”属于_______(填字母)。
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(7)请写出铜绿与盐酸反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有下列十种物质:①H2②铝 ③甲烷 ④CO2 ⑤H2SO4⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨盐酸 ⑩Al2(SO4)3
(1)上述物质中属于电解质的有:_____________________ 。(填序号)
(2)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-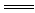 H2O,该反应的化学方程式为
H2O,该反应的化学方程式为_________________ 。
(3)⑩在水中的电离方程式为__________________ ,17.1g该物质溶于水配成250mL溶液,物质的量浓度为_______________ mol·L-1。
(4)⑨的浓溶液与二氧化锰发生反应的化学方程式为:4HCl(浓)+MnO2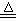 Cl2↑+MnCl2+2H2O,该反应的氧化剂是
Cl2↑+MnCl2+2H2O,该反应的氧化剂是___________ (填化学式),还原剂与氧化剂的物质的量之比是_________ 。写出该反应的离子方程式_____________________________ 。
(1)上述物质中属于电解质的有:
(2)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-
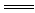 H2O,该反应的化学方程式为
H2O,该反应的化学方程式为(3)⑩在水中的电离方程式为
(4)⑨的浓溶液与二氧化锰发生反应的化学方程式为:4HCl(浓)+MnO2
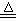 Cl2↑+MnCl2+2H2O,该反应的氧化剂是
Cl2↑+MnCl2+2H2O,该反应的氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有以下物质:ⅰ. 、ⅱ.酒精、ⅲ.
、ⅱ.酒精、ⅲ. 、ⅳ.
、ⅳ. 、ⅴ.
、ⅴ. 溶液、ⅵ.食醋、ⅶ.
溶液、ⅵ.食醋、ⅶ. 、ⅷ.
、ⅷ. 、ⅸ.烧碱溶液、ⅹ.液氯。
、ⅸ.烧碱溶液、ⅹ.液氯。
回答下列问题:
(1)以上物质属于电解质的有_______ (填编号,下同),能导电的有_______ 。
(2)写出物质ⅷ的电离方程式:________ 。
(3)物质ⅴ和物质ⅸ混合后发生反应的离子方程式为________ 。
(4)向 物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入
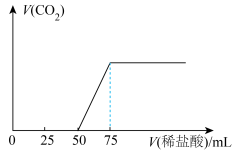
物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是
的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是_______ (填化学式),原 物质ix的浓度为
物质ix的浓度为______ 。
(5)物质ⅳ是一种新型净水剂。制取物质ⅳ时所发生的反应如下: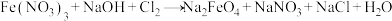
①配平上述反应的化学方程式并用“双线桥”表示电子转移情况:________ 。
②该反应中 是
是________ (填“氧化剂”“还原剂”“氧化产物”或“还原产物”)。
③生成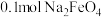 时,转移电子的数自为
时,转移电子的数自为____  (
( 表示阿伏加德罗常数的值),消耗
表示阿伏加德罗常数的值),消耗___ 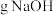 。
。
 、ⅱ.酒精、ⅲ.
、ⅱ.酒精、ⅲ. 、ⅳ.
、ⅳ. 、ⅴ.
、ⅴ. 溶液、ⅵ.食醋、ⅶ.
溶液、ⅵ.食醋、ⅶ. 、ⅷ.
、ⅷ. 、ⅸ.烧碱溶液、ⅹ.液氯。
、ⅸ.烧碱溶液、ⅹ.液氯。回答下列问题:
(1)以上物质属于电解质的有
(2)写出物质ⅷ的电离方程式:
(3)物质ⅴ和物质ⅸ混合后发生反应的离子方程式为
(4)向
 物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入
物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是
的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是 物质ix的浓度为
物质ix的浓度为
(5)物质ⅳ是一种新型净水剂。制取物质ⅳ时所发生的反应如下:
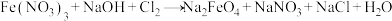
①配平上述反应的化学方程式并用“双线桥”表示电子转移情况:
②该反应中
 是
是③生成
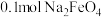 时,转移电子的数自为
时,转移电子的数自为 (
( 表示阿伏加德罗常数的值),消耗
表示阿伏加德罗常数的值),消耗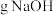 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具。如图是钠的价类二维图:
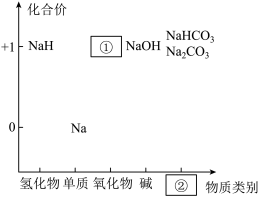
(1)②处应填的物质类别是___________ ;
(2)将钠放入水中发生反应的离子方程式是___________ ;
(3)Na可用石蜡封存,实验室少量Na保存于___________ 中;
(4)将Na2O2投入盛有CuSO4溶液的烧杯中,观察到的现象是___________(填标号);
(5)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应:
____ +____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
+____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
首先请补全方程式并配平__________ ,然后回答反应中被还原的元素是___________ ;反应中每消耗1molNa2O2的同时有___________ mol电子转移。

(1)②处应填的物质类别是
(2)将钠放入水中发生反应的离子方程式是
(3)Na可用石蜡封存,实验室少量Na保存于
(4)将Na2O2投入盛有CuSO4溶液的烧杯中,观察到的现象是___________(填标号);
| A.有气体生成 | B.无气体生成 | C.有蓝色沉淀生成 | D.大量红色固体铜生成 |
(5)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应:
____
 +____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)
+____Na2O2+______→ ______Mn2++______Na++_____+_____H2O(未配平)首先请补全方程式并配平
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就三大酸与金属反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解。该反应的化学方程式为:______________________ 。
(2)在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积________________ (填“大于”、“等于”或“小于”)180 mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为__________________ 。
(3) 欲迅速除去铝壶底部的水垢,又不损坏铝壶,最好的方法是( )
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解。该反应的化学方程式为:
(2)在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积
(3) 欲迅速除去铝壶底部的水垢,又不损坏铝壶,最好的方法是
| A.浓盐酸 | B.稀硝酸 | C.冷的浓硝酸 | D.冷的浓硫酸 |
您最近一年使用:0次



