X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W相邻;②X分别与Y、Z、W可组成化学式为YX3,X2Z和X2W三种共价化合物;③Y的最简氢化物可与其最高价含氧酸反应。
(1)X、Y、Z原子最外层电子数之和是_______ 。
(2)X2W的结构式是_______ ;W在元素周期表中的位置是_______ 。
(3)X、Y和Z组成的一种化合物是强酸,写出该酸的稀溶液与铜反应的离子方程式:_______ 。
(4)Y的最简氢化物与其最高价含氧酸反应产物为_________ (填化学式),写出检验其阳离子的办法________ 。
(5)由X、Z元素构成既有极性键又有非极性键的化合物的电子式是______ 。
(1)X、Y、Z原子最外层电子数之和是
(2)X2W的结构式是
(3)X、Y和Z组成的一种化合物是强酸,写出该酸的稀溶液与铜反应的离子方程式:
(4)Y的最简氢化物与其最高价含氧酸反应产物为
(5)由X、Z元素构成既有极性键又有非极性键的化合物的电子式是
更新时间:2023/09/08 19:32:11
|
【知识点】 根据原子结构进行元素种类推断解读
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E为短周期元素且它们的原子序数依次增大,A的核外电子总数与其周期数相同;其中D原子的L电子层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的L电子层中未成对电子数与D相同,但还有空轨道;D与E同族。请回答下列问题:
(1)A与B形成的共价化合物中既含有 键,又含
键,又含 键的化合物是
键的化合物是_____ (任写一种)。
(2)B的氢化物中空间结构为正四面体形的是_____ (填名称),键角为_____ ,中心原子的杂化方式为_____ 杂化。
(3)A与B形成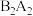 分子,其分子中
分子,其分子中 键和
键和 键的数目之比为
键的数目之比为_____ 。
(4)离子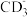 的中心原子的价层电子对数为
的中心原子的价层电子对数为_____ 。
(5)Te位于元素周期表第五周期第ⅥA族,其基态原子的价层电子轨道表示式为_____ ,其核外电子占据的最高能级的电子云轮廓图为_____ 。
(6)第一电子亲和能( )是指基态的气态原子得到一个电子形成气态
)是指基态的气态原子得到一个电子形成气态 价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则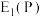
_____ (填“ ”或“
”或“ ”)
”)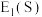 。
。
(7)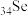 和
和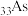 (与N同主族)两种元素中第一电离能较大的是
(与N同主族)两种元素中第一电离能较大的是_____ (填元素符号),试解释其原因:_____ 。
(8)根据对角线规则可知,Be与铝在性质上具有相似性。已知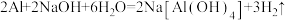 ,Be与
,Be与 溶液反应的化学方程式为
溶液反应的化学方程式为_____ 。
(1)A与B形成的共价化合物中既含有
 键,又含
键,又含 键的化合物是
键的化合物是(2)B的氢化物中空间结构为正四面体形的是
(3)A与B形成
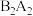 分子,其分子中
分子,其分子中 键和
键和 键的数目之比为
键的数目之比为(4)离子
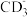 的中心原子的价层电子对数为
的中心原子的价层电子对数为(5)Te位于元素周期表第五周期第ⅥA族,其基态原子的价层电子轨道表示式为
(6)第一电子亲和能(
 )是指基态的气态原子得到一个电子形成气态
)是指基态的气态原子得到一个电子形成气态 价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则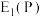
 ”或“
”或“ ”)
”)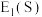 。
。(7)
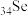 和
和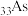 (与N同主族)两种元素中第一电离能较大的是
(与N同主族)两种元素中第一电离能较大的是(8)根据对角线规则可知,Be与铝在性质上具有相似性。已知
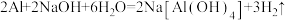 ,Be与
,Be与 溶液反应的化学方程式为
溶液反应的化学方程式为
您最近一年使用:0次
【推荐2】A、B、C、D、E、F、G是短周期元素,周期表中B与C相邻,C与E同主族;A中L层是K层的2倍,B的电子数比C的电子数少1个;F元素的原子在周期表中半径最小;常见化合物D2C2与水反应生成C的气体单质,且溶液使酚酞溶液变红。G是第三周期原子半径最小的主族元素。
(1)B在元素周期表中的位置_____ ;D的最高价氧化物的水化物的电子式____ ,用电子式表示FGC的形成过程为_______ ;
(2)B与F元素可形成18电子分子的电子式为_____ 。
(3)A、B、C的氢化物稳定性顺序为_______ (用分子式表示);G的阴离子的还原性_____ (大于或小于)E的阴离子。
(4)F2C和F2E中,沸点较高的是____ (填化学式),其主要原因是_____ 。
(5)锡(Sn)是古代五金之一,在第五周期第ⅣA,锡能和浓硫酸反应生成Sn(SO4)2和刺激性气味气体,反应的化学方程式为_______ 。
(1)B在元素周期表中的位置
(2)B与F元素可形成18电子分子的电子式为
(3)A、B、C的氢化物稳定性顺序为
(4)F2C和F2E中,沸点较高的是
(5)锡(Sn)是古代五金之一,在第五周期第ⅣA,锡能和浓硫酸反应生成Sn(SO4)2和刺激性气味气体,反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、M、N是五种短周期元素,原子序数依次增大。X原子中没有中子,Y元素最高正价与最低负价之和为0;M与X同主族;Z、N分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)Z、M、N三种元素对应离子半径由大到小的顺序是________ (离子符号表示)。
(2)X与Y组成的最简单化合物的电子式为__________ 。
(3)M的金属性比N强,出能证明该结论的一个事实________ 。
(1)Z、M、N三种元素对应离子半径由大到小的顺序是
(2)X与Y组成的最简单化合物的电子式为
(3)M的金属性比N强,出能证明该结论的一个事实
您最近一年使用:0次



