分类法是化学研究的重要方法。分子、原子、离子、电子等微观粒子,是化学最基本的研究对象,这些粒子的结合、重组,是构成物质及其变化的根本原因。
(1)在洗衣皂中掺入硅酸钠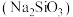 可缓冲洗衣皂的碱性,减少洗衣皂在水中的损耗。关于硅酸钠的分类错误的是___________。
可缓冲洗衣皂的碱性,减少洗衣皂在水中的损耗。关于硅酸钠的分类错误的是___________。
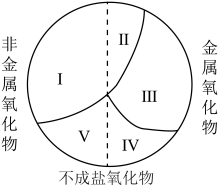
(2)下图是对氧化物的交叉分类示意图,虚线是金属氧化物和非金属氧化物的分界线。已知 在Ⅲ区,下列说法正确的是___________。
在Ⅲ区,下列说法正确的是___________。
(3)在化学变化过程中,原子中的下列粒子数可能发生改变的是___________。
(4)向某无色溶液中加入 溶液,产生白色沉淀,加入稀硝酸,沉淀不溶解,是否能证明该溶液中一定存在
溶液,产生白色沉淀,加入稀硝酸,沉淀不溶解,是否能证明该溶液中一定存在 。
。___________ (填“是”或“否”),理由是___________ 。
(1)在洗衣皂中掺入硅酸钠
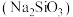 可缓冲洗衣皂的碱性,减少洗衣皂在水中的损耗。关于硅酸钠的分类错误的是___________。
可缓冲洗衣皂的碱性,减少洗衣皂在水中的损耗。关于硅酸钠的分类错误的是___________。| A.化合物 | B.酸 | C.钠盐 | D.硅酸盐 |
 在Ⅲ区,下列说法正确的是___________。
在Ⅲ区,下列说法正确的是___________。
A. 在II区 在II区 | B.碱性氧化物都在Ⅲ区 |
| C.酸性氧化物只包含Ⅰ区 | D.Ⅳ区、Ⅴ区的物质既不能跟酸反应,又不能跟碱反应 |
| A.质子数 | B.中子数 | C.质量数 | D.电子数 |
 溶液,产生白色沉淀,加入稀硝酸,沉淀不溶解,是否能证明该溶液中一定存在
溶液,产生白色沉淀,加入稀硝酸,沉淀不溶解,是否能证明该溶液中一定存在 。
。
更新时间:2023-10-16 21:43:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.离子反应是中学化学中重要的反应类型;离子方程式是用来表示离子反应的化学用语。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在_______(填标号)。
(2)从下列物质中选择合适反应物,按①③的要求,各写出一个符合条件的离子方程式。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、
①写出一个有气体生成的置换反应的离子反应方程式:_______ 。
②有难溶性碱生成的离子反应方程式:_______ 。
(3)某兴趣小组的同学向一定体积的 溶液中逐滴加入
溶液中逐滴加入 的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。
的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。

Ⅱ.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有 、
、 、
、 、
、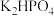 等。已知
等。已知 (次磷酸)与足量的
(次磷酸)与足量的 反应只生成一种盐
反应只生成一种盐 ,
, 水溶液中存在
水溶液中存在 分子。
分子。
(4) 属于
属于_______ 酸; 为
为_______ 盐(填序号)
①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(5)写出 溶液与足量
溶液与足量 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在_______(填标号)。
| A.单质 | B.化合物 | C.水 | D.电解质 |
(2)从下列物质中选择合适反应物,按①③的要求,各写出一个符合条件的离子方程式。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、
①写出一个有气体生成的置换反应的离子反应方程式:
②有难溶性碱生成的离子反应方程式:
(3)某兴趣小组的同学向一定体积的
 溶液中逐滴加入
溶液中逐滴加入 的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。
的稀溶液,通过仪器测得混合溶液的导电能力随时间变化的曲线如图所示。下列有关说法不正确的是_______。
| A.XY段混合溶液的导电能力逐渐减弱,说明生成的白色沉淀BaSO,不是电解质 |
| B.a时刻,两溶液恰好完全反应 |
C.YZ段的导电能力不断增大,主要是由于 溶液电离出的离子导电 溶液电离出的离子导电 |
D.向一定体积的 溶液中逐滴加入稀盐酸,测得溶液的导电能力-时间曲线图与该图保持一致 溶液中逐滴加入稀盐酸,测得溶液的导电能力-时间曲线图与该图保持一致 |
Ⅱ.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有
 、
、 、
、 、
、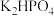 等。已知
等。已知 (次磷酸)与足量的
(次磷酸)与足量的 反应只生成一种盐
反应只生成一种盐 ,
, 水溶液中存在
水溶液中存在 分子。
分子。(4)
 属于
属于 为
为①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(5)写出
 溶液与足量
溶液与足量 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请回答下列问题:
(1)实验室制备Fe(OH)3胶体的具体操作为:向_______ 中滴加几滴饱和的FeCl3溶液,加热煮沸液体至呈_______ 色。该制备操作过程中所涉及反应的离子方程式为_______ 。不能通过向NaOH溶液中滴加饱和的FeCl3溶液制备Fe(OH)3胶体是因为胶体容易发生_______ 现象。为验证丁达尔效应,取一个小烧杯,向其中加入一定量制得的Fe(OH)3胶体并置于暗处,用一束红色激光照射烧杯中的Fe(OH)3胶体,会发现_______ 。
(2)互为同素异形体的物质均为_______ (选填“化合物”或“单质”)。请列举一组互为同素异形体的物质:_______ 。
(3)同学们吃的食品包装袋中有一个小纸袋上面写着“干燥剂”,主要成分是生石灰( )。
)。
①生石灰属于哪类氧化物:_______ 。
②生石灰可作干燥剂的理由是(用化学方程式表示)_______ 。
(4)已知Ca(OH)2、CaCO3、Ca(HCO3)2都是电解质。测定溶液导电能力的实验装置如图所示。现向澄清石灰水中持续通入CO2,灯泡亮度变化为_______。

(1)实验室制备Fe(OH)3胶体的具体操作为:向
(2)互为同素异形体的物质均为
(3)同学们吃的食品包装袋中有一个小纸袋上面写着“干燥剂”,主要成分是生石灰(
 )。
)。①生石灰属于哪类氧化物:
②生石灰可作干燥剂的理由是(用化学方程式表示)
(4)已知Ca(OH)2、CaCO3、Ca(HCO3)2都是电解质。测定溶液导电能力的实验装置如图所示。现向澄清石灰水中持续通入CO2,灯泡亮度变化为_______。

| A.变亮→熄灭→变暗 |
| B.变亮→不变→变亮 |
| C.变暗→熄灭→变亮 |
| D.变暗→不变→变暗 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】2022年1月,南太平洋岛国汤加境内发生了“21世纪至今最剧烈的火山喷发”,对该国造成了严重的破坏。火山喷发过程部分化学反应如下:
① ;
;
②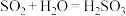 ;
;
③
(1)在上述方程式涉及的物质中,能与盐酸反应的氧化物有_______ (填化学式),属于酸的有_______ (填化学式)。
(2) 与
与 具有某些相似的化学性质,写出用NaOH溶液吸收
具有某些相似的化学性质,写出用NaOH溶液吸收 的化学方程式:
的化学方程式:_______ 。
(3) 是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。已知
是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。已知 称为正盐,
称为正盐, 称为酸式盐,写出
称为酸式盐,写出 的一种酸式盐的化学式:
的一种酸式盐的化学式:_______ 。
(4)互为同素异形体的物质均为_______ (选填“化合物”或“单质”)。请列举一组互为同素异形体的物质:_______ 。
①
 ;
;②
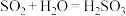 ;
;③

(1)在上述方程式涉及的物质中,能与盐酸反应的氧化物有
(2)
 与
与 具有某些相似的化学性质,写出用NaOH溶液吸收
具有某些相似的化学性质,写出用NaOH溶液吸收 的化学方程式:
的化学方程式:(3)
 是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。已知
是火山爆发过程中产生的酸性气体,属于二元弱酸,其饱和溶液的pH约为4。已知 称为正盐,
称为正盐, 称为酸式盐,写出
称为酸式盐,写出 的一种酸式盐的化学式:
的一种酸式盐的化学式:(4)互为同素异形体的物质均为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)回答以下问题:有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢,⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
其中属于电解质是_______ ;属于非电解质的是 _______ 。
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液 B 升华 C结晶 D过滤 E 蒸馏 F分液
①分离饱和食盐水与碳酸钙的混合物_______ ;
②从硝酸钾和氯化钠的混合液中获得硝酸钾_______ ;
③从溴水中提取溴单质_______ ;
④分离水和煤油的混合物_______ ;
⑤分离乙二醇(沸点为198°C)和丙三醇(沸点为290°C)的混合物_______ ;
(3)用CuSO4 ·5H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗涤干净的实验操作和现象是_______ 。
(4)A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种。现利用另一种溶液X,用如图所示的方法,即可将它们一一确定。 试确定A、B、C、D、X各代表何种溶液。
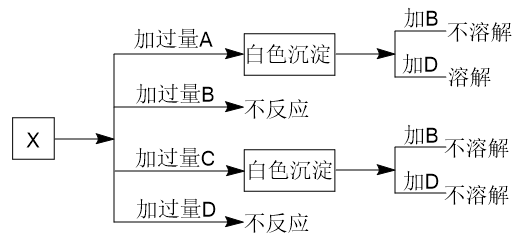
A:_______ B:_______ C:_______ D:_______ X:_______
(1)回答以下问题:有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢,⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
其中属于电解质是
(2)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液 B 升华 C结晶 D过滤 E 蒸馏 F分液
①分离饱和食盐水与碳酸钙的混合物
②从硝酸钾和氯化钠的混合液中获得硝酸钾
③从溴水中提取溴单质
④分离水和煤油的混合物
⑤分离乙二醇(沸点为198°C)和丙三醇(沸点为290°C)的混合物
(3)用CuSO4 ·5H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗涤干净的实验操作和现象是
(4)A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种。现利用另一种溶液X,用如图所示的方法,即可将它们一一确定。 试确定A、B、C、D、X各代表何种溶液。

A:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某溶液中可能有下列阴离子中的一种或几种: 、
、 、
、 、
、 。我校化学学习兴趣小组为确定其成分,取abcd四支试管各加入1mL待测液,进行如下操作:
。我校化学学习兴趣小组为确定其成分,取abcd四支试管各加入1mL待测液,进行如下操作:
(1)向a试管中滴加少量稀盐酸溶液无明显现象,写出发生反应的离子方程式:___________ ;继续滴加稀盐酸有气泡产生,写出发生反应的离子方程式:___________ 。
(2)向b试管中滴加硝酸酸化的 溶液后,溶液变浑浊,写出发生反应的离子方程式:
溶液后,溶液变浑浊,写出发生反应的离子方程式:___________ 。
(3)向c试管中滴加盐酸酸化的 溶液后,无明显现象,说明待测液中无
溶液后,无明显现象,说明待测液中无___________ (填离子符号)。
(4)蘸取d试管中的待测液做焰色实验,透过蓝色钴玻璃观察到火焰呈紫色;通过上述4组实验,说明该溶液是___________ (填化学式)。
 、
、 、
、 、
、 。我校化学学习兴趣小组为确定其成分,取abcd四支试管各加入1mL待测液,进行如下操作:
。我校化学学习兴趣小组为确定其成分,取abcd四支试管各加入1mL待测液,进行如下操作:(1)向a试管中滴加少量稀盐酸溶液无明显现象,写出发生反应的离子方程式:
(2)向b试管中滴加硝酸酸化的
 溶液后,溶液变浑浊,写出发生反应的离子方程式:
溶液后,溶液变浑浊,写出发生反应的离子方程式:(3)向c试管中滴加盐酸酸化的
 溶液后,无明显现象,说明待测液中无
溶液后,无明显现象,说明待测液中无(4)蘸取d试管中的待测液做焰色实验,透过蓝色钴玻璃观察到火焰呈紫色;通过上述4组实验,说明该溶液是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】硫和氮及其化合物在生产生活中应用广泛,含氮氧化物和硫氧化物的尾气需处理后才能排放。请回答下列问题:
(1)下列装置可用于实验室吸收尾气中SO2的是___________ (填标号)。
A、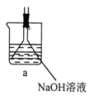 B、
B、 C、
C、 D、
D、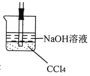
(2)某同学将干燥的二氧化硫气体通入品红与无水乙醇的混合液中,品红溶液不褪色;据此实验推断,使品红试液褪色的粒子可能有___________ 种。
(3)实验室有一瓶放置很久的Na2SO3固体药品,小明同学想设计一个实验验证这瓶药品是否变质?请你帮助他设计一个实验___________ 。
(4)用 Cu与HNO3和H2SO4的混合酸反应制备CuSO4,则参加反应的HNO3和H2SO4的物质的量之比为__________
(5)利用氨水可以将SO2和NO2吸收,原理如下图所示:

NO2被吸收的离子方程式是___________ 。
(6)在酸性NaClO溶液中,HClO氧化NO生成Cl−和NO 。其他条件相同,NO转化为NO
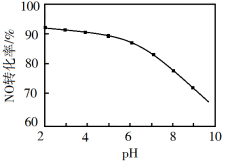
。其他条件相同,NO转化为NO 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。NaClO溶液的初始pH越小,NO转化率越高。其原因是
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。NaClO溶液的初始pH越小,NO转化率越高。其原因是___________ 。
(1)下列装置可用于实验室吸收尾气中SO2的是
A、
 B、
B、 C、
C、 D、
D、
(2)某同学将干燥的二氧化硫气体通入品红与无水乙醇的混合液中,品红溶液不褪色;据此实验推断,使品红试液褪色的粒子可能有
(3)实验室有一瓶放置很久的Na2SO3固体药品,小明同学想设计一个实验验证这瓶药品是否变质?请你帮助他设计一个实验
(4)用 Cu与HNO3和H2SO4的混合酸反应制备CuSO4,则参加反应的HNO3和H2SO4的物质的量之比为
(5)利用氨水可以将SO2和NO2吸收,原理如下图所示:

NO2被吸收的离子方程式是
(6)在酸性NaClO溶液中,HClO氧化NO生成Cl−和NO
 。其他条件相同,NO转化为NO
。其他条件相同,NO转化为NO 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。NaClO溶液的初始pH越小,NO转化率越高。其原因是
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。NaClO溶液的初始pH越小,NO转化率越高。其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我国展开“嫦娥探月”工程,向月球发起探索。2020年嫦娥五号一次带回1700多克月壤样本。研究表明,月球上有丰富的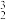 He资源,可开发用作未来的新型能源。
He资源,可开发用作未来的新型能源。
(1)α粒子是带有2个单位正电荷、质量数为4的氦离子,由此推断一个α粒子含有_____ 个电子,它的结构示意图为______ 。
(2)利用核聚变发电,3He是最安全的最清洁的能源,下列说法正确的是______ 。
(3)同温同压下,下列关于氦气和氧气的叙述中,正确的是______ 。
①氦气和氧气所含的分子数相同
②氦分子间的平均距离和氧分子间的平均距离几乎是相等的
③氦分子与氧分子的大小几乎相同
④氦分子和氧分子本身大小对于气体体积影响可以忽略不计
⑤氦气与氧气的密度之比等于32:4
(4)16克氧气含有n个O2分子,则阿伏加德罗常数可表示为______ 。
(5)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,该混合气体的平均分子量为______ ,其中氧气和氦气的分子数之比是_____ 。
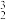 He资源,可开发用作未来的新型能源。
He资源,可开发用作未来的新型能源。(1)α粒子是带有2个单位正电荷、质量数为4的氦离子,由此推断一个α粒子含有
(2)利用核聚变发电,3He是最安全的最清洁的能源,下列说法正确的是
| A.3He、4He的化学性质基本相同 | B.3He、4He具有相同的电子数 |
| C.3He核聚变是化学变化 | D.3He液化是化学变化 |
①氦气和氧气所含的分子数相同
②氦分子间的平均距离和氧分子间的平均距离几乎是相等的
③氦分子与氧分子的大小几乎相同
④氦分子和氧分子本身大小对于气体体积影响可以忽略不计
⑤氦气与氧气的密度之比等于32:4
| A.①② | B.②④ | C.③⑤ | D.②③ |
| A.2n | B. n n | C.16n | D. n n |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】水是生命之源,在化学实验和科学研究中,水也是一种常用的试剂。
(1)写出与H2O分子电子数相等的微粒____________ (阴阳离子及分子各写一个)。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是__ 。
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
(3)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配离子,请写出生成此配离子的离子方程式_____________________ 。
(1)写出与H2O分子电子数相等的微粒
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
(3)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配位数是4的配离子,请写出生成此配离子的离子方程式
您最近一年使用:0次

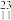 Na+ 中的质子数是
Na+ 中的质子数是

