(1)微粒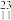 Na+ 中的质子数是
Na+ 中的质子数是_______ ,中子数是_______ ,核外电子数是_______ 。
(2)用电子式表示下列化合物的形成过程
H2S____________ ;
MgF2____________ 。
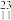 Na+ 中的质子数是
Na+ 中的质子数是(2)用电子式表示下列化合物的形成过程
H2S
MgF2
更新时间:2019-09-18 14:37:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】填写下表:
| 符号 | 质子数 | 中子数 | 质量数 | 电子数 | 结构示意图 |
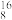 O O | |||||
| 13 | 14 | 13 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Na、Fe、Al是中学化学常见的金属元素。回答下列问题:
(1)焰色反应的实验中,Na元素燃烧时的焰色为_______ 色,观察K元素燃烧时的焰色需要透过_______ 。
(2)碘元素的一种核素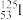 可用于治疗肿瘤。该核素的质子数为
可用于治疗肿瘤。该核素的质子数为_______ ,中子数为_______ ,质量数为_______ ,核外电子数为_______ 。(对应数值125和53)
(1)焰色反应的实验中,Na元素燃烧时的焰色为
(2)碘元素的一种核素
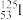 可用于治疗肿瘤。该核素的质子数为
可用于治疗肿瘤。该核素的质子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学键与化学反应有着密不可分的关系.根据相关知识填空,
(1)有下列几种物质①N2②NH3③KOH④He⑤CuSO4⑥NH4Cl⑦HNO3⑧MgF2。这些物质中,只含共价键的是___ (填序号,下向);既含共价键又含离子键的是__ ;属于共价化合物的是__ 。
(2)已加2mol氢气完全燃烧生成水蒸气时放出能量484kJ,且氧气中1molO=O键完全断裂时吸收能量496KJ,水蒸气中1molH—O键形成时放出能量463kJ,则氢气中1molH—H键断裂时吸收能量______ kJ。
(1)有下列几种物质①N2②NH3③KOH④He⑤CuSO4⑥NH4Cl⑦HNO3⑧MgF2。这些物质中,只含共价键的是
(2)已加2mol氢气完全燃烧生成水蒸气时放出能量484kJ,且氧气中1molO=O键完全断裂时吸收能量496KJ,水蒸气中1molH—O键形成时放出能量463kJ,则氢气中1molH—H键断裂时吸收能量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】对于HCl、H2SO4、NaOH、NaCl、NH4Cl、Ne、N2、金刚石,回答下列问题:
(1)不存在化学键的是______ .
(2)属于共价化合物的是_________ .
(3)属于离子化合物的是____________ .
(4)既含离子键,又含共价键的是_____ .
(1)不存在化学键的是
(2)属于共价化合物的是
(3)属于离子化合物的是
(4)既含离子键,又含共价键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)H、D、T三种原子,在标准状况下,它们的单质的密度之比是_______ ,它们与氧的同位素16O、18O相互结合为水,可得水分子的种数为_______ ;[14NH3T]+ 中,电子数、质子数、中子数之比为______
(2)含6.02×1023个中子的73Li的质量是_________ g;核内中子数为N的R2+,质量数为A,则n g它的同价态氧化物中所含电子的物质的量为_______________ 。
(3)①Ne ②HCl ③P4 ④N2H4 ⑤Mg3N2 ⑥Ca(OH)2 ⑦CaC2 ⑧NH4I ⑨AlCl3,请用上述物质的序号填空:
只存在极性共价键的是____________ ,只存在非极性共价键的是_______________ 。既存在离子键又存在非极性共价键的是_______________________ 。
(4)在下列变化中,①碘的升华 ②烧碱熔化 ③MgCl2溶于水 ④HCl溶于水 ⑤Na2O2溶于水,未发生化学键破坏的是_____________ ,仅发生离子键破坏的是_____________ (填写序号)
(2)含6.02×1023个中子的73Li的质量是
(3)①Ne ②HCl ③P4 ④N2H4 ⑤Mg3N2 ⑥Ca(OH)2 ⑦CaC2 ⑧NH4I ⑨AlCl3,请用上述物质的序号填空:
只存在极性共价键的是
(4)在下列变化中,①碘的升华 ②烧碱熔化 ③MgCl2溶于水 ④HCl溶于水 ⑤Na2O2溶于水,未发生化学键破坏的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我国航天航空事业蒸蒸日上,航天航空的关键技术是火箭,火箭燃料有液氢、乙炔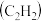 、甲烷、煤油、肼
、甲烷、煤油、肼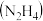 等。请回答下列问题:
等。请回答下列问题:
(1)已知肼的结构简式可表示为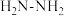 。
。
①肼分子中的化学键类型为_______________________ 。
②肼在氧气中燃烧生成无毒的物质,则反应中肼断裂的化学键有N—H键、_______________________ ,新形成的化学键有_______________________ 。
③根据肼燃烧过程中的能量变化,说明反应物能量之和_______________________ (填“大于”“等于”或“小于”)生成物能量之和。
(2)氢燃料汽车中氢的燃烧与火箭中氢的燃烧最大的不同在于前者使用的是空气作氧化剂,而后者使用的是液氧。火箭中不能使用液化空气,原因是_______________________ 。
(3)火箭发射前,当液氢、液氧加到一定量后,技术人员还要不停地补加,请你说出这种做法的原因_______________________ 。
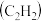 、甲烷、煤油、肼
、甲烷、煤油、肼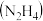 等。请回答下列问题:
等。请回答下列问题:(1)已知肼的结构简式可表示为
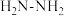 。
。①肼分子中的化学键类型为
②肼在氧气中燃烧生成无毒的物质,则反应中肼断裂的化学键有N—H键、
③根据肼燃烧过程中的能量变化,说明反应物能量之和
(2)氢燃料汽车中氢的燃烧与火箭中氢的燃烧最大的不同在于前者使用的是空气作氧化剂,而后者使用的是液氧。火箭中不能使用液化空气,原因是
(3)火箭发射前,当液氢、液氧加到一定量后,技术人员还要不停地补加,请你说出这种做法的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列物质:
①Cl2 ②Na2O2 ③NaOH ④HCl
⑤H2O2 ⑥Na2O ⑦NH4Cl ⑧CO2
(1)只由离子键构成的物质是________________ (填序号,下同)
(2)只由极性键构成的物质是______
(3)只由非极性键构成的物质_______________
(4)由极性键和非极性键构成的物质是_____________
(5)由离子键和极性键构成的物质是___________
(6)由离子键和非极性键构成的物质是______________
(7)属于离子化合物的是___________________
(8)属于共价化合物的是__________________
①Cl2 ②Na2O2 ③NaOH ④HCl
⑤H2O2 ⑥Na2O ⑦NH4Cl ⑧CO2
(1)只由离子键构成的物质是
(2)只由极性键构成的物质是
(3)只由非极性键构成的物质
(4)由极性键和非极性键构成的物质是
(5)由离子键和极性键构成的物质是
(6)由离子键和非极性键构成的物质是
(7)属于离子化合物的是
(8)属于共价化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知H2O2分子的结构如图所示: H2O2分子不是直线型的,两个H原子犹如在半展开的书的两面线上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,试回答:
H2O2分子不是直线型的,两个H原子犹如在半展开的书的两面线上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,试回答:
(1)写出H2O2分子的电子式________ ,其结构式为________ 。
(2)从极性键、非极性键角度写出分子内的化学键类型________ 。
(3)估计它难溶于CS2,简要说明原因______________________________________ 。
(4)指出氧元素的化合价,简要说明原因________________________________ 。
 H2O2分子不是直线型的,两个H原子犹如在半展开的书的两面线上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,试回答:
H2O2分子不是直线型的,两个H原子犹如在半展开的书的两面线上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,试回答:(1)写出H2O2分子的电子式
(2)从极性键、非极性键角度写出分子内的化学键类型
(3)估计它难溶于CS2,简要说明原因
(4)指出氧元素的化合价,简要说明原因
您最近一年使用:0次

 、
、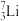 、
、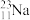 、
、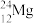 、
、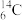 、
、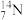 中:
中:

