雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 等离子。某同学收集雾霾样品,经必要的预处理配成无色试样溶液,设计如下实验探究其中含有的离子。
等离子。某同学收集雾霾样品,经必要的预处理配成无色试样溶液,设计如下实验探究其中含有的离子。
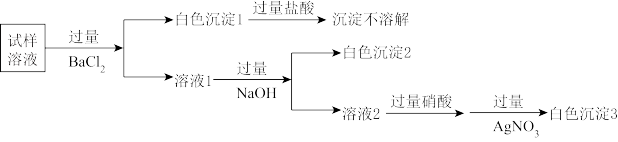
回答下列问题:
(1)不需要经过实验就可判断试样溶液中没有 ,理由是
,理由是___________ ;白色沉淀1的化学式是___________ 。
(2)生成白色沉淀2的离子方程式是___________ 。
(3)试样溶液中一定存在的离子是___________ (填写离子符号,下同),可能含有的离子是___________ 。一定没有的离子除了 外,还有
外,还有___________ 。
(4)检验试样溶液中可能含有的阴离子的方法是___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 等离子。某同学收集雾霾样品,经必要的预处理配成无色试样溶液,设计如下实验探究其中含有的离子。
等离子。某同学收集雾霾样品,经必要的预处理配成无色试样溶液,设计如下实验探究其中含有的离子。
回答下列问题:
(1)不需要经过实验就可判断试样溶液中没有
 ,理由是
,理由是(2)生成白色沉淀2的离子方程式是
(3)试样溶液中一定存在的离子是
 外,还有
外,还有(4)检验试样溶液中可能含有的阴离子的方法是
更新时间:2023-10-22 17:41:26
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】A、B、C、D四种可溶性盐,其阳离子分别是Na+、Ba2+、Fe3+、Ag+中的某一种,阴离子分别是Cl-、 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断这四种盐的化学式分别为:A:___________ ;B:___________ ;C:___________ ;D:___________ 。
(2)写出下列反应的离子方程式:
①A+D→:___________ ;
②C+HCl→气体:________ 。
(3)已知Fe3+与 在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式
在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式______ ,当某溶液X中存在 时,X中不可能大量存在的离子有
时,X中不可能大量存在的离子有______ (选填序号)。
A. B.
B. C.H+ D.Fe3+
C.H+ D.Fe3+
 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。(1)根据上述实验事实,推断这四种盐的化学式分别为:A:
(2)写出下列反应的离子方程式:
①A+D→:
②C+HCl→气体:
(3)已知Fe3+与
 在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式
在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式 时,X中不可能大量存在的离子有
时,X中不可能大量存在的离子有A.
 B.
B. C.H+ D.Fe3+
C.H+ D.Fe3+
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】一澄清溶液中可能含有的离子如表所示,为测定其含有的离子的种类,取该溶液进行实验:
实验①:用pH试纸检验,测得溶液呈强酸性。
实验②:取2 mL原溶液于试管中,加入少量CCl4及数滴新制氯水,经振荡,CCl4层呈紫红色。
实验③:取2 mL原溶液,逐渐向其中加入NaOH溶液,使溶液从酸性逐渐变为碱性,滴加过程中和滴加完毕后,均无沉淀产生。
实验④:另取部分上述实验③中的碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。
已知:Br2、I2易溶于CCl4,且Br2的CCl4溶液呈橙红色,I2的CCl4溶液呈紫红色。
根据所学知识,回答下列问题:
(1)根据实验①,可排除___________ 的存在。(填离子符号,下同)
(2)根据实验②,可证明含有的离子为___________ ,写出氯水中的氯气与溶液中的离子反应的离子方程式___________ 。该反应中被还原的物质为___________ (填离子符号或化学式)。
(3)根据实验③,可确定肯定不含的离子为___________ 。
(4)根据实验④,可证明___________ 的存在,又排除___________ 的存在。
(5)综上所述,该溶液中上述离子尚不能确定是否存在的是___________ 。
| 阳离子 | K+ 、Mg2+ 、Ba2+ 、Al3+ 、H+ |
| 阴离子 | I- 、Br- 、CO 、SO 、SO 、OH- 、OH- |
实验②:取2 mL原溶液于试管中,加入少量CCl4及数滴新制氯水,经振荡,CCl4层呈紫红色。
实验③:取2 mL原溶液,逐渐向其中加入NaOH溶液,使溶液从酸性逐渐变为碱性,滴加过程中和滴加完毕后,均无沉淀产生。
实验④:另取部分上述实验③中的碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。
已知:Br2、I2易溶于CCl4,且Br2的CCl4溶液呈橙红色,I2的CCl4溶液呈紫红色。
根据所学知识,回答下列问题:
(1)根据实验①,可排除
(2)根据实验②,可证明含有的离子为
(3)根据实验③,可确定肯定不含的离子为
(4)根据实验④,可证明
(5)综上所述,该溶液中上述离子尚不能确定是否存在的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某无色透明溶液溶液中可能含有下列某些离子:K+、Mg2+、Fe3+、Ba2+、SO 、OH-、CO
、OH-、CO 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:
Ⅰ.取少量原溶液滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少量原溶液滴入BaCl2溶液,无白色沉淀产生。
Ⅲ.另取少量原溶液先滴加硝酸再加AgNO3溶液,产生白色沉淀。
Ⅳ.再取少许原溶液滴入少量H2SO4溶液,有白色沉淀产生。
(1)根据以上现象判断,原溶液中肯定不存在的离子是_______ ;肯定存在的离子是_______ ;可能存在的离子是_______ ,检验该离子的实验方案为_______
(2)写出实验Ⅲ和Ⅳ中可能发生反应的离子方程式:
Ⅲ._______ 。
Ⅳ._______ 。
 、OH-、CO
、OH-、CO 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:Ⅰ.取少量原溶液滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少量原溶液滴入BaCl2溶液,无白色沉淀产生。
Ⅲ.另取少量原溶液先滴加硝酸再加AgNO3溶液,产生白色沉淀。
Ⅳ.再取少许原溶液滴入少量H2SO4溶液,有白色沉淀产生。
(1)根据以上现象判断,原溶液中肯定不存在的离子是
(2)写出实验Ⅲ和Ⅳ中可能发生反应的离子方程式:
Ⅲ.
Ⅳ.
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】A、B、C、D四种可溶性盐,其阳离子分别是Na+、Ba2+、Fe3+、Ag+中的某一种,阴离子分别是Cl-、 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断这四种盐的化学式分别为:A:___________ ;B:___________ ;C:___________ ;D:___________ 。
(2)写出下列反应的离子方程式:
①A+D→:___________ ;
②C+HCl→气体:________ 。
(3)已知Fe3+与 在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式
在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式______ ,当某溶液X中存在 时,X中不可能大量存在的离子有
时,X中不可能大量存在的离子有______ (选填序号)。
A. B.
B. C.H+ D.Fe3+
C.H+ D.Fe3+
 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有B盐溶液具有颜色。②分别向4支试管中加入2mL稀盐酸,发现A盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。(1)根据上述实验事实,推断这四种盐的化学式分别为:A:
(2)写出下列反应的离子方程式:
①A+D→:
②C+HCl→气体:
(3)已知Fe3+与
 在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式
在溶液中“相遇”时,会有红蝎色沉淀生成并产生气泡,写出相应的离子方程式 时,X中不可能大量存在的离子有
时,X中不可能大量存在的离子有A.
 B.
B. C.H+ D.Fe3+
C.H+ D.Fe3+
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D四种可溶性盐,其阳离子分别是 、
、 、
、 、
、 中的某一种,阴离子分别是
中的某一种,阴离子分别是 、
、 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有A盐溶液呈蓝色。②分别向4支试管中加入2mL稀盐酸,发现B盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有A盐溶液呈蓝色。②分别向4支试管中加入2mL稀盐酸,发现B盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断这几种盐的化学式分别为:B_______ ;C_______ ;D_______ 。
(2)按要求写出下列反应的方程式:
①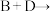
_______ 。(写离子方程式)
② 气体:
气体:_______ 。(写化学方程式)
 、
、 、
、 、
、 中的某一种,阴离子分别是
中的某一种,阴离子分别是 、
、 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有A盐溶液呈蓝色。②分别向4支试管中加入2mL稀盐酸,发现B盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有A盐溶液呈蓝色。②分别向4支试管中加入2mL稀盐酸,发现B盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。(1)根据上述实验事实,推断这几种盐的化学式分别为:B
(2)按要求写出下列反应的方程式:
①
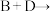
②
 气体:
气体:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】某固体X可能含有 、Cu2+、Na+、Cl-、
、Cu2+、Na+、Cl-、 、
、 中的几种离子,将固体X均分为两份,进行如下实验:
中的几种离子,将固体X均分为两份,进行如下实验:
A.一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得白色沉淀,过滤。在沉淀中加入足量稀盐酸,沉淀部分溶解,并产生无色无味气体。将滤液取出少许,加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
B.另一份固体与过量NaOH固体混合后充分加热,没有产生刺激性气味气体。
回答下列问题:
(1)该固体溶液中一定不存在的离子有_______ ,(不考虑溶液中少量的H+和OH-,下同),可能存在的离子有_______ ,一定存在的离子有_______ 。
(2)确定该溶液中存在阳离子的理论依据是_______ ,请你设计实验方案加以验证,具体操作和现象是_______ 。
 、Cu2+、Na+、Cl-、
、Cu2+、Na+、Cl-、 、
、 中的几种离子,将固体X均分为两份,进行如下实验:
中的几种离子,将固体X均分为两份,进行如下实验:A.一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得白色沉淀,过滤。在沉淀中加入足量稀盐酸,沉淀部分溶解,并产生无色无味气体。将滤液取出少许,加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
B.另一份固体与过量NaOH固体混合后充分加热,没有产生刺激性气味气体。
回答下列问题:
(1)该固体溶液中一定不存在的离子有
(2)确定该溶液中存在阳离子的理论依据是
您最近一年使用:0次
【推荐1】锂/磷酸氧铜电池是一种以磷酸氧铜作为正极材料的锂离子电池,其正极的活性物质是Cu4O(PO4)2,制备流程如下:
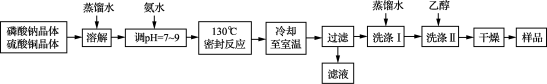
主要反应原理:2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)实验室进行“过滤”操作使用的玻璃仪器除烧杯外主要有____________ 。
(2)流程中“洗涤Ⅰ”后,检验沉淀已洗涤干净的方法是__________ 。

主要反应原理:2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)实验室进行“过滤”操作使用的玻璃仪器除烧杯外主要有
(2)流程中“洗涤Ⅰ”后,检验沉淀已洗涤干净的方法是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4、NH4HCO3的NaCl。某学生设计了如图所示方案提取纯净的NaCl溶液。(已知:NH4HCO3 NH3↑+CO2↑+H2O)
NH3↑+CO2↑+H2O)

如果此方案正确,那么:
(1)操作①可选择________ 仪器。
(2)操作②为什么不用硝酸钡溶液,其理由是___________________________ 。
(3)进行操作②后,如何判断 已除尽,方法是
已除尽,方法是_____________________ 。
(4)操作③的目的是_______________________________________________ ,为什么不先过滤后加碳酸钠溶液?理由是_________________________ 。
(5)操作④的目的是______________________________________________ 。
 NH3↑+CO2↑+H2O)
NH3↑+CO2↑+H2O)
如果此方案正确,那么:
(1)操作①可选择
(2)操作②为什么不用硝酸钡溶液,其理由是
(3)进行操作②后,如何判断
 已除尽,方法是
已除尽,方法是(4)操作③的目的是
(5)操作④的目的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】硫的化合物在生产、生活中应用广泛。
Ⅰ.某兴趣小组探究SO2气体还原Fe3+、I2。
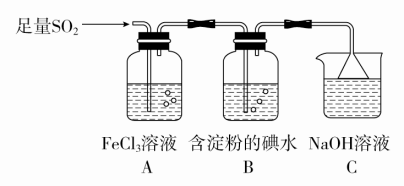
(1)通入足量SO2后,装置B中的现象是__________ ;装置C的作用是_________ 。
(2)该小组同学认为SO2与FeCl3溶液发生的是氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:________________ 。
②请设计实验方案验证有Fe2+生成:________________________ 。
Ⅱ.(3)铬是环境中的一种主要污染物,可以用焦亚硫酸钠(Na2S2O5)处理含铬酸性废水(含有 ),利用氧化还原反应,将六价铬还原为三价铬,
),利用氧化还原反应,将六价铬还原为三价铬,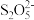 被氧化为
被氧化为 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为__________ 。
(4)已知: Na2S2O5溶于水会生成NaHSO3。检验Na2S2O5晶体在空气中已被氧化的实验方法是______ 。
Ⅰ.某兴趣小组探究SO2气体还原Fe3+、I2。

(1)通入足量SO2后,装置B中的现象是
(2)该小组同学认为SO2与FeCl3溶液发生的是氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:
②请设计实验方案验证有Fe2+生成:
Ⅱ.(3)铬是环境中的一种主要污染物,可以用焦亚硫酸钠(Na2S2O5)处理含铬酸性废水(含有
 ),利用氧化还原反应,将六价铬还原为三价铬,
),利用氧化还原反应,将六价铬还原为三价铬,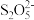 被氧化为
被氧化为 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为(4)已知: Na2S2O5溶于水会生成NaHSO3。检验Na2S2O5晶体在空气中已被氧化的实验方法是
您最近一年使用:0次



