回答下列问题。
(1)将金属钠投入FeCl3溶液中的离子方程式___________ 。
(2)请写出将 通入水中发生的离子反应方程式
通入水中发生的离子反应方程式___________ 。
(3)写出硫酸氢钠在熔融状态下的电离方程式___________ 。
(4)过氧化钠与水的反应中,其中水的作用是___________ (填“氧化剂”或“还原剂”或“既不是氧化剂也不是还原剂”)。
(5)84消毒液不能与洁厕灵大量混合使用的原因是___________ (书写离子方程式)。
(6)漂白粉的主要成分___________ 。(填化学式)
(1)将金属钠投入FeCl3溶液中的离子方程式
(2)请写出将
 通入水中发生的离子反应方程式
通入水中发生的离子反应方程式(3)写出硫酸氢钠在熔融状态下的电离方程式
(4)过氧化钠与水的反应中,其中水的作用是
(5)84消毒液不能与洁厕灵大量混合使用的原因是
(6)漂白粉的主要成分
更新时间:2023-10-03 16:44:12
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】阅读下列科普短文并填空:
海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如①NaCl、②MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和③食盐水用以生产④NaOH、⑤NaClO、⑥Cl2、⑦NaHCO3、⑧盐酸等,苦卤经过氯气氧化、热空气吹出、⑨SO2吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼⑩金属钠。海底埋藏大量可燃冰资源,⑪甲烷是一种清洁能源。
(1)标有序号的物质中属于分散系的是___________ (填序号,下同),属于电解质的是___________ 。
(2)⑩与水的化学反应属于四种基本反应类型中的___________ 。
(3)写出⑦溶于水的电离方程式:___________ ;④与⑦在水溶液中反应的离子方程式为:___________ ;将⑨通入足量④的溶液中,写出反应的离子方程式:___________ 。
(4)从海水提取溴的过程中涉及的反应有:2H2O+SO2+Br2 =4H++2Br-+SO ,2Br-+Cl2=Br2+2Cl-,根据上述反应可判断 Br-、Cl-、SO2的还原性由强到弱的顺序为
,2Br-+Cl2=Br2+2Cl-,根据上述反应可判断 Br-、Cl-、SO2的还原性由强到弱的顺序为___________ 。
海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如①NaCl、②MgSO4等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和③食盐水用以生产④NaOH、⑤NaClO、⑥Cl2、⑦NaHCO3、⑧盐酸等,苦卤经过氯气氧化、热空气吹出、⑨SO2吸收等一系列操作可获得Br2。电解熔融氯化钠可冶炼⑩金属钠。海底埋藏大量可燃冰资源,⑪甲烷是一种清洁能源。
(1)标有序号的物质中属于分散系的是
(2)⑩与水的化学反应属于四种基本反应类型中的
(3)写出⑦溶于水的电离方程式:
(4)从海水提取溴的过程中涉及的反应有:2H2O+SO2+Br2 =4H++2Br-+SO
 ,2Br-+Cl2=Br2+2Cl-,根据上述反应可判断 Br-、Cl-、SO2的还原性由强到弱的顺序为
,2Br-+Cl2=Br2+2Cl-,根据上述反应可判断 Br-、Cl-、SO2的还原性由强到弱的顺序为
您最近一年使用:0次
【推荐2】回答下列问题:
(1)请写出以下物质溶于水的电离方程式:
H2SO4_______
(NH4)2SO4_______
(2)71 g某一价金属的硫酸盐中,含有0.5 mol SO ,则该硫酸盐的摩尔质量为
,则该硫酸盐的摩尔质量为___________ ,该金属的相对原子质量为___________ 。
(1)请写出以下物质溶于水的电离方程式:
H2SO4
(NH4)2SO4
(2)71 g某一价金属的硫酸盐中,含有0.5 mol SO
 ,则该硫酸盐的摩尔质量为
,则该硫酸盐的摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下列几种物质:①NaHCO3晶体 ② Na2O2 ③ 盐酸 ④ CO2 ⑤ Ba(OH)2溶液 ⑥ C2H5OH(酒精)⑦KMnO4 ⑧ 氨水 ⑨饱和FeCl3溶液。根据要求回答下列问题:
(1)上述各物质属于电解质的是___________ (填物质编号,下同);属于非电解质的是___________ 。
(2)① 在水中的电离方程式为___________ ;⑦在水中的电离方程式为___________ 。
(3)写出少量④ 通入⑤ 中反应的离子方程式:___________ ;③和⑧在水溶液中反应的离子方程式:___________ 。
(4)将⑨加入到沸水中,继续加热溶液呈红褐色,即制得Fe(OH)3胶体,写出该反应的离子方程式:___________ 。
(1)上述各物质属于电解质的是
(2)① 在水中的电离方程式为
(3)写出少量④ 通入⑤ 中反应的离子方程式:
(4)将⑨加入到沸水中,继续加热溶液呈红褐色,即制得Fe(OH)3胶体,写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】 在常温下为黄色气体,熔点为-59.5℃,沸点为11℃,易溶于水,其水溶液是一种广谱杀菌剂,在碱性环境中易发生反应:
在常温下为黄色气体,熔点为-59.5℃,沸点为11℃,易溶于水,其水溶液是一种广谱杀菌剂,在碱性环境中易发生反应: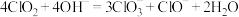 。
。 的制备方法有多种。回答下列问题:
的制备方法有多种。回答下列问题:
(1)一种制备 的反应为
的反应为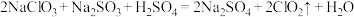 ,用单线桥法标明该反应中电子转移的方向和数目:
,用单线桥法标明该反应中电子转移的方向和数目:_______ 。
(2)一种有效成分为 、
、 、
、 的“二氧化氯泡腾片”溶于水时,逸出大量
的“二氧化氯泡腾片”溶于水时,逸出大量 ,同时
,同时 在酸性条件下发生自身氧化还原反应,得到
在酸性条件下发生自身氧化还原反应,得到 溶液。
溶液。
① 中Cl元素的化合价为
中Cl元素的化合价为_______ 。
②上述反应产生大量 的离子方程式为
的离子方程式为_______ 。
③上述反应生成 的离子方程式为
的离子方程式为_______ 。
(3)实验室可用如图所示装置制备 (夹持装置略)。
(夹持装置略)。

①装置A中发生反应的化学方程式为_______ 。
②装置B收集 时,为了收集更多的
时,为了收集更多的 ,可采取的措施为
,可采取的措施为_______ (填一条)。
(4) 的稳定性较差,易分解,常用
的稳定性较差,易分解,常用 和NaOH的混合溶液将其转化为
和NaOH的混合溶液将其转化为 进行保存,该反应的离子方程式为
进行保存,该反应的离子方程式为_______ ,若加入过量的NaOH可能导致的后果是_______ 。
 在常温下为黄色气体,熔点为-59.5℃,沸点为11℃,易溶于水,其水溶液是一种广谱杀菌剂,在碱性环境中易发生反应:
在常温下为黄色气体,熔点为-59.5℃,沸点为11℃,易溶于水,其水溶液是一种广谱杀菌剂,在碱性环境中易发生反应: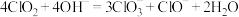 。
。 的制备方法有多种。回答下列问题:
的制备方法有多种。回答下列问题:(1)一种制备
 的反应为
的反应为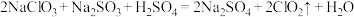 ,用单线桥法标明该反应中电子转移的方向和数目:
,用单线桥法标明该反应中电子转移的方向和数目:(2)一种有效成分为
 、
、 、
、 的“二氧化氯泡腾片”溶于水时,逸出大量
的“二氧化氯泡腾片”溶于水时,逸出大量 ,同时
,同时 在酸性条件下发生自身氧化还原反应,得到
在酸性条件下发生自身氧化还原反应,得到 溶液。
溶液。①
 中Cl元素的化合价为
中Cl元素的化合价为②上述反应产生大量
 的离子方程式为
的离子方程式为③上述反应生成
 的离子方程式为
的离子方程式为(3)实验室可用如图所示装置制备
 (夹持装置略)。
(夹持装置略)。
①装置A中发生反应的化学方程式为
②装置B收集
 时,为了收集更多的
时,为了收集更多的 ,可采取的措施为
,可采取的措施为(4)
 的稳定性较差,易分解,常用
的稳定性较差,易分解,常用 和NaOH的混合溶液将其转化为
和NaOH的混合溶液将其转化为 进行保存,该反应的离子方程式为
进行保存,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】生产生活中常用84消毒液杀菌消毒。化学课外小组用Cl2和NaOH溶液制取84消毒液。请回答下列问题:
(1)制取84消毒液需要 的NaOH溶液80mL,配制NaOH溶液时称量NaOH固体的质量为
的NaOH溶液80mL,配制NaOH溶液时称量NaOH固体的质量为_____ ,配制过程中使用的玻璃仪器有烧杯、玻璃棒、胶头滴管、_____ ;定容时俯视刻度线将导致所配溶液浓度_____ (填“偏高”、“偏低”或“不影响”)。
(2)制取84消毒液的离子方程式为_____ 。
(3)该消毒液也用于漂白,为增强漂白性向消毒液中滴加几滴稀盐酸,写出反应的化学方程式_____ 。
(4)已知酸性:H2CO3>HClO> ,向84消毒液中通入少量CO2的离子方程式为:
,向84消毒液中通入少量CO2的离子方程式为:_____ 。
(5)NaClO除了用于消毒外,在化工生产上常用作重要的氧化剂。比如,用NaClO和FeCl3溶液在NaOH的作用下制备一种新型水处理剂Na2FeO4,写出该反应的离子方程式:_____ 。
(1)制取84消毒液需要
 的NaOH溶液80mL,配制NaOH溶液时称量NaOH固体的质量为
的NaOH溶液80mL,配制NaOH溶液时称量NaOH固体的质量为(2)制取84消毒液的离子方程式为
(3)该消毒液也用于漂白,为增强漂白性向消毒液中滴加几滴稀盐酸,写出反应的化学方程式
(4)已知酸性:H2CO3>HClO>
 ,向84消毒液中通入少量CO2的离子方程式为:
,向84消毒液中通入少量CO2的离子方程式为:(5)NaClO除了用于消毒外,在化工生产上常用作重要的氧化剂。比如,用NaClO和FeCl3溶液在NaOH的作用下制备一种新型水处理剂Na2FeO4,写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】烟气中的SO2会给环境和人体健康带来极大的危害,工业上采取多种方法减少SO2的排放。
方法1(双碱法):用NaOH吸收SO2,并用CaO使NaOH再生,即:NaOH溶液 Na2SO3溶液。
Na2SO3溶液。
(1)过程①的离子方程式为_______ 。
(2)常温下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,吸收过程中水的电离平衡_______ (填“向左”“向右”或“不”)移动,该溶液中由水电离出的c(H+)=________ 。
(3)CaO在水中存在如下转化:CaO(s)+H2O(l)=Ca(OH)2(s),Ca(OH)2(s) Ca2+(aq)+2OH-(aq),从化学反应原理的角度解释过程②中NaOH再生的原理:
Ca2+(aq)+2OH-(aq),从化学反应原理的角度解释过程②中NaOH再生的原理:_______ 。
(4)理论上,该工艺中NaOH只作为启动碱,实际主要消耗的是生石灰。实际吸收过程中,由于存在一定氧气,会发生副反应,因副产物_______ (填名称)在工艺中较难循环再生成NaOH,需要不断向系统中补充NaOH。
方法2:用氨水除去。
(5)已知常温时,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.4×10-2、Ka1=6.0×10-8。则常温下2 mol/L氨水溶液的c(OH-)=_______ 。将SO2通入该氨水中,当溶液恰好呈中性时,溶液中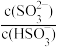 =
=_______ 。
方法1(双碱法):用NaOH吸收SO2,并用CaO使NaOH再生,即:NaOH溶液
 Na2SO3溶液。
Na2SO3溶液。(1)过程①的离子方程式为
(2)常温下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,吸收过程中水的电离平衡
(3)CaO在水中存在如下转化:CaO(s)+H2O(l)=Ca(OH)2(s),Ca(OH)2(s)
 Ca2+(aq)+2OH-(aq),从化学反应原理的角度解释过程②中NaOH再生的原理:
Ca2+(aq)+2OH-(aq),从化学反应原理的角度解释过程②中NaOH再生的原理:(4)理论上,该工艺中NaOH只作为启动碱,实际主要消耗的是生石灰。实际吸收过程中,由于存在一定氧气,会发生副反应,因副产物
方法2:用氨水除去。
(5)已知常温时,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.4×10-2、Ka1=6.0×10-8。则常温下2 mol/L氨水溶液的c(OH-)=
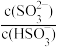 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列问题。
(1)氯气可直接用于自来水的消毒,氯气通入水中可用来杀菌消毒,其中杀菌消毒的物质是___________ (填化学式);用少量氯气消毒的自来水养金鱼时,通常需要先将自来水晒一晒,其原因是___________ (用化学方程式表示)。
(2)氯气可用来制取漂白粉,但干燥的氢氧化钙与氯气并不易发生反应,氯气只能被氢氧化钙所吸附。为此,在工业上采用加入少许水的消石灰来进行氯化,其原因是___________ ;漂白粉也能用于消毒,其有效成分生效的化学方程是___________ 。
(1)氯气可直接用于自来水的消毒,氯气通入水中可用来杀菌消毒,其中杀菌消毒的物质是
(2)氯气可用来制取漂白粉,但干燥的氢氧化钙与氯气并不易发生反应,氯气只能被氢氧化钙所吸附。为此,在工业上采用加入少许水的消石灰来进行氯化,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氯气极其相关产品在生产生活中应用广泛。
(1)氯气属于有毒气体,贮氯罐意外泄漏时,消防员会喷洒稀氢氧化钠溶液,其作用是__________ 。(用化学方程式表示)。
实验室常用NaOH溶液吸收多余的氯气,下列也可用于吸收氯气的是_________ (填字母)。
a.NaCl溶液 b.FeSO4溶液 c.KMnO4溶液
(2)家庭中常用消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)等清洁卫生。某品牌消毒液包装上的说明如下图。
①分析“对金属制品有腐蚀作用”的原因:_______________ 。
②需“密闭保存”的原因:______________ 。
③“与洁厕灵同时使用”会产生有毒的氯气,请写出反应的离子方程式_____________ 。
(3)已知空气中氯气含量超过0.1mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗0.001ml/L Kl溶液100mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是_______ 。
(1)氯气属于有毒气体,贮氯罐意外泄漏时,消防员会喷洒稀氢氧化钠溶液,其作用是
实验室常用NaOH溶液吸收多余的氯气,下列也可用于吸收氯气的是
a.NaCl溶液 b.FeSO4溶液 c.KMnO4溶液
(2)家庭中常用消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)等清洁卫生。某品牌消毒液包装上的说明如下图。

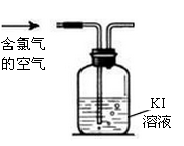
①分析“对金属制品有腐蚀作用”的原因:
②需“密闭保存”的原因:
③“与洁厕灵同时使用”会产生有毒的氯气,请写出反应的离子方程式
(3)已知空气中氯气含量超过0.1mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗0.001ml/L Kl溶液100mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)将硅酸盐Ca2Mg3Fe2(Si4O11)2(OH)2改写成氧化物的形式:________________________ 。
(2)用化学方程式表示生活中漂白粉的作用原理:__________________________________ 。
(3)选择合适的试剂除去下列各物质中的杂质(括号内为杂质),并写出相应方程式。
①CO2(HCl)____________ , 离子方程式: ________________________________ 。
②SiO2(CaO)___________ , 离子方程式:_________________________________ 。
③NO(NO2)____________ , 化学方程式:_________________________________ 。
(2)用化学方程式表示生活中漂白粉的作用原理:
(3)选择合适的试剂除去下列各物质中的杂质(括号内为杂质),并写出相应方程式。
①CO2(HCl)
②SiO2(CaO)
③NO(NO2)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】取黄豆粒大小的一块金属钠,用滤纸擦干其表面的煤油,然后加入CuSO4溶液中,观察实验现象并写出反应的化学方程式:
(1)钠与水反应的实验现象是___________ 。反应化学方程式是___________ 。
(2)加入CuSO4后,实验现象是____________ ,反应的化学方程式是_________ 。
(1)钠与水反应的实验现象是
(2)加入CuSO4后,实验现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将一小块钠投入CuSO4溶液中,观察到的现象是__ (填序号)。
①钠浮于液面上;②熔化成小球;③发出嘶嘶的响声,放出气体;④有蓝色沉淀产生;⑤析出大量红色的铜。
请写出Na和H2O反应的离子方程式__ ,NaHCO3俗称__ ,写出NaHCO3和HCl反应的离子方程式__ 。
①钠浮于液面上;②熔化成小球;③发出嘶嘶的响声,放出气体;④有蓝色沉淀产生;⑤析出大量红色的铜。
请写出Na和H2O反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学学习中要注重对过程的分析,按要求回答下列问题:
(1)向石蕊试液中通入氯气,观察到的现象是________________________ ,用化学方程式进行分析________________________________ ;若将氯水久置,将会有气泡冒出,用化学方程式进行分析_______________________________
(2)将一小块钠投入到盛FeCl3的溶液中,观察到的现象是__________________ ,用化学方程式进行分析________________________________ 。
(1)向石蕊试液中通入氯气,观察到的现象是
(2)将一小块钠投入到盛FeCl3的溶液中,观察到的现象是
您最近一年使用:0次



