自然界一共存在三种硅的稳定同位素,分别是28Si、29Si和30Si。
(1)Si原子的结构示意图为_______ 。
(2)28Si是硅的一种同位素,其原子核内质子数为________ ,Si原子的电子式为_______ ,Si与C的化学性质相似,由此猜想二者在原子结构上的相似之处是_______ 。
(3)计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素_______ 。
(1)Si原子的结构示意图为
(2)28Si是硅的一种同位素,其原子核内质子数为
(3)计算硅元素的近似相对原子质量的计算式为:28×a1%+29×a2%+30×a3%,其中a1%、a2%……是指各同位素
更新时间:2023-10-31 07:51:12
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在 、
、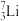 、
、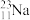 、
、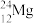 、
、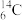 、
、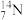 中:
中:
(1)__________ 和__________ 互为同位素;
(2)__________ 和__________ 的质量数相等,但不能互称同位素;
(3)__________ 和__________ 的中子数相等,但质子数不等,所以不是同一种元素
 、
、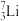 、
、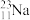 、
、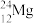 、
、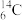 、
、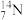 中:
中:(1)
(2)
(3)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)有以下物质: ①NaHSO4晶体 ②SO3③液态硫酸 ④铁 ⑤BaSO4固体 ⑥饱和FeCl3溶液 ⑦酒精(C2H5OH)⑧熔融的K2SO4,其中能导电的是__________ ,属于电解质的是__________ ,属于非电解质的是__________ 。
(2)下列各组化学用语中:①3He、4He ② 2H2 O、1H2O ③ 1H、3H ④14N和13C质子数相同的有_________ ,中子数相同的有________ ,互为同位素的有________
(2)下列各组化学用语中:①3He、4He ② 2H2 O、1H2O ③ 1H、3H ④14N和13C质子数相同的有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学基本概念是学习化学的基石,请正确回答下列问题。
Ⅰ.现有下列基本粒子:1H、2H、3H、230Th、232Th、24Na、24Mg、O2、O3、14N、14C,请回答下列问题:
(1)这些粒子分属_______ 种元素,有_______ 种不同的核素。互为同素异形体的粒子为_______ 。
(2)碳的不同核素12C、13C、14C与氧的不同核素16O、17O、18O可化合生成二氧化碳,可得相对分子质量不同的二氧化碳分子种数为_______ 种。
Ⅱ.现有下列10种物质:①MgBr2 ②NH4Cl ③Na2O2 ④Ba(OH)2 ⑤N2 ⑥CO2 ⑦AlCl3 ⑧H2SO4 ⑨C2H5OH。请完成填空:
(3)属于非电解质的是_______ 。(填编号)
(4)既有离子键又有极性键的是_______ 。(填编号)
(5)1mol Na2O2与水充分反应转移的电子数为_______ 。
(6)用电子式表示MgBr2的形成过程_______ 。
Ⅰ.现有下列基本粒子:1H、2H、3H、230Th、232Th、24Na、24Mg、O2、O3、14N、14C,请回答下列问题:
(1)这些粒子分属
(2)碳的不同核素12C、13C、14C与氧的不同核素16O、17O、18O可化合生成二氧化碳,可得相对分子质量不同的二氧化碳分子种数为
Ⅱ.现有下列10种物质:①MgBr2 ②NH4Cl ③Na2O2 ④Ba(OH)2 ⑤N2 ⑥CO2 ⑦AlCl3 ⑧H2SO4 ⑨C2H5OH。请完成填空:
(3)属于非电解质的是
(4)既有离子键又有极性键的是
(5)1mol Na2O2与水充分反应转移的电子数为
(6)用电子式表示MgBr2的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】观察下列表格,回答相关问题:
(1)其中属于离子化合物的物质有___________ 。
(2)试比较F-、Cl-、Br-的离子半径大小___________ (用元素符号表示);推测离子半径与离子晶体熔点的关系___________ ;猜想KCl的熔点___________ (高于/低于)NaCl的熔点。
(3)由12C、35Cl、37Cl构成的30g CCl4中,35Cl的质量为___________ g(保留2位小数)。
| 物质 | NaF | NaCl | NaBr | KCl | AlCl3 | CH4 | CCl4 |
| 熔点/℃ | 995 | 801 | 755 | 190 | -182.5 | -23 |
(2)试比较F-、Cl-、Br-的离子半径大小
(3)由12C、35Cl、37Cl构成的30g CCl4中,35Cl的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求填空
(1)写出溴原子的核外电子排布式_______
(2)写出氮原子的轨道表示式_________
(3)请解释Fe3+比Fe2+稳定的原因________
(4)由23Na、35Cl、37Cl构成的15g氯化钠中,37Cl的质量为_______
(1)写出溴原子的核外电子排布式
(2)写出氮原子的轨道表示式
(3)请解释Fe3+比Fe2+稳定的原因
(4)由23Na、35Cl、37Cl构成的15g氯化钠中,37Cl的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ、下列物质:①1H、2H、3H ;②H2O、D2O、T2O;③O2、O3;④12C、14C
(1)互为同位素的是______ (填序号,下同);
(2)互为同素异形体的是_____ ;
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有___ 种;
Ⅱ、用化学用语回答下列问题:
(1)写出NaOH的电子式____ ;
(2)用电子式表示二氧化碳分子的形成过程_________ ;
Ⅲ、下列物质:①N2 ②H2O2 ③NH3 ④Na2O ⑤NH4Cl
(1)含有极性键和非极性键的是_______ (填序号,下同);
(2)含有极性键的离子化合物是_________ ;
(3)氟化氢水溶液中存在的氢键有________ 种;
(4)分子(CN)2分子中每个原子最外层均满足8电子稳定结构,其结构式为_____ 。
(1)互为同位素的是
(2)互为同素异形体的是
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有
Ⅱ、用化学用语回答下列问题:
(1)写出NaOH的电子式
(2)用电子式表示二氧化碳分子的形成过程
Ⅲ、下列物质:①N2 ②H2O2 ③NH3 ④Na2O ⑤NH4Cl
(1)含有极性键和非极性键的是
(2)含有极性键的离子化合物是
(3)氟化氢水溶液中存在的氢键有
(4)分子(CN)2分子中每个原子最外层均满足8电子稳定结构,其结构式为
您最近一年使用:0次



