Ⅰ.现有下列物质:①固体氢氧化钡,②石墨棒,③纯醋酸,④液态氯化氢,⑤硫酸氢钾固体,⑥熔融氯化钠,⑦酒精(C2H5OH),⑧碳酸钠粉末。请用序号回答下列问题:
(1)以上物质中能导电的是_______ 。
(2)以上物质中属于电解质的是_______ 。
(3)以上物质中属于非电解质的是_______ 。
Ⅱ.高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止刻蚀液与下层(砷化镓)反应。
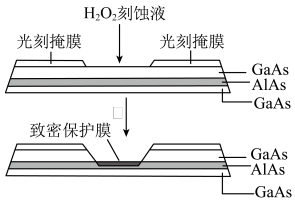
(4)已知:Ga和Al最外层电子数相同,As和N最外层电子数相同。在H2O2与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂的物质的量之比为_______ 。
(5)配平下列化学方程式_______ 。
_______Cu+_______HNO3(稀)=_______Cu(NO3)2+_______NO↑+_______H2O
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
Ⅱ.高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止刻蚀液与下层(砷化镓)反应。

(4)已知:Ga和Al最外层电子数相同,As和N最外层电子数相同。在H2O2与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂的物质的量之比为
(5)配平下列化学方程式
_______Cu+_______HNO3(稀)=_______Cu(NO3)2+_______NO↑+_______H2O
更新时间:2023-11-26 17:34:02
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】(一)现有以下物质:①碳棒 ②盐酸 ③H2SO4 ④氨水 ⑤熔融KOH ⑥NH3 ⑦CCl4 ⑧CO2 ⑨冰醋酸 ⑩NaHSO4固体
(1)上述物质中,可导电的是___________ 。
(2)上述物质中,属于非电解质的是___________ 。
(3)上述物质中,属于电解质但不导电的是___________ 。
(4)上述物质中,属于弱电解质的是___________ 。
(5)写出③、⑨两种物质在水溶液中的电离方程式。
③:___________ 。
⑨:___________ 。
(二)书写下列反应的离子方程式。
①Na2CO3溶液和H2SO4:___________ ;
②KCl溶液和AgNO3溶液:___________ ;
③NaOH溶液和NaHSO4溶液:___________
(1)上述物质中,可导电的是
(2)上述物质中,属于非电解质的是
(3)上述物质中,属于电解质但不导电的是
(4)上述物质中,属于弱电解质的是
(5)写出③、⑨两种物质在水溶液中的电离方程式。
③:
⑨:
(二)书写下列反应的离子方程式。
①Na2CO3溶液和H2SO4:
②KCl溶液和AgNO3溶液:
③NaOH溶液和NaHSO4溶液:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】利用分类法研究化学物质可系统、全面认识物质的性质。
Ⅰ.下列三组物质中,均有一种物质的类别与其他三种不同
①MgO、Na2O、CO2、CuO
②H2SO3、H2O、H2SO4、HNO3
③Mg(OH)2、Fe(OH)3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):①_______ ; ②_______ ; ③_______ 。
(2)这三种物质相互作用可生成一种新物质K2CO3,该反应_______ (填“是”或“不是”)氧化还原反应。
(3)写出CO2与足量KOH溶液反应的化学方程式:_____
II.现有以下物质:
①NaCl晶体②液态HCl③CaCO3固体④熔融KCl⑤蔗糖 ⑥铜⑦CO2⑧H2SO4⑨KOH固体
(1)以上物质中能导电的是_______ 。
(2)以上物质中属于电解质的是_______ ,属于非电解质的是_______ 。
(3)以上物质中,溶于水能导电的非电解质是_______ 。
Ⅰ.下列三组物质中,均有一种物质的类别与其他三种不同
①MgO、Na2O、CO2、CuO
②H2SO3、H2O、H2SO4、HNO3
③Mg(OH)2、Fe(OH)3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):①
(2)这三种物质相互作用可生成一种新物质K2CO3,该反应
(3)写出CO2与足量KOH溶液反应的化学方程式:
II.现有以下物质:
①NaCl晶体②液态HCl③CaCO3固体④熔融KCl⑤蔗糖 ⑥铜⑦CO2⑧H2SO4⑨KOH固体
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中,溶于水能导电的非电解质是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】CO2、碳酸盐、有机物等均是自然界碳循环中的重要物质。回答下列问题:
(1)下列物质属于化合物但不属于电解质的是______ (填字母)。
A.石墨 B.汽油 C.乙醇 D.碳酸
(2)倍半碳酸钠(Na2CO3·NaHCO3·2H2O)在水溶液中的电离方程式为__________________________ 。
(3)金属钠在足量CO2中燃烧生成常见的盐和单质,写出反应的化学方程式:____________ 。
(4)铜器表面的难溶物Cu2(OH)2CO3可用稀硫酸洗涤除去,该反应的离子方程式为________________ 。
(5)工业上制取金刚砂的反应为: ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为______ 。
(1)下列物质属于化合物但不属于电解质的是
A.石墨 B.汽油 C.乙醇 D.碳酸
(2)倍半碳酸钠(Na2CO3·NaHCO3·2H2O)在水溶液中的电离方程式为
(3)金属钠在足量CO2中燃烧生成常见的盐和单质,写出反应的化学方程式:
(4)铜器表面的难溶物Cu2(OH)2CO3可用稀硫酸洗涤除去,该反应的离子方程式为
(5)工业上制取金刚砂的反应为:
 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:
①“84”消毒液;②高铁酸钠(Na2FeO4);③ClO2;④O3;⑤碘酒;⑥75%酒精。 回答下列问题:
(1)上述杀菌消毒剂属于电解质的是___________ (填序号)。
(2)“84”消毒液可由 Cl2与NaOH 溶液反应制得,Cl2与NaOH溶液反应的离子方程式为___________
(3)工业上可在NaOH溶液中,用NaClO氧化 Fe(OH)3制备 Na2FeO4。制备反应的离子方程式为___________ 。
①“84”消毒液;②高铁酸钠(Na2FeO4);③ClO2;④O3;⑤碘酒;⑥75%酒精。 回答下列问题:
(1)上述杀菌消毒剂属于电解质的是
(2)“84”消毒液可由 Cl2与NaOH 溶液反应制得,Cl2与NaOH溶液反应的离子方程式为
(3)工业上可在NaOH溶液中,用NaClO氧化 Fe(OH)3制备 Na2FeO4。制备反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】有以下10种物质,请回答下列问题:
①干冰②氢氧化钠固体③氯气④稀硫酸⑤NaHSO4溶液⑥熔融碳酸氢钠固体⑦氢氧化钡溶液⑧冰醋酸③氯化氢⑩NH3⑪Na2CO3·10H2O
(1)其中能导电的是___________ (填写符号,下同);属于电解质的是___________ ;属于非电解质的是___________ 。
(2)分别写出物质⑪在水中的电离方程式:___________ 。
(3)写出物质①和足量⑦在水中发生反应的离子方程式:___________ 。
(4)写出②和⑤发生反应的离子方程式:___________ 。
(5)写出物质④和⑦反应的离子方程式:___________ 。
①干冰②氢氧化钠固体③氯气④稀硫酸⑤NaHSO4溶液⑥熔融碳酸氢钠固体⑦氢氧化钡溶液⑧冰醋酸③氯化氢⑩NH3⑪Na2CO3·10H2O
(1)其中能导电的是
(2)分别写出物质⑪在水中的电离方程式:
(3)写出物质①和足量⑦在水中发生反应的离子方程式:
(4)写出②和⑤发生反应的离子方程式:
(5)写出物质④和⑦反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】红热的铁与水蒸气反应的化学方程式为___________ ,该反应中氧化剂是___________ (填化学式)。将烧至红热的铁丝伸到盛有氯气的集气瓶中,可观察到铁丝剧烈燃烧,产生棕黄色的烟,反应的化学方程式为___________ ,该反应中被还原的物质是___________ (填化学式)。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质不属于硅酸盐的是_______。
(2)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为_______ ,工艺师常用_______ (填物质名称)来雕刻玻璃。
(3)Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是_______ 。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
(4)工业上常利用反应2C+SiO2 Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是_______ (填化学式,下同),氧化剂是_______ 。
(1)下列物质不属于硅酸盐的是_______。
| A.陶瓷 | B.玻璃 | C.水泥 | D.生石灰 |
(3)Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩埚
(4)工业上常利用反应2C+SiO2
 Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】回答下列问题
(1)已知下列十种物质①CH3COOH ②Cu ③NO ④干冰 ⑤硫酸 ⑥Ba(OH)2 ⑦Fe(OH)3胶体⑧液氨⑨稀硝酸⑩NaHSO4。根据上述提供的物质,回答下列问题
①属于电解质的是_______ (填序号,下同),属于非电解质的是_______ 。
②在熔融状态下不导电而在水溶液下导电的电解质是_______ 。
(2)地壳中含量最多的金属元素原子结构示意图_______ ;写出CH3COOH电离方程式_______
(3)下列微粒:Fe2+、Cl-、H+、HCl、Zn,其中只有氧化性的微粒是______ ,只有还原性的微粒是______ ,既有氧化性又有还原性的微粒是______ 。
(1)已知下列十种物质①CH3COOH ②Cu ③NO ④干冰 ⑤硫酸 ⑥Ba(OH)2 ⑦Fe(OH)3胶体⑧液氨⑨稀硝酸⑩NaHSO4。根据上述提供的物质,回答下列问题
①属于电解质的是
②在熔融状态下不导电而在水溶液下导电的电解质是
(2)地壳中含量最多的金属元素原子结构示意图
(3)下列微粒:Fe2+、Cl-、H+、HCl、Zn,其中只有氧化性的微粒是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】Cl2是一种有毒气体,如果泄漏会造成严重的危害。
(1)已知:3Cl2+8NH3 = 6NH4Cl+ N2,化工厂可用浓氨水来检验Cl2是否泄漏。当有少量Cl2泄漏,可以观察到的现象是__________________________________ 。
(2)喷射石灰乳等碱性物质可以减轻少量Cl2泄漏造成的危害。Cl2和石灰乳反应的化学方程式是_____________________ 。
(3)实验室常用烧碱溶液吸收Cl2。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为8︰1时,混合液中NaClO和NaClO3的物质的量之比为_______ 。
(1)已知:3Cl2+8NH3 = 6NH4Cl+ N2,化工厂可用浓氨水来检验Cl2是否泄漏。当有少量Cl2泄漏,可以观察到的现象是
(2)喷射石灰乳等碱性物质可以减轻少量Cl2泄漏造成的危害。Cl2和石灰乳反应的化学方程式是
(3)实验室常用烧碱溶液吸收Cl2。若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为8︰1时,混合液中NaClO和NaClO3的物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。

(1)反应I:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ•mol-1
反应III:S(s)+O2(g)=SO2(g) ΔH3=-297kJ•mol-1
反应II的热化学方程式:_____ 。
(2)对反应II,在同一投料比,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。p2____ p1(填“>”或“<”),得出该结论的理由是_____ 。

(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+SO2=____ +SO +2I-
+2I-

(1)反应I:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551kJ•mol-1
反应III:S(s)+O2(g)=SO2(g) ΔH3=-297kJ•mol-1
反应II的热化学方程式:
(2)对反应II,在同一投料比,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。p2

(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+SO2=
 +2I-
+2I-
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】对于数以万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
I.现有以下物质:
① ②
② ③
③ ④
④ 胶体 ⑤
胶体 ⑤ (酒精) ⑥
(酒精) ⑥ ⑦稀硫酸 ⑧
⑦稀硫酸 ⑧ 溶液
溶液
(1)属于电解质的是___________ ,属于非电解质的是___________ ,属于强电解质的是___________ 。
(2)向④ 胶体中加入⑦可以观察到的现象是
胶体中加入⑦可以观察到的现象是___________ 。
(3)“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化剂及军事科学中。所谓“纳米材料”是指研究、开发出的微粒直径从几纳米到几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物可能具有的性质是___________。
(4)磷能形成多种具有独特性质的物质。
①如磷能形成红磷、白磷、黑磷等多种单质,它们互为___________ (填相互关系)。白磷有剧毒,硫酸铜可作为白磷中毒的解毒剂,请配平相应的化学方程式:___________
______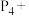 ______
______ ______
______ ______
______ ______
______ ______
______
②磷的一种组成为 的盐,能与盐酸反应,但不能与
的盐,能与盐酸反应,但不能与 溶液反应,下列有关
溶液反应,下列有关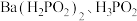 的分析中正确的是
的分析中正确的是___________ (填字母)。
A. 是酸式盐 B.
是酸式盐 B. 是正盐
是正盐
C.均具有较强的还原性 D. 是三元弱酸
是三元弱酸
I.现有以下物质:
①
 ②
② ③
③ ④
④ 胶体 ⑤
胶体 ⑤ (酒精) ⑥
(酒精) ⑥ ⑦稀硫酸 ⑧
⑦稀硫酸 ⑧ 溶液
溶液(1)属于电解质的是
(2)向④
 胶体中加入⑦可以观察到的现象是
胶体中加入⑦可以观察到的现象是(3)“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化剂及军事科学中。所谓“纳米材料”是指研究、开发出的微粒直径从几纳米到几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物可能具有的性质是___________。
| A.能全部透过滤纸 | B.有丁达尔效应 | C.所得液体为胶体 | D.所得物质一定是悬浊液 |
①如磷能形成红磷、白磷、黑磷等多种单质,它们互为
______
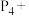 ______
______ ______
______ ______
______ ______
______ ______
______
②磷的一种组成为
 的盐,能与盐酸反应,但不能与
的盐,能与盐酸反应,但不能与 溶液反应,下列有关
溶液反应,下列有关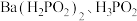 的分析中正确的是
的分析中正确的是A.
 是酸式盐 B.
是酸式盐 B. 是正盐
是正盐C.均具有较强的还原性 D.
 是三元弱酸
是三元弱酸
您最近一年使用:0次



