电化学是化学研究重要分支,在生产生活中发挥着非常重要的作用。请回答下列问题:
铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为 。
。
(1)放电时,正极的电极反应式:______ ,电解质溶液中硫酸的浓度______ (填“增大”“减小”或“不变”),当外电路通过1mol 时,理论上负极板的质量增加
时,理论上负极板的质量增加______ g。
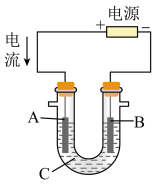
(2)用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。
如下图所示,电解液c选用______ 溶液,A电极的材料是______ ,B电极反应式是______ 。
铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为
 。
。(1)放电时,正极的电极反应式:
 时,理论上负极板的质量增加
时,理论上负极板的质量增加(2)用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。
如下图所示,电解液c选用

更新时间:2023-12-04 11:17:58
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:
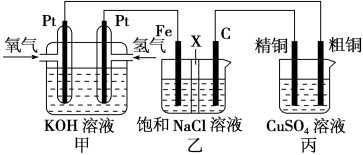
(1)石墨电极为______ (填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入”酚酞溶液,________ (填“铁极”或“石墨极”)区的溶液先变红。乙池中电解总反应化学方程式为_________ 。
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,溶液中硫酸铜浓度将________ (填“增大”“减小”或“不变”)。精铜电极上的电极反应式为_________ 。
(3)若在标准状况下,有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下体积为________ mL;丙装置中阴极析出铜的质量为__________ g。
(4)若将甲改用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得燃料电池,则该电池负极反应式为______ ,正极反应式为_______ 。

(1)石墨电极为
(2)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,溶液中硫酸铜浓度将
(3)若在标准状况下,有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下体积为
(4)若将甲改用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得燃料电池,则该电池负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极_____ (填图中的字母);在电极d上发生的电极反应式为_____ 。

若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为_____ 。
(2)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是_____ 。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(1)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极

若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为
(2)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电化学应用广泛。请回答下列问题:
(1)自发进行的氧化还原反应可以设计成原电池。若电池放电时的反应式为:2Cu+2H2SO4+O2= 2CuSO4+2H2O,该电池的负极材料为_______ ;正极的电极反应式为____________ 。
(2)燃料电池和二次电池的应用非常广泛。
①如图为甲烷燃料电池的示意图,则负极的电极反应式为_____________________ ;

②铅蓄电池为生活中常用的二次电池。放电时的反应为:PbO2 +Pb+2H2SO4=2PbSO4 + 2H2O,铅蓄电池负极的电极反应式为_____ ;充电时,铅蓄电池的PbO2极应与外加直流电源的____ 极相连。
(3)以铅蓄电池为电源精炼粗铜(含Fe、Pb、Ag、Au及其他不反应物质)时,以硫酸铜溶液为电解质溶液,粗铜做____ 极;精炼一段时间后,当阴极增重128 g时,铅蓄电池参加反应的硫酸的物质的量为____ mol。
(1)自发进行的氧化还原反应可以设计成原电池。若电池放电时的反应式为:2Cu+2H2SO4+O2= 2CuSO4+2H2O,该电池的负极材料为
(2)燃料电池和二次电池的应用非常广泛。
①如图为甲烷燃料电池的示意图,则负极的电极反应式为

②铅蓄电池为生活中常用的二次电池。放电时的反应为:PbO2 +Pb+2H2SO4=2PbSO4 + 2H2O,铅蓄电池负极的电极反应式为
(3)以铅蓄电池为电源精炼粗铜(含Fe、Pb、Ag、Au及其他不反应物质)时,以硫酸铜溶液为电解质溶液,粗铜做
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)一种熔融碳酸盐燃料电池原理示意如图所示。电池工作时,外电路上电流的方向应从电极 向电极
向电极
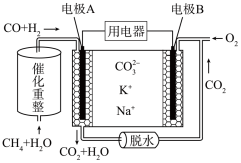
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①假设使用的“燃料”是氢气(H2),则a极的电极反应式为
若电池中氢气(H2)通入量为224 mL(标准状况),且反应完全,则理论上通过电流表的电量为
②假设使用的“燃料”是甲醇(CH3OH),则a极的电极反应式为
如果消耗甲醇160g,假设化学能完全转化为电能,则转移电子的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
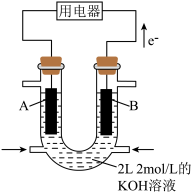
【推荐2】如图所示为 燃料电池的装置(A、B为多孔碳棒);
燃料电池的装置(A、B为多孔碳棒);______ (填A或B)处电极入口通甲烷,其电极反应式为______ ;当消耗甲烷的体积为 (标准状况下)时,消耗
(标准状况下)时,消耗 的质量为
的质量为______ g。
 燃料电池的装置(A、B为多孔碳棒);
燃料电池的装置(A、B为多孔碳棒); (标准状况下)时,消耗
(标准状况下)时,消耗 的质量为
的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学能转化为电能的原理的发现和各式各样电池装置的发明,是贮能和功能技术的巨大进步。
回答下列问题:
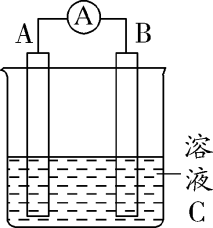
(1)上图中C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为__________________ ,反应进行一段时间后溶液C的pH将___________ (填“升高”“降低”或“基本不变”)。
(2)若将反应Cu +2Ag+=2Ag +Cu2+按图1所示设计一个原电池装置,则负极A的材料为___________ ,溶液C为___________ ,当导线上有2.5mole-流过时,正极生成银的质量为________________ 。
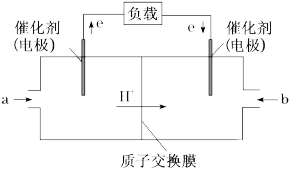
(3)下图为甲烷(CH4)燃料电池的构造示意图,d 电极是___________ (填“正极”或“负极”),C电极的反应方程式为___________________________ 。
回答下列问题:
(1)上图中C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
(2)若将反应Cu +2Ag+=2Ag +Cu2+按图1所示设计一个原电池装置,则负极A的材料为
(3)下图为甲烷(CH4)燃料电池的构造示意图,d 电极是
您最近一年使用:0次



