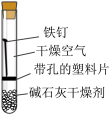
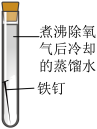
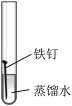
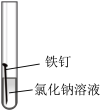
某小组同学对不同条件下铁钉的锈蚀进行了实验。
(1)一周后观察,铁钉被腐蚀程度最大的是___________ (填实验序号)。
(2)实验小组将实验④中氯化钠溶液分别替换为pH=2和pH=4的盐酸溶液。在密闭容器中,分别用压强传感器记录实验过程中的压强变化,如图所示。___________ (填字母,下同)。
a.两容器中负极反应均为Fe-2e⁻=Fe2+
b.曲线a记录的是pH=2的盐酸中压强的变化
c.在弱酸性溶液中,铁钉能发生吸氧腐蚀
d.曲线b记录的容器中正极反应是O2+4e⁻+2H2O=4OH⁻
(3)电化学原理在保护海水中钢闸门中有广泛应用。______ 。
a.牺牲阳极法 b.外加电流法
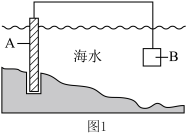
②为了减缓海水对钢闸门A的腐蚀,图1中材料B可以选择______ 。
a.碳棒 b.锌板 c.铜板
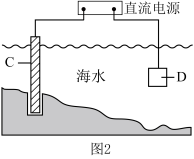
③图2中,钢闸门C应连接直流电源的___________ (填“正”或“负”)极。
| 序号 | ① | ② | ③ | ④ |
| 实验 |
|
|
|
|
(1)一周后观察,铁钉被腐蚀程度最大的是
(2)实验小组将实验④中氯化钠溶液分别替换为pH=2和pH=4的盐酸溶液。在密闭容器中,分别用压强传感器记录实验过程中的压强变化,如图所示。

a.两容器中负极反应均为Fe-2e⁻=Fe2+
b.曲线a记录的是pH=2的盐酸中压强的变化
c.在弱酸性溶液中,铁钉能发生吸氧腐蚀
d.曲线b记录的容器中正极反应是O2+4e⁻+2H2O=4OH⁻
(3)电化学原理在保护海水中钢闸门中有广泛应用。
a.牺牲阳极法 b.外加电流法
②为了减缓海水对钢闸门A的腐蚀,图1中材料B可以选择
a.碳棒 b.锌板 c.铜板
③图2中,钢闸门C应连接直流电源的
更新时间:2023-12-25 22:10:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某小组学生研究常见的金属腐蚀现象,分析其原理。按要求回答下列问题。
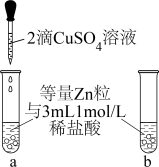
(1)甲同学设计如图所示对比实验。当a中滴入 溶液后,观察到其中产生气泡的速率较b中的
溶液后,观察到其中产生气泡的速率较b中的__ (填“快”或“慢”)。其原因是_____________________________________________________ 。
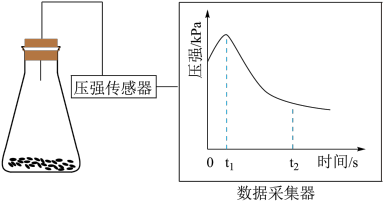
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。
①0~ 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为____________ 。
② ~
~ 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为_____________________________________________________ 。
③0~ 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为________________________________________________ 。
(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
①暖贴工作时,铁粉发生的反应为________________________ (填“氧化反应”或“还原反应”)。
②当暖贴放热结束时,铁粉转化成的物质中可能含有________________________ 。
(1)甲同学设计如图所示对比实验。当a中滴入
 溶液后,观察到其中产生气泡的速率较b中的
溶液后,观察到其中产生气泡的速率较b中的
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。

①0~
 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为②
 ~
~ 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为③0~
 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
| 品名:一次性保暖贴 主要成分:铁粉、水、食盐、活性炭、蛭石、吸水性树脂 产品性能:平均温度55,最高温度63,发热时间12小时以上 |
②当暖贴放热结束时,铁粉转化成的物质中可能含有
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图所示的是铁钉在水中被腐蚀的实验:
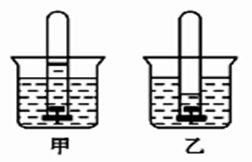
(1)甲图发生的是_________ 腐蚀,电极反应式是正极________ ,负极__________ 。
(2)乙图发生的是___________ 腐蚀,电极反应式是:正极________________ ,负极________________ 。

(1)甲图发生的是
(2)乙图发生的是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一
Ⅰ.如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁块,放置一段时间均被腐蚀,这两种腐蚀都属于电化学腐蚀。

(1)红墨水柱两边的液面变为左低右高,则___________ (填“a”或“b”)边盛有食盐水。
(2)b试管中铁发生的是___________ 腐蚀。
Ⅱ.下面两个图都是金属防护的例子。
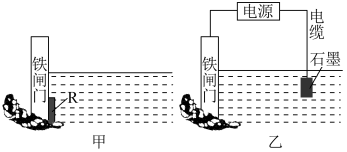
(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用___________ (从下面选项中选择),此方法叫做___________ 保护法。
A.铜 B.钠 C.锌 D.石墨
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的___________ 极。
(5)采取以上两种方法,___________ (填“甲”或“乙”)种能使铁闸门保护得更好。
Ⅰ.如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁块,放置一段时间均被腐蚀,这两种腐蚀都属于电化学腐蚀。

(1)红墨水柱两边的液面变为左低右高,则
(2)b试管中铁发生的是
Ⅱ.下面两个图都是金属防护的例子。

(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的
(5)采取以上两种方法,
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)写出下列物质的电离方程式:
①H2S:_______
②NaHCO3溶于水:_______ ③NaHSO4溶于水:_______
(2)下出下列盐的水解方程式(离子方程式):
①NH4Cl:_______
②明矾净水原理(只写相应离子的水解方程式):_______
③泡沫灭火器(硫酸铝和碳酸氢钠)的灭火原理:_______
(3)写出难溶电解质的溶度积表达式。Mg(OH)2:_______
(4)下出下列反应方程式:
①钢铁发生吸氧腐蚀的正极反应式:_______
②氢氧燃料电池,H2SO4做电解质溶液,正极反应式:_______
③电解饱和食盐水的总反应方程式:_______
①H2S:
②NaHCO3溶于水:
(2)下出下列盐的水解方程式(离子方程式):
①NH4Cl:
②明矾净水原理(只写相应离子的水解方程式):
③泡沫灭火器(硫酸铝和碳酸氢钠)的灭火原理:
(3)写出难溶电解质的溶度积表达式。Mg(OH)2:
(4)下出下列反应方程式:
①钢铁发生吸氧腐蚀的正极反应式:
②氢氧燃料电池,H2SO4做电解质溶液,正极反应式:
③电解饱和食盐水的总反应方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求回答下列问题:
(1)钢铁制品在潮湿环境中发生的电化学腐蚀类型主要是_______ 腐蚀,此时正极反应为_______ ,一 段时间后,钢铁制品表面会生成铁锈,其主要成分为_______ (填化学式)。
(2)燃料电池具有广阔的发展前景,能量转化效率高。工作时,燃料和氧化剂由外部供给,分别在惰性电极上参与电极反应。若通入的燃料为甲烷(CH4),电解质溶液为酸性,则CH4在电极上发生反应的方程式为_______ 。
(1)钢铁制品在潮湿环境中发生的电化学腐蚀类型主要是
(2)燃料电池具有广阔的发展前景,能量转化效率高。工作时,燃料和氧化剂由外部供给,分别在惰性电极上参与电极反应。若通入的燃料为甲烷(CH4),电解质溶液为酸性,则CH4在电极上发生反应的方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】请用所学的化学知识解释下列反应。
(1)Ag2O-Zn-KOH 组成的纽扣电池,正极区 pH 增大,请用电极反应式解释:______________ 。
(2)炒过菜的铁锅不及时清洗(未洗净残液中含 NaCl),不久会生锈,写出正极电极反应 式:_____________ ,其锈蚀过程属于_____ (填“析氢腐蚀”或“吸氧腐蚀”)。
(3)CuO 中含 Fe2O3,要想用此化合物制得纯净的 CuCl2 固体涉及流程为:

①物质 a 为加入_____ 把 pH 调到_____ 。
②操作 c 为在_____ 条件下加热蒸干得固体 CuCl2。
(4)C2H6在足量 O2中完全燃烧,当转移 7 mol e-时放热 a kJ,写出表示 C2H6 燃烧热的热化学方程式:_____ 。
(5)CO2 中混有 HCl,可用饱和 NaHCO3 溶液吸收 HCl,请用平衡移动原理解释原因_____
(1)Ag2O-Zn-KOH 组成的纽扣电池,正极区 pH 增大,请用电极反应式解释:
(2)炒过菜的铁锅不及时清洗(未洗净残液中含 NaCl),不久会生锈,写出正极电极反应 式:
(3)CuO 中含 Fe2O3,要想用此化合物制得纯净的 CuCl2 固体涉及流程为:

| Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀 pH | 1.9 | 4.7 |
| 完全沉淀 pH | 3.2 | 6.7 |
①物质 a 为加入
②操作 c 为在
(4)C2H6在足量 O2中完全燃烧,当转移 7 mol e-时放热 a kJ,写出表示 C2H6 燃烧热的热化学方程式:
(5)CO2 中混有 HCl,可用饱和 NaHCO3 溶液吸收 HCl,请用平衡移动原理解释原因
您最近半年使用:0次
【推荐1】根据原电池原理和电解原理进行如图回答。请回答:用如图所示装置进行实验(K闭合)。
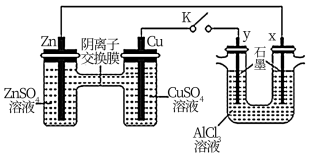
(1)Zn极为___________ 极;实验过程中,SO
____________ (填“从左向右”、“从右向左”或“不”)移动,Cu极的电极反应式为:___________ 。
(2)y极为___________ 极;x的电极反应现象为___________ ;写出右边装置的总反应式:___________ 。
(3)写出生活中对钢闸门的一种电化学保护方法___________ 。
(4)有人设想寻求合适的催化剂和电极材料,以O2、CH4为电极反应物,以NaOH为电解质溶液制取新型燃料电池,请写出该电池的正极反应式___________ 。

(1)Zn极为

(2)y极为
(3)写出生活中对钢闸门的一种电化学保护方法
(4)有人设想寻求合适的催化剂和电极材料,以O2、CH4为电极反应物,以NaOH为电解质溶液制取新型燃料电池,请写出该电池的正极反应式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
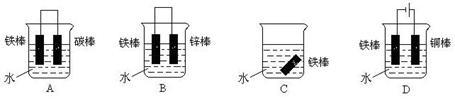
(1)下列哪个装置可防止铁棒被腐蚀_____________ 。
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如右:
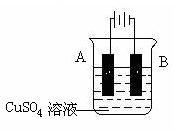
请回答:
①A电极对应的金属是______ (写元素名称),B电极的电极反应式是____________ 。
②若电镀前铁、铜两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为51.2 g,则电镀时电路中通过的电子物质的量为_______ 。
(1)下列哪个装置可防止铁棒被腐蚀

(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如右:

请回答:
①A电极对应的金属是
②若电镀前铁、铜两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为51.2 g,则电镀时电路中通过的电子物质的量为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
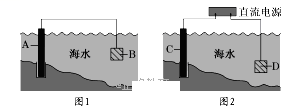
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择________ (填字母)。
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:______________________ 。
(2)图2中,钢闸门C作________ 极。若用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应为________________________________________ ,检测该电极反应产物的方法是________________________ 。

(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:
(2)图2中,钢闸门C作
您最近半年使用:0次