元素周期表是学习化学的重要工具。下表为某些元素在周期表中的位置。
(1)按①→②→③→④的顺序,其原子半径逐渐_____ (填“增大”或“减小”),得电子能力逐渐______ (填“增强”或“减弱”,下同),单质的氧化性逐渐______ ,非金属性逐渐______ ,最简单氢化物的稳定性逐渐______ 。
(2)表中化学性质最稳定的元素为___________ (填元素符号)。
(3)⑥与③形成原子个数比为1:1的化合物,属于______ 化合物(填“离子”或“共价”)其电子式为:________ ,含有的化学键________ 。
(4)⑦与⑧的最高价氧化物对应的水化物是否可以相互反应______ (填“是”或“否”)。
(5)⑨的最高价氧化物对应的水化物为________ (填化学式)。
周期 | 族 | |||||||
Ⅰ A | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | 0 | |
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)按①→②→③→④的顺序,其原子半径逐渐
(2)表中化学性质最稳定的元素为
(3)⑥与③形成原子个数比为1:1的化合物,属于
(4)⑦与⑧的最高价氧化物对应的水化物是否可以相互反应
(5)⑨的最高价氧化物对应的水化物为
更新时间:2024-01-24 09:38:33
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】填写下列表格。
| 元素(原子团)名称 | 化学式 | 质子数 | 原子(离子)结构示意图 | 核外电子数 |
| 硫离子 | ||||
| 硫酸根 | ||||
| 铵根 |
您最近一年使用:0次
【推荐2】按要求完成下列问题:
(1)写出羟基的电子式:_______
(2) 的分子式
的分子式_______
(3)与H2加成生成2,4-二甲基己烷的炔烃的系统命名_______
(4)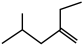 的系统命名
的系统命名_______ 。
(1)写出羟基的电子式:
(2)
 的分子式
的分子式(3)与H2加成生成2,4-二甲基己烷的炔烃的系统命名
(4)
 的系统命名
的系统命名
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】门捷列夫在他的第一张周期表上留下的空位中的元素“类铝”于1875年由法国化学家布瓦博德朗发现,并命名为镓,而布瓦博德朗当时并未受到门捷列夫预言的启发。门捷列夫在得知这一发现后指出:他相信镓和“类铝”是同一种物质,并认为镓的密度应该是5.9-6.0g/cm3,而不是布瓦博德朗发表的4.7g/cm3。当时布瓦博德朗认为只有他本人才拥有镓,门捷列夫怎么会知道这种金属的密度呢?他没有固执己见,重新提纯了镓,最后测得的密度果然是5.94g/cm3。这一发现使他大为惊讶,他在一篇论文中写道:“我以为没有必要再来说明门捷列夫这一理论的巨大意义了。”
(1)阅读上述资料,你得到什么启示?写一篇小论文与同学交流_________ 。
(2)请你查阅资料,了解门捷列夫还预言了哪些新元素,以及当时这些新元素是如何被确认的,撰写研究报告,并与同学交流____________ 。
(1)阅读上述资料,你得到什么启示?写一篇小论文与同学交流
(2)请你查阅资料,了解门捷列夫还预言了哪些新元素,以及当时这些新元素是如何被确认的,撰写研究报告,并与同学交流
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,根据表中给出10种元素按要求作答。
(1)镁元素位于元素周期表中第____________ 周期____________ 族;
(2)空气组成中体积分数最大的气体是____________ ;
(3)O与S相比,原子半径较小的是____________ ;
(4)金刚石的组成元素是____________ ;
(5)单质的化学性质最不活泼的元素是____________ ;
(6)Na与Mg元素相比,金属性较强的是____________ ;
(7)NH3与PH3相比,热稳定性较弱的是____________ ;
(8)H2SO4与H3PO4相比,酸性较强的是____________ ;
(9)Mg(OH)2与Al(OH)3,其中属于两性氢氧化物的是____________ ;
(10)单质呈黄绿色的气体组成元素是____________ ,其单质的水溶液呈____________ (填“酸性”或“碱性”)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | C | N | O | Ne | ||||
3 | Na | Mg | Al | P | S | Cl |
(1)镁元素位于元素周期表中第
(2)空气组成中体积分数最大的气体是
(3)O与S相比,原子半径较小的是
(4)金刚石的组成元素是
(5)单质的化学性质最不活泼的元素是
(6)Na与Mg元素相比,金属性较强的是
(7)NH3与PH3相比,热稳定性较弱的是
(8)H2SO4与H3PO4相比,酸性较强的是
(9)Mg(OH)2与Al(OH)3,其中属于两性氢氧化物的是
(10)单质呈黄绿色的气体组成元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下列为元素周期表的一部分、表中阿拉伯数字(1、2……)是元素周期表中行或列的序号,请参照元素A~I在表中的位置,回答下列问题。
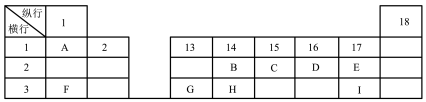
(1)B、C、H三元素中非金属性最强的是__________ (写出元素符号)。
(2)表中某元素能形成两性氧化物,写出该氧化物的化学式___________ 。
(3)D与F构成原子个数比为1:1和1:2的两种离子化合物Z和M,写出Z与H2O反应的化学方程式_____________________________________ 。

(1)B、C、H三元素中非金属性最强的是
(2)表中某元素能形成两性氧化物,写出该氧化物的化学式
(3)D与F构成原子个数比为1:1和1:2的两种离子化合物Z和M,写出Z与H2O反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】氧、硫、硒(Se)、碲(Te)、钋(Po)是元素周期表中原子序数依次增大的同主族元素。回答下列问题:
(1)硒在元素周期表中的位置________ 。
(2) Po的中子数为
Po的中子数为________ 。
(3)某温度时,该族单质与H2反应生成气态H2X的热化学方程式如下:
O2(g)+2H2(g)=2H2O(g) △H1=-484 kJ/mol
S(g)+H2(g) H2S(g) △H2=-20 kJ/mol
H2S(g) △H2=-20 kJ/mol
Se(g)+H2(g) H2Se(g) △H3=+81kJ/mol
H2Se(g) △H3=+81kJ/mol
①硫和硒氢化物的热稳定性:H2S________ H2Se(填“>”、“=”或“<”);判断依据是________ 。
②写出O2(g)与H2S(g)反应生成H2O(g)和S(g)的热化学方程式________ 。
(1)硒在元素周期表中的位置
(2)
 Po的中子数为
Po的中子数为(3)某温度时,该族单质与H2反应生成气态H2X的热化学方程式如下:
O2(g)+2H2(g)=2H2O(g) △H1=-484 kJ/mol
S(g)+H2(g)
 H2S(g) △H2=-20 kJ/mol
H2S(g) △H2=-20 kJ/molSe(g)+H2(g)
 H2Se(g) △H3=+81kJ/mol
H2Se(g) △H3=+81kJ/mol①硫和硒氢化物的热稳定性:H2S
②写出O2(g)与H2S(g)反应生成H2O(g)和S(g)的热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】最新报道,我国科学家通过与多个国家进行科技合作,成功研发出铯(Cs)原子喷泉钟,使我国时间频率基准的精度从30万年不差1秒提高到600万年不差1秒,标志着我国时间频率基准研究进入世界先进行列,已知铯位于元素周期表中第六周期第IA族,根据艳在元素周期表中的位置,推断下列内容:
(1)铯的原子核外共有____ 个电子层,最外层电子数为___ .
(2)铯单质与水剧烈反应,放出______ 色气体,同时使紫色石蕊溶液显______ 色.
(3)预测铯单质的还原性比钠单质的还原性______ (填“弱”或“强”).
(1)铯的原子核外共有
(2)铯单质与水剧烈反应,放出
(3)预测铯单质的还原性比钠单质的还原性
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】元素周期律反映了元素性质随原子序数递增的周期性变化规律。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最强的是___________ (填碱的化学式)。
(2)碱金属元素中,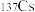 和
和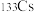 之间的关系是互为
之间的关系是互为___________ ,金属钾的氧化物有多种,写出 与
与 反应的化学方程式:
反应的化学方程式:___________ 。
(3)可根据元素周期律推测元素的某些性质。如已知卤族元素的性质递变规律,可推知元素砹(At)形成的氢化物HAt的稳定性___________ HI的稳定性(填“大于”或“小于”),AgAt___________ 溶于水(填“易”或“难”)。
(4)某实验小组欲通过化学实验证明元素的非金属性:Br>S。
供选择的试剂:氯水、溴水、溴化钠溶液、新制 溶液、四氯化碳、酚酞。
溶液、四氯化碳、酚酞。
①完成该实验需要选用的最合适的试剂为___________ 。
②简述实验操作和实验现象:___________ 。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最强的是
(2)碱金属元素中,
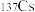 和
和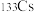 之间的关系是互为
之间的关系是互为 与
与 反应的化学方程式:
反应的化学方程式:(3)可根据元素周期律推测元素的某些性质。如已知卤族元素的性质递变规律,可推知元素砹(At)形成的氢化物HAt的稳定性
(4)某实验小组欲通过化学实验证明元素的非金属性:Br>S。
供选择的试剂:氯水、溴水、溴化钠溶液、新制
 溶液、四氯化碳、酚酞。
溶液、四氯化碳、酚酞。①完成该实验需要选用的最合适的试剂为
②简述实验操作和实验现象:
您最近一年使用:0次

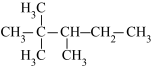 ,请用系统命名法对该有机物命名
,请用系统命名法对该有机物命名

