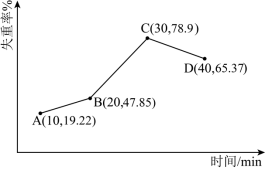
采用热重分析法测定NiSO4·nH2O样品中所含结晶水数。将该样品在900℃下进行煅烧,失重率随时间变化如图所示,A点时失掉3个结晶水,则n值为___________ 。

2024高三·全国·专题练习 查看更多[1]
(已下线)题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
更新时间:2024-02-01 12:28:05
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】按要求计算并填空
(1)32gSO2标况下的体积为____________ L,含有______________ 个氧原子。
(2)1.204×1023个NH3分子所含的氢原子数与________ mol CH4含有的氢原子数相同。
(3)标况下,某CO2和H2混合气体的密度为1.25g/L,则混合气体中CO2和H2的体积比约为______________ 。
(4)200 mL某硫酸盐溶液中含SO42- 1.5 NA个,含金属离子NA个,则该硫酸盐溶液的物质的量浓度为________ mol/L。
(5)把VmL含有Al2(SO4)3和(NH4)2SO4的混合溶液分成两等份,一份加入含足量NaOH的溶液并加热,铵根离子完全反应生成a mol NH3(已知NH4++OH- NH3↑+H2O);另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中Al3+的浓度为
NH3↑+H2O);另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中Al3+的浓度为_____________ mol/L。
(6)将20.0g质量分数为14.0%的 NaNO3溶液与30.0g质量分数为24.0%的NaNO3溶液混合,得到的密度为1.15g/cm3的混合溶液。混合后溶液的物质的量浓度为______ (结果保留1位小数)。
(1)32gSO2标况下的体积为
(2)1.204×1023个NH3分子所含的氢原子数与
(3)标况下,某CO2和H2混合气体的密度为1.25g/L,则混合气体中CO2和H2的体积比约为
(4)200 mL某硫酸盐溶液中含SO42- 1.5 NA个,含金属离子NA个,则该硫酸盐溶液的物质的量浓度为
(5)把VmL含有Al2(SO4)3和(NH4)2SO4的混合溶液分成两等份,一份加入含足量NaOH的溶液并加热,铵根离子完全反应生成a mol NH3(已知NH4++OH-
 NH3↑+H2O);另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中Al3+的浓度为
NH3↑+H2O);另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中Al3+的浓度为(6)将20.0g质量分数为14.0%的 NaNO3溶液与30.0g质量分数为24.0%的NaNO3溶液混合,得到的密度为1.15g/cm3的混合溶液。混合后溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】设NA表示阿伏伽德罗常数。
(1)已知一个NO、NO2分子的质量分别是ag、bg。则一个氧原子的质量是________ ,氧原子的摩尔质量是(用含a、b数字的式子表示)________ ,10 g NO2物质的量为(用含b的式子表示)________ 。
(2)已知H2+Cl2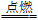 2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为
2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为________ NA,此时气体总质量为________ 。
(3)含有NA个OH-的Ca(OH)2的质量是________ ,n(Ca2+)=________ 。
(1)已知一个NO、NO2分子的质量分别是ag、bg。则一个氧原子的质量是
(2)已知H2+Cl2
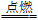 2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为
2HCl,在某密闭容器中使NA个Cl2与2 mol H2充分反应后,容器中气体分子数目为(3)含有NA个OH-的Ca(OH)2的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】硫酸钠-过氧化氢加合物(xNa2SO4·yH2O2·zH2O)的组成可通过下列实验测定:①准确称取17.700g样品,配制成100.00mL溶液A。②将A两等份,取一份,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65g。③另一份加适量稀硫酸酸化后,与50mL0.2mol·L-1KMnO4溶液恰好完全反应。已知H2O2与KMnO4反应的化学方程式如下:2KMnO4+5H2O2+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O,通过计算确定样品的组成__________ (写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】如图:以一铜锌合金为阳极,一纯铜为阴极(起始时两电极质量相等),进行电解,电解液为硫酸铜溶液,当外电路有1.806×1023个电子转移时,阴极比阳极重19.25g,求铜锌合金中铜的质量分数。

(已知:电极反应式为 阳极: Zn-2e-=Zn2+、Cu-2e-=Cu2+
阴极:Cu2++2e-="Cu " )____

(已知:电极反应式为 阳极: Zn-2e-=Zn2+、Cu-2e-=Cu2+
阴极:Cu2++2e-="Cu " )
您最近一年使用:0次



