Na2CO3可用于纺织、制肥皂、造纸、制玻璃等,NaHCO3可用于制药、焙制糕点等,两者都是白色固体;某实验小组通过以下实验来探究Na2CO3和NaHCO3两种物质的性质。
(1)称取两种固体各 2g,分别放入两个小烧杯中,再各滴加 10mL 蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加 2 滴酚酞试液。
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得到结论___________ 。
②同学们在两烧杯中还观察到了其它现象。其中,盛放Na2CO3 的烧杯中出现的现象:
I.溶液温度升高;
Ⅱ.滴入酚酞后溶液呈___________ 色。
(2)“套管实验”的实验装置如图所示,请分析实验原理,并回答下列问题:
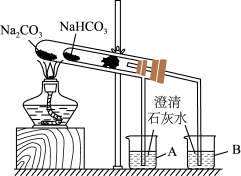
①整个实验过程中,能观察到烧杯 B 中的现象是___________ 。
②写出实验过程中试管中发生反应的化学方程式:___________ 。
③该实验可证明 NaHCO3 的热稳定性___________ (填“强于”“弱于”或“等于”)Na2CO3;证明热稳定性的实验装置中,能否将 NaHCO3、Na2CO3的位置互换?___________ (填“能”或“不能”)。
(3)能用来鉴别 Na2CO3 和 NaHCO3 两种白色固体的实验操作是___________ 。
A.将Na2CO3和NaHCO3 配制成同浓度的溶液,用pH试纸测定pH值并做比较
B.分别加热两种固体样品,看固体是否全部分解挥发
C.分别在这两种物质的溶液中,加入少量NaCl溶液
(1)称取两种固体各 2g,分别放入两个小烧杯中,再各滴加 10mL 蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加 2 滴酚酞试液。
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得到结论
②同学们在两烧杯中还观察到了其它现象。其中,盛放Na2CO3 的烧杯中出现的现象:
I.溶液温度升高;
Ⅱ.滴入酚酞后溶液呈
(2)“套管实验”的实验装置如图所示,请分析实验原理,并回答下列问题:

①整个实验过程中,能观察到烧杯 B 中的现象是
②写出实验过程中试管中发生反应的化学方程式:
③该实验可证明 NaHCO3 的热稳定性
(3)能用来鉴别 Na2CO3 和 NaHCO3 两种白色固体的实验操作是
A.将Na2CO3和NaHCO3 配制成同浓度的溶液,用pH试纸测定pH值并做比较
B.分别加热两种固体样品,看固体是否全部分解挥发
C.分别在这两种物质的溶液中,加入少量NaCl溶液
更新时间:2024-02-23 18:27:23
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备NaHCO3,进一步处理得到产品Na2CO3和NH4Cl,实验流程如图:
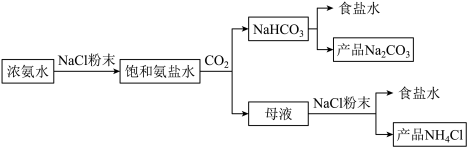
回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO3,正确的连接顺序是_______ (按气流方向,用小写字母表示)。为使A中分液漏斗内的稀盐酸顺利滴下,可将分液漏斗上部的玻璃塞打开或_______ 。
A.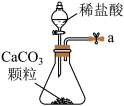 B.
B.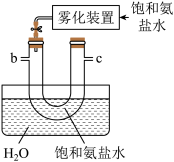 C.
C. D.
D. E.
E.
(2)B中使用雾化装置的优点是_______ 。
(3)生成NaHCO3的总反应的化学方程式为_______ 。
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO3和滤液:
①对固体NaHCO3充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.14 g,则固体NaHCO3的质量为_______ g。
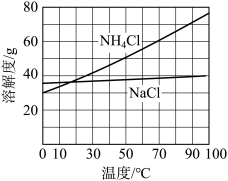
②向滤液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为_______ 、_______ 、洗涤、干燥。

回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO3,正确的连接顺序是
A.
 B.
B. C.
C. D.
D. E.
E.
(2)B中使用雾化装置的优点是
(3)生成NaHCO3的总反应的化学方程式为
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO3和滤液:
①对固体NaHCO3充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.14 g,则固体NaHCO3的质量为
②向滤液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某实验小组利用传感器探究 和
和 的性质。
的性质。
【查阅资料】
pH越小, 越小,溶液碱性越弱。
越小,溶液碱性越弱。
【实验过程】
【分析与解释】
(1)实验Ⅰ中,溶解时吸收热量的物质是_______ 。
(2)实验Ⅱ中, 溶液和澄清石灰水反应的离子方程式为
溶液和澄清石灰水反应的离子方程式为_______ , 未参与该反应的实验证据是
未参与该反应的实验证据是_______ 。
(3)实验Ⅱ中,滴加 溶液的pH变化与滴加
溶液的pH变化与滴加 溶液的有明显差异,原因是滴加
溶液的有明显差异,原因是滴加 溶液的烧杯中,参与反应的离子有
溶液的烧杯中,参与反应的离子有_______ 。
(4)除了以上方法,还有什么化学方法可以区分 和
和 固体?写出对应的实验方案及结论:
固体?写出对应的实验方案及结论:_______ 。
 和
和 的性质。
的性质。【查阅资料】
pH越小,
 越小,溶液碱性越弱。
越小,溶液碱性越弱。【实验过程】
| 编号 | 实验操作 | 实验数据 |
| 实验Ⅰ | 测量下述实验过程的温度变化 |  |
| 实验Ⅱ | 测量下述过程的pH变化 |  |
(1)实验Ⅰ中,溶解时吸收热量的物质是
(2)实验Ⅱ中,
 溶液和澄清石灰水反应的离子方程式为
溶液和澄清石灰水反应的离子方程式为 未参与该反应的实验证据是
未参与该反应的实验证据是(3)实验Ⅱ中,滴加
 溶液的pH变化与滴加
溶液的pH变化与滴加 溶液的有明显差异,原因是滴加
溶液的有明显差异,原因是滴加 溶液的烧杯中,参与反应的离子有
溶液的烧杯中,参与反应的离子有(4)除了以上方法,还有什么化学方法可以区分
 和
和 固体?写出对应的实验方案及结论:
固体?写出对应的实验方案及结论:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示(部分夹持装置已略去)。

(1)图Ⅰ、Ⅱ所示实验中能够达到实验目的的是___________ (填序号)。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为___________ 、___________ 。
(3)若用实验IV验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是___________ (填化学式)。

(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应。
①当澄清石灰水过量时,反应的离子方程式为___________ 。此反应中1mol碳酸氢钠参加反应,生成沉淀质量为___________ 克。
②当碳酸氢钠与氢氧化钙的物质的量之比为2∶1时,所得溶液中溶质的化学式___________ ,请设计实验检验所得溶液中溶质的阴离子:___________ 。

(1)图Ⅰ、Ⅱ所示实验中能够达到实验目的的是
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为
(3)若用实验IV验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是

(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应。
①当澄清石灰水过量时,反应的离子方程式为
②当碳酸氢钠与氢氧化钙的物质的量之比为2∶1时,所得溶液中溶质的化学式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】甲同学尝试用碳酸氢钠作膨松剂蒸馒头,发现蒸出来的馒头有碱味。
Ⅰ.解释现象
(1)甲对此进行解释:因为碳酸氢钠溶液显碱性。他设计如图所示实验,观察到___________ ,认为自己的解释正确。

(2)乙同学不认同甲的解释,依据是碳酸氢钠受热分解产生的碳酸钠也显碱性,写出该反应的化学方程式___________ 。
Ⅱ.设计复合膨松剂。
设计原理:碳酸氢钠及碳酸钠均可与酸反应。
(3)乙在实验室中利用盐酸进行模拟实验。设计了如图所示实验装置,发现2个气球均膨胀,写出发生反应的离子方程式___________ 、___________ 。装置___________ 中(填“A”或者“B”)气球膨胀体积更大,请通过计算说明___________ 。

Ⅰ.解释现象
(1)甲对此进行解释:因为碳酸氢钠溶液显碱性。他设计如图所示实验,观察到

(2)乙同学不认同甲的解释,依据是碳酸氢钠受热分解产生的碳酸钠也显碱性,写出该反应的化学方程式
Ⅱ.设计复合膨松剂。
设计原理:碳酸氢钠及碳酸钠均可与酸反应。
(3)乙在实验室中利用盐酸进行模拟实验。设计了如图所示实验装置,发现2个气球均膨胀,写出发生反应的离子方程式

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】Na2CO3可用于纺织、制肥皂、造纸、制玻璃等,NaHCO3可用于制药、焙制糕点等,两者都是白色固体;某实验小组通过以下实验来探究Na2CO3和NaHCO3两种物质的性质。
(1)称取两种固体各2g,分别放入两个小烧杯中,再各滴加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加2滴酚酞试液。
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得到结论_______ 。
②同学们在两烧杯中还观察到了其它现象。其中盛放Na2CO3的烧杯中出现的现象:I溶液温度升高,Ⅱ_______ (填字母序号)。
a.滴入酚酞后呈无色
b.滴入酚酞后呈红色
(2)“套管实验”的实验装置如图所示,整个实验过程中,能观察到烧杯B中的现象是_______ 。
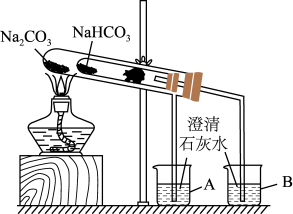
(3)写出实验过程中试管中发生反应的化学方程式:_______ 。
(4)该实验可证明NaHCO3的热稳定性_______ (填“强于”“弱于”或“等于”Na2CO3;证明热稳定性的实验装置中,能否将NaHCO3、Na2CO3的位置互换?_______ (填“能”或“不能”)。
(5)能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是_______ 。
A.将Na2CO3和NaHCO3配制成同浓度的溶液,用pH试纸测定pH值并做比较
B.分别在这两种物质的溶液中,加入少量CaCl2溶液
C.分别在这两种物质的溶液中,加入少量Ca(OH)2溶液
(1)称取两种固体各2g,分别放入两个小烧杯中,再各滴加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴加2滴酚酞试液。
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得到结论
②同学们在两烧杯中还观察到了其它现象。其中盛放Na2CO3的烧杯中出现的现象:I溶液温度升高,Ⅱ
a.滴入酚酞后呈无色
b.滴入酚酞后呈红色
(2)“套管实验”的实验装置如图所示,整个实验过程中,能观察到烧杯B中的现象是

(3)写出实验过程中试管中发生反应的化学方程式:
(4)该实验可证明NaHCO3的热稳定性
(5)能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是
A.将Na2CO3和NaHCO3配制成同浓度的溶液,用pH试纸测定pH值并做比较
B.分别在这两种物质的溶液中,加入少量CaCl2溶液
C.分别在这两种物质的溶液中,加入少量Ca(OH)2溶液
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
(1)某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了如图实验,如图Ⅰ~Ⅳ所示。
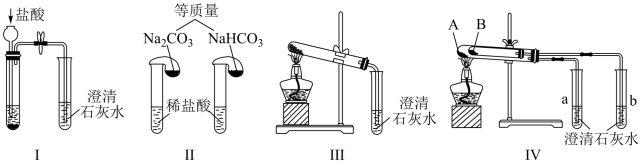
①只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是_______ (填装置序号);
②图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为_______ 、_______ ;与实验Ⅲ相比,实验Ⅳ的优点是_______ (填字母);
A.Ⅳ比Ⅲ复杂
B. Ⅳ比Ⅲ安全
C. Ⅳ比Ⅲ操作简便
D. Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
③若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管 中装入的固体最好是
中装入的固体最好是_______ (填化学式)。
(2)已知 和
和 两支试管所盛的溶液中共含有
两支试管所盛的溶液中共含有 、
、 、
、 、
、 、
、 、
、 六种离子,向试管
六种离子,向试管 的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
①试管 的溶液中所含的上述离子有
的溶液中所含的上述离子有_______ ;
②若向某试管中滴入稀盐酸产生沉淀,则该试管为_______ (填“ ”或“
”或“ ”);
”);
③若向试管 的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是_______ (填化学式);
④若向由试管 溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量
溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量 溶液,则发生反应的离子方程式为
溶液,则发生反应的离子方程式为_______ 。
(1)某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了如图实验,如图Ⅰ~Ⅳ所示。

①只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是
②图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为
A.Ⅳ比Ⅲ复杂
B. Ⅳ比Ⅲ安全
C. Ⅳ比Ⅲ操作简便
D. Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
③若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管
 中装入的固体最好是
中装入的固体最好是(2)已知
 和
和 两支试管所盛的溶液中共含有
两支试管所盛的溶液中共含有 、
、 、
、 、
、 、
、 、
、 六种离子,向试管
六种离子,向试管 的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
的溶液中滴入酚酞试液呈粉红色。请回答下列问题:①试管
 的溶液中所含的上述离子有
的溶液中所含的上述离子有②若向某试管中滴入稀盐酸产生沉淀,则该试管为
 ”或“
”或“ ”);
”);③若向试管
 的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是④若向由试管
 溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量
溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量 溶液,则发生反应的离子方程式为
溶液,则发生反应的离子方程式为
您最近一年使用:0次



