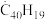 (g)⇌C40H18(g)+H•(g)及
(g)⇌C40H18(g)+H•(g)及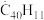 ⇌C40H10(g)+H•(g)反应的lnK(K为平衡常数)随温度倒数的关系如图所示。已知本实验条件下,
⇌C40H10(g)+H•(g)反应的lnK(K为平衡常数)随温度倒数的关系如图所示。已知本实验条件下,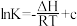 (R为理想气体常数,c为截距)。图中两条线几乎平行,从结构的角度分析其原因是
(R为理想气体常数,c为截距)。图中两条线几乎平行,从结构的角度分析其原因是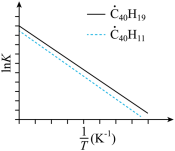
2024高三下·全国·专题练习 查看更多[1]
(已下线)题型四 平衡图像原因解释-备战2024年高考化学答题技巧与模板构建
更新时间:2024-02-29 21:35:59
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】汽车尾气中含有CO、NO、NO2、碳氢化合物等多种污染物。回答下列问题:
(1)汽车燃料中不含氮元素,尾气中所含NO产生的原因是____________________ 。
(2)已知:2C8H18(1)+25O2(g)=16CO2(g)+18H2O(g) △H1=-10244kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2
2NO(g)+2CO(g)=N2(g)+2CO2(g) △H3=-746kJ·mol-1
①若H2O(1)=H2O(g) △H=+44kJ·mol-1,则表示辛烷燃烧热的热化学方程式为____________________ 。
②部分化学键键能数据如下:
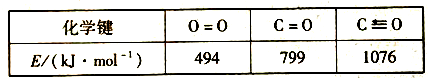
△H2=__________ kJ·mol-1
(3)1573K时,N2+O2 2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为
2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为__________ mol,N2的转化率为__________ 。
(4)反应NO(g)+CO(g)=N2(g)+CO2(g)的平衡常数为1.68×1060,从热力学角度看,该反应程度应该很大,实际汽车尾气中该反应的程度很小,原因是____________________ ,要增大汽车尾气净化装置中单位时间内该反应的程度,关键是要____________________ 。
(5)T<500K时,反应NO2(g)+CO(g)=NO(g)+CO2(g)分两步进行:
第一步:NO2(g)+NO2(g)→NO3(g)+NO(g) (慢反应)
第二步:NO3(g)+CO(g)→NO(g)+CO2(g) (快反应)
下列表述正确的是__________ (填标号)
A.反应速率与NO浓度有关 B.反应速率与NO2浓度有关
C.反应的中间产物只有NO3 D.第二步反应活化能较高
(1)汽车燃料中不含氮元素,尾气中所含NO产生的原因是
(2)已知:2C8H18(1)+25O2(g)=16CO2(g)+18H2O(g) △H1=-10244kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2
2NO(g)+2CO(g)=N2(g)+2CO2(g) △H3=-746kJ·mol-1
①若H2O(1)=H2O(g) △H=+44kJ·mol-1,则表示辛烷燃烧热的热化学方程式为
②部分化学键键能数据如下:

△H2=
(3)1573K时,N2+O2
 2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为
2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为(4)反应NO(g)+CO(g)=N2(g)+CO2(g)的平衡常数为1.68×1060,从热力学角度看,该反应程度应该很大,实际汽车尾气中该反应的程度很小,原因是
(5)T<500K时,反应NO2(g)+CO(g)=NO(g)+CO2(g)分两步进行:
第一步:NO2(g)+NO2(g)→NO3(g)+NO(g) (慢反应)
第二步:NO3(g)+CO(g)→NO(g)+CO2(g) (快反应)
下列表述正确的是
A.反应速率与NO浓度有关 B.反应速率与NO2浓度有关
C.反应的中间产物只有NO3 D.第二步反应活化能较高
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】计算并按要求填空。
(1)已知16g CH4(g)与适量O2(g)反应生成CO2(g)和H2O(l)放出890.3kJ热量,写出该反应对应的热化学方程式___________ ;
(2)已知1gC2H2完全燃烧生成CO2(g)和H2O(l)放出的热量为50.0kJ,写出表示C2H2标准燃烧热的热化学方程式___________ ;
(3)已知拆开1mol H-H键,1mol N-H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为___________ ;
(4)某种优质燃油由甲、乙两种有机物混合而成,甲、乙两种物质含有C、H、O三种元素中的两种或三种。已知甲、乙及CO、H2的燃烧热如下:
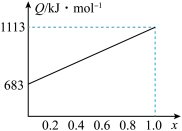
取甲、乙按不同比例混合的燃油23g,在足量的O2中燃烧时,放出的热量Q与混合物中乙的物质的量分数x的关系如图。试求:
(a)乙的相对分子质量为___________ ;
(b)1mol由甲、乙等物质的量混合而成的燃油在一定量的O2中燃烧,放出热量2876kJ•mol-1,则反应中生成CO___________ mol。
(1)已知16g CH4(g)与适量O2(g)反应生成CO2(g)和H2O(l)放出890.3kJ热量,写出该反应对应的热化学方程式
(2)已知1gC2H2完全燃烧生成CO2(g)和H2O(l)放出的热量为50.0kJ,写出表示C2H2标准燃烧热的热化学方程式
(3)已知拆开1mol H-H键,1mol N-H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2(g)与H2(g)反应生成NH3(g)的热化学方程式为
(4)某种优质燃油由甲、乙两种有机物混合而成,甲、乙两种物质含有C、H、O三种元素中的两种或三种。已知甲、乙及CO、H2的燃烧热如下:
| 物质 | 甲 | 乙 | CO | H2 |
| 燃烧热/kJ•mol-1 | 1366 | 5518 | 283 | 286 |

取甲、乙按不同比例混合的燃油23g,在足量的O2中燃烧时,放出的热量Q与混合物中乙的物质的量分数x的关系如图。试求:
(a)乙的相对分子质量为
(b)1mol由甲、乙等物质的量混合而成的燃油在一定量的O2中燃烧,放出热量2876kJ•mol-1,则反应中生成CO
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】回答下列问题:
(1)一氧化碳催化加氢制甲醇,反应原理为:
 。
。
①若已知CO、 、
、 的燃烧热分别为
的燃烧热分别为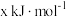 、
、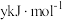 、
、 ,则
,则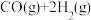


_______ 。
②已知反应中相关的化学键键能数据如下:
且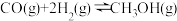
 ,试计算断开
,试计算断开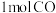 气体中的
气体中的 需提供的最低能量为
需提供的最低能量为_______ 。
(2)燃料的热值是指单位质量某种燃料完全燃烧放出的热量,其常用单位为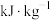 。已知下列物质的燃烧热(25℃、
。已知下列物质的燃烧热(25℃、 ):
):
据上表数据填写:
①试写出表示辛烷燃烧热的热化学方程式_______ 。
② 的热值为
的热值为_______ 。
③上表所列燃料的热值最大的是_______ (填化学式)。
(3)中和热是反应热的一种。
①取 溶液和
溶液和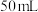 盐酸进行实验,若实验测得的反应前后温度差平均值
盐酸进行实验,若实验测得的反应前后温度差平均值 ,中和后生成溶液的比热容
,中和后生成溶液的比热容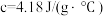 (若近似认为
(若近似认为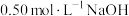 溶液和
溶液和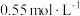 盐酸的密度都是
盐酸的密度都是 )。则生成
)。则生成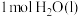 时的反应热
时的反应热
_______ (取小数点后一位,下同)。
②强酸与强碱的稀溶液发生中和反应生成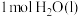 时的反应热
时的反应热 。若用一定浓度的稀硫酸与含
。若用一定浓度的稀硫酸与含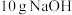 的稀碱溶液完全反应,反应放出的热量为
的稀碱溶液完全反应,反应放出的热量为_______ 。
(1)一氧化碳催化加氢制甲醇,反应原理为:

 。
。①若已知CO、
 、
、 的燃烧热分别为
的燃烧热分别为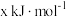 、
、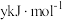 、
、 ,则
,则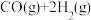


②已知反应中相关的化学键键能数据如下:
| 化学键 |  |  | 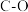 |  |
 | 436 | 413 | 343 | 465 |
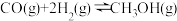
 ,试计算断开
,试计算断开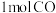 气体中的
气体中的 需提供的最低能量为
需提供的最低能量为(2)燃料的热值是指单位质量某种燃料完全燃烧放出的热量,其常用单位为
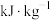 。已知下列物质的燃烧热(25℃、
。已知下列物质的燃烧热(25℃、 ):
):| 燃料 |  |  |  | 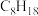 (辛烷) (辛烷) |
燃烧热/( ) ) | 285.8 | 283.0 | 890.3 | 5518 |
①试写出表示辛烷燃烧热的热化学方程式
②
 的热值为
的热值为③上表所列燃料的热值最大的是
(3)中和热是反应热的一种。
①取
 溶液和
溶液和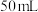 盐酸进行实验,若实验测得的反应前后温度差平均值
盐酸进行实验,若实验测得的反应前后温度差平均值 ,中和后生成溶液的比热容
,中和后生成溶液的比热容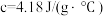 (若近似认为
(若近似认为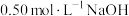 溶液和
溶液和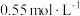 盐酸的密度都是
盐酸的密度都是 )。则生成
)。则生成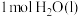 时的反应热
时的反应热
②强酸与强碱的稀溶液发生中和反应生成
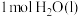 时的反应热
时的反应热 。若用一定浓度的稀硫酸与含
。若用一定浓度的稀硫酸与含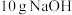 的稀碱溶液完全反应,反应放出的热量为
的稀碱溶液完全反应,反应放出的热量为
您最近一年使用:0次



