某无色透明溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种离子,每种离子的物质的量浓度均为
中的若干种离子,每种离子的物质的量浓度均为 。现将某小组对该溶液进行的实验及现象描述如下:
。现将某小组对该溶液进行的实验及现象描述如下:
①向溶液中加入过量 溶液,发现生成无色无味气体和溶液甲;
溶液,发现生成无色无味气体和溶液甲;
②向溶液甲中加大过量 溶液,生成大量白色沉淀和溶液乙;
溶液,生成大量白色沉淀和溶液乙;
③向过滤所得的白色沉淀上滴入过量稀盐酸,发现沉淀部分溶解并生成无色无味能使澄清石灰水变浑浊的气体。
则下列说法不正确的是
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种离子,每种离子的物质的量浓度均为
中的若干种离子,每种离子的物质的量浓度均为 。现将某小组对该溶液进行的实验及现象描述如下:
。现将某小组对该溶液进行的实验及现象描述如下:①向溶液中加入过量
 溶液,发现生成无色无味气体和溶液甲;
溶液,发现生成无色无味气体和溶液甲;②向溶液甲中加大过量
 溶液,生成大量白色沉淀和溶液乙;
溶液,生成大量白色沉淀和溶液乙;③向过滤所得的白色沉淀上滴入过量稀盐酸,发现沉淀部分溶解并生成无色无味能使澄清石灰水变浑浊的气体。
则下列说法不正确的是
A.原溶液中一定有 |
B.原溶液中可能有 |
C.原溶液中可能有 |
D.向溶液甲中加入过量盐酸酸化后,再滴入少量 溶液,会出现白色沉淀 溶液,会出现白色沉淀 |
更新时间:2024-03-02 16:12:18
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,下列各组离子在指定溶液中能大量共存的是
| A.无色透明的溶液中:Fe3+、Mg2+、SO42-、Cl- |
| B.使酚酞变红的溶液中:K+、Na +、CO32-、NO3- |
| C.c(Fe2+ ) =1 mol·L-1的溶液中:K+、 H+、MnO4-、SO42- |
| D.能使紫色石蕊变红的溶液中:Na+、 NH4+、SO42-、HCO3- |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列各组离子可以在酸性溶液中大量共存的是
A.Mg2+、Na+、SO 、Cl- 、Cl- | B.Na+、K+、Cl-、HCO |
C.K+、Ba2+、CO 、SO 、SO | D.K+、Na+、OH-、SO |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的Na2O2物质的量(mol)的关系如图所示,则原溶液中的Mg2+、Al3+、NH4+物质的量分别为( )


| A.2mol、3mol、6mol | B.3mol、3mol、6mol |
| C.2mol、3mol、4mol | D.3mol、2mol、2mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】甲、乙两车间排放出的污水中分别含有大量且不同的4种离子,这些离子是Ag+、Ba2+、Fe3+、Na+、Cl-、NO3-、OH-、SO42-。经检测,甲车间的污水pH>7,则下列判断正确的是
| A.甲车间的污水中可能含有Ba2+ |
| B.乙车间的污水中可能含有Na+ |
| C.甲车间的污水中不可能含有SO42- |
| D.乙车间的污水中一定含有Fe3+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO 、NO
、NO 、Cl⁻中的4种离子(忽略水的电离),所含离子的物质的量均为 1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变。下列说法错误的是
、Cl⁻中的4种离子(忽略水的电离),所含离子的物质的量均为 1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变。下列说法错误的是
 、NO
、NO 、Cl⁻中的4种离子(忽略水的电离),所含离子的物质的量均为 1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变。下列说法错误的是
、Cl⁻中的4种离子(忽略水的电离),所含离子的物质的量均为 1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变。下列说法错误的是| A.该溶液中一定有Na⁺ |
| B.若向该溶液中逐渐加入 NaOH溶液,先生成沉淀,后沉淀部分溶解 |
C.加入稀硫酸发生反应的离子方程式为: 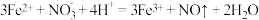 |
| D.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为 80g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验方案、现象、得出的结论均正确的是
| 选项 | 实验及现象 | 结论 |
| A | 用玻璃棒蘸取某样品进行焰色反应时观察到黄色火焰 | 该样品含钠元素 |
| B | 向NaHCO3溶液中加入过量盐酸振荡、静置、有气泡产生 | 证明非金属性Cl>C |
| C | 将10mL2mol/L的KI溶液与1mL1mol/LFeCl3溶液混合充分反应后滴加KSCN,溶液颜色变红 | KI与FeCl3反应有可逆性 |
| D | 向酸化的KMnO4溶液通入SO2,向反应后的溶液中加入BaCl2产生白色沉淀 | 证明SO2被氧化为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述正确的是( )
| A.在过滤和配制一定物质的量浓度的溶液中的玻璃棒作用完全相同 |
| B.可用冷却热饱和溶液的方法除去NaCl的少量杂质KNO3 |
| C.在某溶液中先加入氯化钡,产生白色沉淀,然后再加入稀盐酸,沉淀不溶解,证明有SO42-存在 |
| D.除去粗盐中的SO42﹣、Ca2+、Mg2+等杂质,加入的药品顺序为:BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】亚硫酸氢铵(NH4HSO3)可用作防腐剂、还原剂,也用于制造二氧化硫、保险粉等,某化学兴趣小组设计如图装置(加热和夹持装置已省略)制备亚硫酸氢铵,回答下列问题:
(1)实验开始时,先关闭K1,打开K2,戊装置的试管内反应的化学方程式为___________ 。
(2)一段时间后,关闭K2,打开K1,甲装置圆底烧瓶内发生反应的化学方程式为___________ ;先打开K2后打开K1的原因可能是___________ ;丙装置的作用是 ___________ ;丁装置用于吸收多余的SO2,则丁装置中的试剂为 ___________ (填字母)。
a.无水CaCl2
b.碱石灰
c.P2O5
d.浓硫酸
(3)亚硫酸氢铵有较强的还原性,设计实验检验制备的亚硫酸氢铵样品是否被氧化:___________ (填操作、现象及相应的结论,可供选择的试剂:水、稀盐酸、稀硝酸、氯化钡溶液、硝酸银溶液)。

(1)实验开始时,先关闭K1,打开K2,戊装置的试管内反应的化学方程式为
(2)一段时间后,关闭K2,打开K1,甲装置圆底烧瓶内发生反应的化学方程式为
a.无水CaCl2
b.碱石灰
c.P2O5
d.浓硫酸
(3)亚硫酸氢铵有较强的还原性,设计实验检验制备的亚硫酸氢铵样品是否被氧化:
您最近一年使用:0次



