物质的分类、转化、化学计量在化学中占有重要地位。
(1)以下物质:
①液氯,②HCl气体,③氨水,④熔融Na2SO4,⑤蔗糖,⑥KClO3晶体,⑦SO2,⑧空气。
属于混合物的是___________ (填相应物质前序号,下同);所给状态下能导电的是___________ ;属于电解质的是___________ 。
(2)写出④的电离方程式___________ ,⑥的电离方程式___________ 。
(1)以下物质:
①液氯,②HCl气体,③氨水,④熔融Na2SO4,⑤蔗糖,⑥KClO3晶体,⑦SO2,⑧空气。
属于混合物的是
(2)写出④的电离方程式
更新时间:2024-03-15 16:39:00
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有以下物质:①Cu ②澄清石灰水 ③液氨 ④ 晶体 ⑤液态HCl ⑥
晶体 ⑤液态HCl ⑥ 胶体 ⑦医用酒精 ⑧
胶体 ⑦医用酒精 ⑧ ⑨碳酸钡 ⑩
⑨碳酸钡 ⑩ 。回答下列问题(用相应物质的序号填写):
。回答下列问题(用相应物质的序号填写):
(1)属于电解质的有_______ ,属于非电解质的有_______ 。
(2)写出向⑨中加入⑤的水溶液发生反应的离子方程式_______ 。
(3)写出向②中滴加少量④的水溶液的离子方程式_______ 。
(4)向⑥中逐滴加入⑤的水溶液的现象是_______ ,产生这种现象的原因是_______ 。(请以文字结合离子方程式回答)
 晶体 ⑤液态HCl ⑥
晶体 ⑤液态HCl ⑥ 胶体 ⑦医用酒精 ⑧
胶体 ⑦医用酒精 ⑧ ⑨碳酸钡 ⑩
⑨碳酸钡 ⑩ 。回答下列问题(用相应物质的序号填写):
。回答下列问题(用相应物质的序号填写):(1)属于电解质的有
(2)写出向⑨中加入⑤的水溶液发生反应的离子方程式
(3)写出向②中滴加少量④的水溶液的离子方程式
(4)向⑥中逐滴加入⑤的水溶液的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】I.现有9种物质:①Na;②盐酸;③ ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦ 胶体;⑧Na2O2;⑨CO
胶体;⑧Na2O2;⑨CO
(1)属于电解质的是_______ (用序号填空,下同);属于酸性氧化物的是_______ 。
(2)实验室中少量①通常保存在_____ 中;④在工业上大量用于_____ (写出一种用途即可)。
(3)⑧与⑥反应的化学方程式_______
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式_______ 。
Ⅱ.某种飞船以联氨 和
和 为动力源,发生反应:
为动力源,发生反应: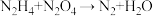 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。
(5)①配平该方程式_______ 。
②该反应中,氧化产物与还原产物的质量之比为_______ 。
 ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦ 胶体;⑧Na2O2;⑨CO
胶体;⑧Na2O2;⑨CO(1)属于电解质的是
(2)实验室中少量①通常保存在
(3)⑧与⑥反应的化学方程式
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式
Ⅱ.某种飞船以联氨
 和
和 为动力源,发生反应:
为动力源,发生反应: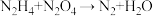 ,反应温度可高达
,反应温度可高达 ,回答下列问题。
,回答下列问题。(5)①配平该方程式
②该反应中,氧化产物与还原产物的质量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有下列10种物质①熔融的氢氧化钠 ②蔗糖 ③纯净的盐酸 ④金属钠 ⑤硫酸 ⑥二氧化硫 ⑦硫粉 ⑧胆矾 ⑨酒精溶液 ⑩液氮
(1)①属于电解质的有_______
②属于非电解质的有_______
(2)完成以下计算
①等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2物质的量之比为___
②配置100mL1mol⋅L−1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g⋅mL−1,质量分数为98%)的体积为___ mL.
(1)①属于电解质的有
②属于非电解质的有
(2)完成以下计算
①等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2物质的量之比为
②配置100mL1mol⋅L−1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g⋅mL−1,质量分数为98%)的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】借助现代科技手段研究化学反应原理能加深对知识本质的理解。
(1)下图是电解质导电性测试实验装置, 的电离方程式为
的电离方程式为___________ ,接通电源后,灯泡不亮,本质原因是___________ ,要使灯泡发光,可采取的操作是___________ ;将少量 溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是
溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是___________ 。

(2)下图是一套验证气体性质的实验装置,回答下列问题:
①实验室可用二氧化锰与浓盐酸制备氯气,反应的离子方程式为___________ ,如图所示,在A处通入干燥的氯气。一段时间后,观察到C处红布条褪色,则B处的开关应该处于___________ (填“关闭”或“打开”)状态。
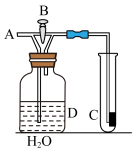
②实验后,利用数字传感器对D中的有色溶液进行光照实验分析,溶液光照实验前后比较,数目增加的离子有___________ (填化学式),对光照后溶液的叙述错误的是___________ (填标号)。
a.颜色变浅 b.漂白性增强 c.酸性增强 d.氧化性减弱
(1)下图是电解质导电性测试实验装置,
 的电离方程式为
的电离方程式为 溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是
溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是
(2)下图是一套验证气体性质的实验装置,回答下列问题:
①实验室可用二氧化锰与浓盐酸制备氯气,反应的离子方程式为

②实验后,利用数字传感器对D中的有色溶液进行光照实验分析,溶液光照实验前后比较,数目增加的离子有
a.颜色变浅 b.漂白性增强 c.酸性增强 d.氧化性减弱
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求填空:①CaCO3②液态HCl ③熔融NaCl ④盐酸 ⑤Na3PO4固体⑥铜丝⑦NaOH溶液⑧稀硫酸⑨液氨
(1)上述状态下可导电的是_______ 。
(2)属于强电解质的是_______ 。
II.写出下列物质在水溶液中或熔融状态下的电离方程式
(3)NaHSO4(熔融):_______
(4)NaHCO3:_______
(5)KAl(SO4)2:_______
(6)H2SO3_______ 。
III.请按题目要求完成相应问题:
(7)已知Mn2O7属于酸性氧化物,写出其与强碱反应的离子方程式_______ 。
(8)用醋酸除水垢(碳酸钙)反应的离子方程式_______ 。
(9)Fe(OH)3胶体制备的离子方程式_______ 。
(10)足量的CO2通入澄清石灰水的离子方程式_______ 。
(1)上述状态下可导电的是
(2)属于强电解质的是
II.写出下列物质在水溶液中或熔融状态下的电离方程式
(3)NaHSO4(熔融):
(4)NaHCO3:
(5)KAl(SO4)2:
(6)H2SO3
III.请按题目要求完成相应问题:
(7)已知Mn2O7属于酸性氧化物,写出其与强碱反应的离子方程式
(8)用醋酸除水垢(碳酸钙)反应的离子方程式
(9)Fe(OH)3胶体制备的离子方程式
(10)足量的CO2通入澄清石灰水的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】今有10种物质:①Na ②稀硝酸 ③纯醋酸 ④NH3 ⑤空气 ⑥CO2 ⑦Fe(OH)3胶体 ⑧NaCl晶体 ⑨BaCO3 ⑩碘酒
(1)能导电的物质______ ;(用序号填空,下同)
(2)电解质,但熔融状态下并不导电______ .
(3)强电解质_______ ;
(4)非电解质_______ ;
(5)区分Fe(OH)3胶体和FeCl3溶液实验方法______ ;
(6)实验室中①通常保存在_______ 中;
(7)写出②和⑨反应的离子方程式_______ .
(8)向Fe(OH)3胶体中逐滴滴入过量的盐酸,会出现一系列变化:先出现___________ ,原因:________ ,随后________ ,原因________ (用离子方程式表示)。
(1)能导电的物质
(2)电解质,但熔融状态下并不导电
(3)强电解质
(4)非电解质
(5)区分Fe(OH)3胶体和FeCl3溶液实验方法
(6)实验室中①通常保存在
(7)写出②和⑨反应的离子方程式
(8)向Fe(OH)3胶体中逐滴滴入过量的盐酸,会出现一系列变化:先出现
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有下列物质:①金刚石、②铜、③ 、④干冰、⑤液氯、⑥
、④干冰、⑤液氯、⑥ 粉末、⑦稀硫酸、⑧
粉末、⑦稀硫酸、⑧ 胶体、⑨
胶体、⑨ 固体⑩乙醇。回答下列问题:
固体⑩乙醇。回答下列问题:
(1)属于电解质的是_______ (填序号,下同),属于非电解质的是_______ 。
(2)属于混合物的是_______ 。
(3)写出⑨在水中的电离方程式:_______ 。
(4) 胶体中分散质粒子直径的范围是
胶体中分散质粒子直径的范围是_______ ,用激光笔照射,可以从侧面看到一条光路,这个现象被称为_______ 。
 、④干冰、⑤液氯、⑥
、④干冰、⑤液氯、⑥ 粉末、⑦稀硫酸、⑧
粉末、⑦稀硫酸、⑧ 胶体、⑨
胶体、⑨ 固体⑩乙醇。回答下列问题:
固体⑩乙醇。回答下列问题:(1)属于电解质的是
(2)属于混合物的是
(3)写出⑨在水中的电离方程式:
(4)
 胶体中分散质粒子直径的范围是
胶体中分散质粒子直径的范围是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学来源于生活又服务于生活,请用化学用语回答下列问题:
(1)漂粉精中有效成分的化学式为:_______ 。
(2)“硅材料”是无机非金属材料的主角,其中广泛应用于光导纤维的材料是:_______ 。
(3)向浑浊的水中加入明矾后,水可得到净化。写出明矾在水中的电离方程式:_______ 。往明矾溶液中逐滴加入Ba(OH)2溶液,若使 恰好完全沉淀,发生反应的离子方程式为:
恰好完全沉淀,发生反应的离子方程式为:_______ ;若使Al3+恰好完全沉淀,发生反应的离子方程式为:_______ 。
(4)饮用水中的 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,反应中若生成标准状况下3.36LN2,则转移的电子数目为:
还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,反应中若生成标准状况下3.36LN2,则转移的电子数目为:_______ 。
(1)漂粉精中有效成分的化学式为:
(2)“硅材料”是无机非金属材料的主角,其中广泛应用于光导纤维的材料是:
(3)向浑浊的水中加入明矾后,水可得到净化。写出明矾在水中的电离方程式:
 恰好完全沉淀,发生反应的离子方程式为:
恰好完全沉淀,发生反应的离子方程式为:(4)饮用水中的
 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,反应中若生成标准状况下3.36LN2,则转移的电子数目为:
还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O,反应中若生成标准状况下3.36LN2,则转移的电子数目为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】生活离不开化学。家庭厨卫中有许多中学化学常见的物质,下列物质括号内为厨卫物品的主要成分:①食盐 ;②料酒(乙醇);③食醋(乙酸);④碱面
;②料酒(乙醇);③食醋(乙酸);④碱面 ;⑤发酵粉(
;⑤发酵粉( 和酒石酸);⑥“84”消毒液
和酒石酸);⑥“84”消毒液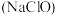 ;⑦洁厕灵
;⑦洁厕灵 。回答下列问题:
。回答下列问题:
(1)写出 在水中的电离方程式:
在水中的电离方程式:_______ 。
(2)当食盐不慎洒落在天然气的火焰上,观察到的现象是_______ 。
(3)②③的主要成分可以归为一类物质,其分类的依据是_______ (填标号)。
A.两种物质都是电解质
B.两种物质都是含碳化合物
C.两种物质都是氧化物
(4)⑥和⑦不能混合使用的原因是_______ (用离子方程式表示)。
(5)用面粉制作馒头的发酵过程中会产生有机酸(一种弱酸),导致口感变差,若在蒸馒头前加入适量④,可使蒸好的馒头松软可口无酸味,用化学方程式解释④的作用:_______ (设有机酸化学式为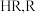 表示有机酸根)。
表示有机酸根)。
(6)欲用 固体配制
固体配制 质量分数为25%、密度为
质量分数为25%、密度为 的“84”消毒液。
的“84”消毒液。
①用电子天平(精确度为 )称量
)称量 的质量为
的质量为_______ g,若配制过程中发现液面超过了刻度线,处理方法为_______ 。
②该“84”消毒液的物质的量浓度约为_______  (保留小数点后一位)。
(保留小数点后一位)。
 ;②料酒(乙醇);③食醋(乙酸);④碱面
;②料酒(乙醇);③食醋(乙酸);④碱面 ;⑤发酵粉(
;⑤发酵粉( 和酒石酸);⑥“84”消毒液
和酒石酸);⑥“84”消毒液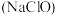 ;⑦洁厕灵
;⑦洁厕灵 。回答下列问题:
。回答下列问题:(1)写出
 在水中的电离方程式:
在水中的电离方程式:(2)当食盐不慎洒落在天然气的火焰上,观察到的现象是
(3)②③的主要成分可以归为一类物质,其分类的依据是
A.两种物质都是电解质
B.两种物质都是含碳化合物
C.两种物质都是氧化物
(4)⑥和⑦不能混合使用的原因是
(5)用面粉制作馒头的发酵过程中会产生有机酸(一种弱酸),导致口感变差,若在蒸馒头前加入适量④,可使蒸好的馒头松软可口无酸味,用化学方程式解释④的作用:
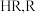 表示有机酸根)。
表示有机酸根)。(6)欲用
 固体配制
固体配制 质量分数为25%、密度为
质量分数为25%、密度为 的“84”消毒液。
的“84”消毒液。①用电子天平(精确度为
 )称量
)称量 的质量为
的质量为②该“84”消毒液的物质的量浓度约为
 (保留小数点后一位)。
(保留小数点后一位)。
您最近一年使用:0次



