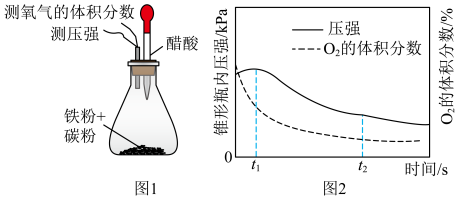
按图1进行实验,测得锥形瓶内气压和空气中氧气的体积分数随时间变化如图2所示。t1~t2之间主要发生_______ (填“吸氧”或“析氢”)腐蚀,其正极反应式为_______ 。
更新时间:2024-05-11 14:39:45
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)电化腐蚀是钢铁发生腐蚀的主要原因,当水膜氢离子浓度较小时,主要发生吸氧腐蚀,其负极反应式为___________ ,正极反应式为___________ 。
(2)将氯化铁溶液蒸干灼烧得到的固体物质是___________ ;(填化学式,下同)将硫酸铝溶液蒸干得到的固体物质是___________ 。
(3)除CaSO4水垢的方法,热的纯碱溶液洗涤再用盐酸洗涤效果更好的原理是___________ ﹔写出反应的化学方程式___________ 、___________ ﹔明矾净水的离子方程式___________ 。
(4)在2 mL 0. 1 mol/L的NaCl溶液中,加入 2 mL 0.1 mol/L的AgNO3溶液,可观察到___________ ,此反应的离子方程式为___________ 。将此混合液过滤,滤渣加入2 mL 0.1 mol/L的KI溶液,搅拌,可观察到___________ ,反应的离子方程式为___________ 。
(5)对于Ag2S(s) 2Ag+(aq)+S2-(aq),其 Ksp的表达式为
2Ag+(aq)+S2-(aq),其 Ksp的表达式为___________ 。
(2)将氯化铁溶液蒸干灼烧得到的固体物质是
(3)除CaSO4水垢的方法,热的纯碱溶液洗涤再用盐酸洗涤效果更好的原理是
(4)在2 mL 0. 1 mol/L的NaCl溶液中,加入 2 mL 0.1 mol/L的AgNO3溶液,可观察到
(5)对于Ag2S(s)
 2Ag+(aq)+S2-(aq),其 Ksp的表达式为
2Ag+(aq)+S2-(aq),其 Ksp的表达式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】钢铁腐蚀现象在生产、生活中普遍存在,也是科学研究的关注点之一
(1)碳钢管发生电化学腐蚀是因为形成了原电池,其负极的电极反应式为_______ 。
(2)外加电流的阴极保护法是防止钢铁腐蚀的常用方法之一,该方法中,需将被保护的碳钢管与直流电源的_______ (填“正极”或“负极”)相连。
(3)在铁制品表面镀锌可防止铁制品被腐蚀,镀锌层即使局部破损,仍可防止破损部位被腐蚀,原因是_______ 。
(4)研究人员就大气环境对碳钢腐蚀的影响进行了研究。其中,A、B两个城市的气候环境和碳钢腐蚀速率数据如下:
①研究人员认为,A、B两城市中碳钢同时发生吸氧腐蚀和析氢腐蚀。碳钢发生析氢腐蚀时,正极的电极反应式为_______ 。
②结合化学用语解释A、B两城市中碳钢能发生析氢腐蚀的原因:_______ 。
③用电化学原理分析B城市碳钢腐蚀速率高于A城市的主要原因:_______ 。
(1)碳钢管发生电化学腐蚀是因为形成了原电池,其负极的电极反应式为
(2)外加电流的阴极保护法是防止钢铁腐蚀的常用方法之一,该方法中,需将被保护的碳钢管与直流电源的
(3)在铁制品表面镀锌可防止铁制品被腐蚀,镀锌层即使局部破损,仍可防止破损部位被腐蚀,原因是
(4)研究人员就大气环境对碳钢腐蚀的影响进行了研究。其中,A、B两个城市的气候环境和碳钢腐蚀速率数据如下:
| 城市 | 年均温度℃ | 年均湿度% |  的浓度( 的浓度(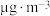 ) ) | 大气 沉积速率( 沉积速率( ) ) | 腐蚀速率(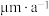 ) ) |
| A | 17.0 | 76 | 61 | 29 | 58 |
| B | 12.3 | 72 | 54 | 420 | 79 |
②结合化学用语解释A、B两城市中碳钢能发生析氢腐蚀的原因:
③用电化学原理分析B城市碳钢腐蚀速率高于A城市的主要原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】如图装置中,小试管内为红墨水,具支试管内盛有pH=4久置的雨水和生铁片。实验时观察到:开始时导管内液面下降,一段时间后导管内液面回升,略高于小试管内液面。
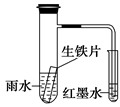
(1)开始时,生铁发生_____ 腐蚀,负极反应式为______ 。
(2)一段时间后,生铁发生______ 腐蚀,正极反应式为______ ,具支试管内雨水的pH的变化情况为_____ ,最后生铁片表面形成红棕色铁锈(Fe2O3•xH2O),那么后期溶液中发生的反应方程式有______ 、2Fe(OH)3=Fe2O3•xH2O+(3-x)H2O。

(1)开始时,生铁发生
(2)一段时间后,生铁发生
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】如图所示为某研究性学习小组探究金属腐蚀条件的实验装置图,试分析实验并回答下列问题:
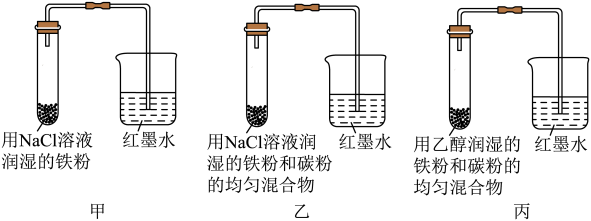
(1)起始时若甲、乙、丙三套装置的导管中液面高度相同,则过一段时间后导管中液面最高的是_____ (填装置代号).
(2)通过甲、乙装置的对比实验说明,钢铁中碳的含量越_____ (填“高”或“低”)越容易被腐蚀.
(3)乙装置中发生电化学腐蚀时正极的电极反应式为_____ .
(4)为防止铁的锈蚀,工业上普遍采用的方法是_____ (写出一点即可).

(1)起始时若甲、乙、丙三套装置的导管中液面高度相同,则过一段时间后导管中液面最高的是
(2)通过甲、乙装置的对比实验说明,钢铁中碳的含量越
(3)乙装置中发生电化学腐蚀时正极的电极反应式为
(4)为防止铁的锈蚀,工业上普遍采用的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】如图所示,甲、乙两试管中各放一枚铁钉,甲试管中装有 溶液,乙试管中装有
溶液,乙试管中装有 溶液。
溶液。
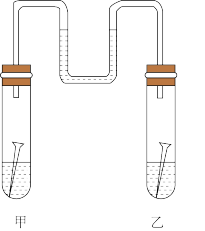
(1)数天后可观察到导管中出现的现象是_______________________________________________________ 。
(2)甲中正极的电极反应式为__________________ ,乙中正极的电极反应式为_________________________ 。
(3)试管中残留气体平均相对分子质量的变化:甲________ (填“增大”“减小”或“不变”,下同),乙________ 。
 溶液,乙试管中装有
溶液,乙试管中装有 溶液。
溶液。
(1)数天后可观察到导管中出现的现象是
(2)甲中正极的电极反应式为
(3)试管中残留气体平均相对分子质量的变化:甲
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀________________ 。
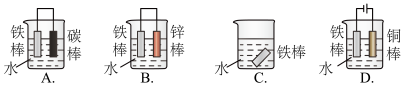
(2)某学生在A、B、C、D四只小烧瓶中分别放入:干燥的细铁丝;浸过食盐水的细铁丝;浸过清水的细铁丝;食盐水及细铁丝,并使铁丝完全浸没在食盐水中。然后装配成如图所示的四套装置,每隔一段时间测量导管中水面上升的高度,结果如下表所示(表中所列数据为导管中水面上升的高度/cm)

不同时间水面上升的高度
①上述实验中,铁生锈的速率由大到小的排列顺序为(填小烧瓶号):_______ 。
②实验中的铁生锈属于电化学腐蚀的__________ (填腐蚀类型)。
③写出铁腐蚀正极的电极反应式:________________________________
④镀铜可防止铁制品腐蚀,电镀时用_______ 作阳极.
⑤利用图装置,可以模拟铁的电化学防护。
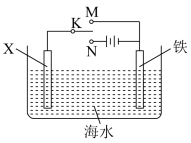
若X为碳棒,为减缓铁的腐蚀,开关K应置于___________________ 处。若X为锌棒,开关K置于M处,该电化学防护法称为______________
⑥2Cu+O2+ 2H2SO4 =2CuSO4 + 2H2O反应中Cu被腐蚀,若将该反应设计为原电池,其正极电极反应式为____________________ 。
(1)下列哪个装置可防止铁棒被腐蚀

(2)某学生在A、B、C、D四只小烧瓶中分别放入:干燥的细铁丝;浸过食盐水的细铁丝;浸过清水的细铁丝;食盐水及细铁丝,并使铁丝完全浸没在食盐水中。然后装配成如图所示的四套装置,每隔一段时间测量导管中水面上升的高度,结果如下表所示(表中所列数据为导管中水面上升的高度/cm)

不同时间水面上升的高度
| 时间/小时 | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A瓶(盛干燥铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| B瓶(盛沾了食盐水的铁丝) | 0 | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 |
| C瓶(盛沾了清水的铁丝) | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
| D瓶(盛完全浸没在食盐水中的铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
②实验中的铁生锈属于电化学腐蚀的
③写出铁腐蚀正极的电极反应式:
④镀铜可防止铁制品腐蚀,电镀时用
⑤利用图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于
⑥2Cu+O2+ 2H2SO4 =2CuSO4 + 2H2O反应中Cu被腐蚀,若将该反应设计为原电池,其正极电极反应式为
您最近一年使用:0次



