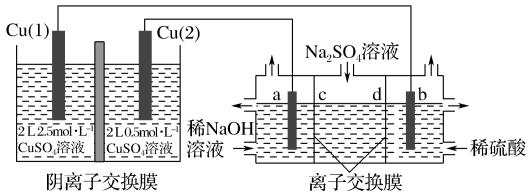
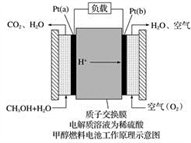
科学家预言,燃料电池将是21世纪获得电能的重要途径。近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下:
请回答下列问题:
(1)Pt(a)电极是电池的________ 极,电极反应式为__________________ ;Pt(b)电极发生________ (填“氧化”或“还原”)反应,电极反应式为___________ 。
(2)电池的总反应方程式为____________________ 。
(3)如果该电池工作时电路中通过2 mol电子,则消耗的CH3OH有______ mol。

请回答下列问题:
(1)Pt(a)电极是电池的
(2)电池的总反应方程式为
(3)如果该电池工作时电路中通过2 mol电子,则消耗的CH3OH有
更新时间:2015-02-10 16:22:42
|
【知识点】 化学电源
相似题推荐
填空题
|
适中
(0.65)
【推荐1】Ⅰ.燃料电池一般指采用 、
、 等可燃物质与
等可燃物质与 一起构成的电池装置。它可直接将化学能转化为电能,甲烷电池以KOH溶液为电解质,其总反应的化学方程式为
一起构成的电池装置。它可直接将化学能转化为电能,甲烷电池以KOH溶液为电解质,其总反应的化学方程式为 。
。
(1)负极上的电极反应为___________ 。
(2)消耗5.6L(标准状况下) 时,有
时,有___________ mol电子发生转移。
(3)开始放电时,正极附近溶液的氢氧根离子浓度___________ (填“增大”、“减小”或“不变”)。
Ⅱ.钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。利用如图装置,可以模拟铁的电化学防护。
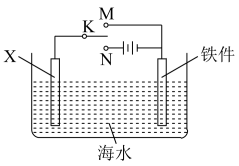
(4)①若X为碳棒,为减缓铁件的腐蚀,开关K应置于___________ 处。(填M或N)
②若X为锌,开关K置于M处,该电化学防护法称为___________ 。
 、
、 等可燃物质与
等可燃物质与 一起构成的电池装置。它可直接将化学能转化为电能,甲烷电池以KOH溶液为电解质,其总反应的化学方程式为
一起构成的电池装置。它可直接将化学能转化为电能,甲烷电池以KOH溶液为电解质,其总反应的化学方程式为 。
。(1)负极上的电极反应为
(2)消耗5.6L(标准状况下)
 时,有
时,有(3)开始放电时,正极附近溶液的氢氧根离子浓度
Ⅱ.钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。利用如图装置,可以模拟铁的电化学防护。

(4)①若X为碳棒,为减缓铁件的腐蚀,开关K应置于
②若X为锌,开关K置于M处,该电化学防护法称为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、空间电视转播站、飞机、轮船、电脑、收音机、照相机、电子手表、心脏起搏器等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染。请根据题中提供的信息,回答下列问题:
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为____ ,当线路中转移0.1mol电子时,则被腐蚀铜的质量为____ g。
(2)蓄电池在放电时起原电池作用,在充电时起电解池的作用。铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。则正极电极反应式为____ 。
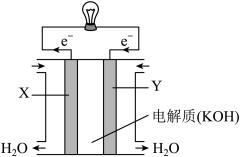
(3)如图为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH。则X极为电池的____ (填“正”或“负”)极,X极的电极反应方程式为 ____ 。
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为
(2)蓄电池在放电时起原电池作用,在充电时起电解池的作用。铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。则正极电极反应式为
(3)如图为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH。则X极为电池的

您最近一年使用:0次