已知A2+、B+、C3-、D- 是第三周期元素的四种离子。下列叙述中正确的是
| A.四种离子都具有相同的电子层结构 |
| B.原子半径:r(D)> r(C)> r(A)> r(B) |
| C.离子半径:r(B+)> r(A2+)> r(C3-)> r(D-) |
| D.B、D两元素的最高价氧化物的水化物在溶液中反应的离子方程式可表示为H++OH-=H2O |
更新时间:2016-12-09 08:09:50
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W为原子序数依次增大的短周期主族元素,X与Y同族;科学家在核反应中用中子(即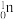 )轰击
)轰击 ,得到核素
,得到核素 和
和 ,即
,即 。下列说法错误的是
。下列说法错误的是
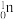 )轰击
)轰击 ,得到核素
,得到核素 和
和 ,即
,即 。下列说法错误的是
。下列说法错误的是| A.4种元素中W的非金属性最强 | B.原子半径: |
| C.Y与X、W均可形成离子化合物 | D.W的氢化物的沸点一定高于Z的氢化物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】六种短周期主族元素A、B、C、D、E、F的原子序数依次增大,A和D同主族,C和F同主族。B、C、D、E的离子均具有相同的电子层结构,E在同周期元素中离子半径最小。A和B、C、F均能形成共价化合物,A和B形成的化合物Y在水中呈碱性,D和F形成的化合物在水中呈中性。下列说法错误的是
| A.简单离子半径:B > D |
| B.简单氢化物水溶液酸性:F > C > B |
| C.D的单质能将E单质从EF3的溶液中置换出来 |
| D.化合物AF与化合物Y可反应生成含有共价键的离子化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知a、b、c、d、e是原子序数依次增大的短周期元素,其中a的一种核素常用来鉴定文物;c元素所组成的单质和氢化物中各有一种可以用来做消毒剂和漂白剂;d元素的简单离子半径是第三周期中最小的;e的最外层电子数是最内层电子数的3倍。下列判断正确的是
| A.a、b、c三种元素分别形成的单质均只有一种 |
| B.d的氧化物能溶于过量氨水 |
| C.e在过量的氧气中燃烧得到eO3 |
| D.a、b、d、e的单质都能与c的单质发生氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知:X元素的气态氢化物分子式为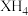 ,其中X元素的质量分数为
,其中X元素的质量分数为 。Y原子的内层电子总数是其最外层电子数的2.5倍。Z元素原子的外围电子排布为
。Y原子的内层电子总数是其最外层电子数的2.5倍。Z元素原子的外围电子排布为 。W元素原子的未成对电子数在前四周期中最多。下列有关说法中错误的是
。W元素原子的未成对电子数在前四周期中最多。下列有关说法中错误的是
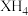 ,其中X元素的质量分数为
,其中X元素的质量分数为 。Y原子的内层电子总数是其最外层电子数的2.5倍。Z元素原子的外围电子排布为
。Y原子的内层电子总数是其最外层电子数的2.5倍。Z元素原子的外围电子排布为 。W元素原子的未成对电子数在前四周期中最多。下列有关说法中错误的是
。W元素原子的未成对电子数在前四周期中最多。下列有关说法中错误的是A.可燃冰的主要成分是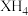 的水合物,过度开采容易造成温室效应 的水合物,过度开采容易造成温室效应 |
| B.X与Y形成化合物时,X呈正价 |
C.W元素的价电子排布式为 |
D.四种元素的最高化合价: |
您最近一年使用:0次