I.肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。 已知在25℃、l0lkPA时,16gN2H4在氧气中完全燃烧生成氮气和H2O,放出热量312kJ。
(1)该条件下,N2H4完全燃烧的热化学方程式为______________
(2)传统制备肼的方法是以NAClO氧化NH3,制得肼的稀溶液,该反应的方程式为______________
II.钢铁工业是国家工业的基础。请回答钢铁腐蚀、防护过程中的有关问题。
(1)铁在潮湿的空气中容易被腐蚀,写出铁发生电化学腐蚀时,负极的电极反应式______________
(2)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。图中A、B、C、D四个区域,生成铁锈最多的是_______ (填字母)
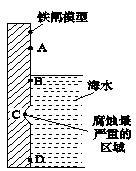
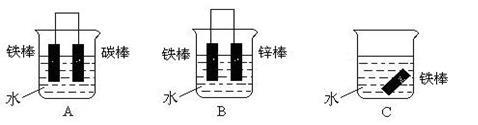
(3)下列各个装置中铁棒被腐蚀由难到易的顺序是______ (填字母)
(1)该条件下,N2H4完全燃烧的热化学方程式为
(2)传统制备肼的方法是以NAClO氧化NH3,制得肼的稀溶液,该反应的方程式为
II.钢铁工业是国家工业的基础。请回答钢铁腐蚀、防护过程中的有关问题。
(1)铁在潮湿的空气中容易被腐蚀,写出铁发生电化学腐蚀时,负极的电极反应式
(2)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。图中A、B、C、D四个区域,生成铁锈最多的是

(3)下列各个装置中铁棒被腐蚀由难到易的顺序是

更新时间:2016-12-09 08:15:33
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】化学反应可视为旧键断裂和新化学键形成的过程。化学键的键能是两个原子间形成1 mol化学键时释放的能量或断开1 mol化学键所吸收的能量。
现提供以下化学键的键能:(kJ·mol−1)P—P:198 P—O:360 O==O:498 P==O:585。
则P4(白磷)+5O2 P4O10是
P4O10是___ 反应(填“放热”或“吸热”),能量变化为___ kJ。(提示:白磷是正四面体形的分子,如图 ,当与氧形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键结合一个氧原子)
,当与氧形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键结合一个氧原子)
现提供以下化学键的键能:(kJ·mol−1)P—P:198 P—O:360 O==O:498 P==O:585。
则P4(白磷)+5O2
 P4O10是
P4O10是 ,当与氧形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键结合一个氧原子)
,当与氧形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键结合一个氧原子)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学反应在发生物质变化的同时伴随有能量的变化,是人类获取能量的重要途径,而许多能量的利用与化学反应中的能量变化密切相关。
Ⅰ、H2+Cl2=2HCl的反应过程如图所示:
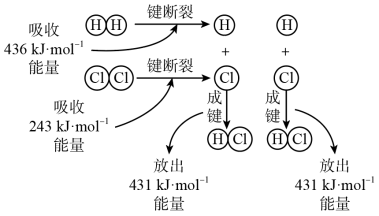
(1)根据如图填写下表:
(2)该反应为___________ 反应(填“放热”或“吸热”)。
Ⅱ、硅是太阳能电池的重要材料。工业冶炼纯硅的原理是:
粗硅冶炼:(a)SiO2+2C Si+2CO↑;
Si+2CO↑;
精炼硅:(b)Si+3HCl SiHCl3+H2;
SiHCl3+H2;
(c)SiHCl3+H2 Si+3HCl
Si+3HCl
化学反应与能量变化如图所示,回答下列问题:

(3)(a)是___________ 反应,(c)是___________ 反应(填“吸热"或“放热”)。
(4)反应(b)破坏反应物中的化学键所吸收的能量___________ (填“大于”或“小于”)形成生成物中化学键所放出的能量。
Ⅲ、为了探究化学反应的热效应,某兴趣小组进行了如图所示实验:
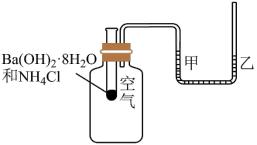
(5)室温下,观察到的现象是___________ ;则该反应是___________ (填“放热”或“吸热”)反应。
Ⅰ、H2+Cl2=2HCl的反应过程如图所示:

(1)根据如图填写下表:
| 化学键 | 断裂或形成1mol化学键时能量变化 | 反应中能量变化 |
| Cl-Cl | 吸收243kJ | 共吸收679kJ |
| H-H | 吸收436kJ | |
| H-Cl | 放出431kJ | 共放出 |
Ⅱ、硅是太阳能电池的重要材料。工业冶炼纯硅的原理是:
粗硅冶炼:(a)SiO2+2C
 Si+2CO↑;
Si+2CO↑;精炼硅:(b)Si+3HCl
 SiHCl3+H2;
SiHCl3+H2;(c)SiHCl3+H2
 Si+3HCl
Si+3HCl化学反应与能量变化如图所示,回答下列问题:

(3)(a)是
(4)反应(b)破坏反应物中的化学键所吸收的能量
Ⅲ、为了探究化学反应的热效应,某兴趣小组进行了如图所示实验:

(5)室温下,观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氢气,二甲醚,乙醇都是极具发展潜力的绿色清洁能源。
Ⅰ.关于氢能,根据要求回答问题:
制备氢气常采用以下方法:①电解水法: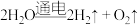
②水煤气法: ,
,
③太阳能光催化分解水法:
(1)三种方法中最节能的是_______ (填标号)。
(2)已知拆开1mol H-H、1mol O=O和1mol H-O分别需要的能量依次为436kJ、498kJ和463kJ,则理论上每 完全分解,需
完全分解,需_______ (填“放出”或“吸收”能量_______ kJ。下列能正确表示该过程的能量变化示意图的是_______ (填标号)。
A.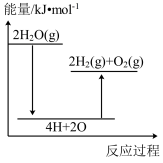 B.
B.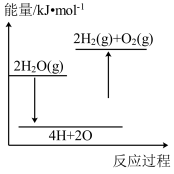
C.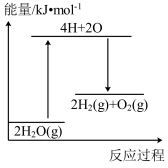 D.
D.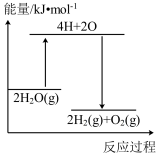
Ⅱ.二甲醚 气体是一种可再生绿色新能源,被誉为“21世纪的清洁燃料”。
气体是一种可再生绿色新能源,被誉为“21世纪的清洁燃料”。
(3)写出二甲醚一种同分异构体的结构简式:_______ 。
(4)工业上可用水煤气合成二甲醚: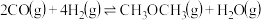
①测得CO和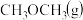 的浓度随时间变化如图所示,则反应开始至平衡时的
的浓度随时间变化如图所示,则反应开始至平衡时的 平均反应速率
平均反应速率
_______ 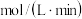 。
。

②若该反应在恒容密闭容器中进行,下列叙述中正确的是_______ 。
A.及时分离出 ,可以加快化学反应速率
,可以加快化学反应速率
B.恒容时,充入He增大压强,化学反应速率不变
C.容器内压强不再变化,说明该反应已达到最大的限度
D. ,说明该反应已达到平衡状态
,说明该反应已达到平衡状态
Ⅰ.关于氢能,根据要求回答问题:
制备氢气常采用以下方法:①电解水法:
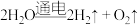
②水煤气法:
 ,
,
③太阳能光催化分解水法:

(1)三种方法中最节能的是
(2)已知拆开1mol H-H、1mol O=O和1mol H-O分别需要的能量依次为436kJ、498kJ和463kJ,则理论上每
 完全分解,需
完全分解,需A.
 B.
B.
C.
 D.
D.
Ⅱ.二甲醚
 气体是一种可再生绿色新能源,被誉为“21世纪的清洁燃料”。
气体是一种可再生绿色新能源,被誉为“21世纪的清洁燃料”。(3)写出二甲醚一种同分异构体的结构简式:
(4)工业上可用水煤气合成二甲醚:
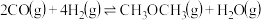
①测得CO和
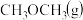 的浓度随时间变化如图所示,则反应开始至平衡时的
的浓度随时间变化如图所示,则反应开始至平衡时的 平均反应速率
平均反应速率
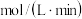 。
。
②若该反应在恒容密闭容器中进行,下列叙述中正确的是
A.及时分离出
 ,可以加快化学反应速率
,可以加快化学反应速率B.恒容时,充入He增大压强,化学反应速率不变
C.容器内压强不再变化,说明该反应已达到最大的限度
D.
 ,说明该反应已达到平衡状态
,说明该反应已达到平衡状态
您最近一年使用:0次
【推荐1】根据下列四种电化学装置图,回答下列问题:
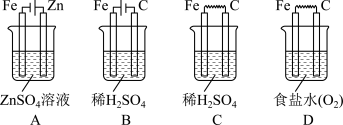
(1)装置名称:A____ 。
(2)装置A中Fe是____ 极;装置B中Fe是____ 极;装置D中Fe是____ 极。
(3)装置B、C相比较,其反应速率的大小关系是___ 。

(1)装置名称:A
(2)装置A中Fe是
(3)装置B、C相比较,其反应速率的大小关系是
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】(1).炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
①铁锅的锈蚀是_______ 腐蚀(填“析氢”或“吸氧”)。
②写出铁锅腐蚀正极的电极反应式:___________________________
(2).①某同学用碳棒,铜棒,稀硫酸和干电池为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑请在右边画出能够实验这一反应的装置图。
__________________

②某同学由于在做铜与稀硫酸的反应实验时操作出现失误,看到碳棒和铜棒上都有气泡产生且铜棒没有被腐蚀。请你分析其原因:_______________________
(3)由氢气和氧气反应生成1 mol水蒸气,放出241.8 kJ热量(25℃、101 kPa下测得)
①写出该反应的热化学方程式:____________________
②若1 mol水蒸气转化为液态水放热44kJ,氢气的燃烧热为_________ kJ/mol。
①铁锅的锈蚀是
②写出铁锅腐蚀正极的电极反应式:
(2).①某同学用碳棒,铜棒,稀硫酸和干电池为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑请在右边画出能够实验这一反应的装置图。

②某同学由于在做铜与稀硫酸的反应实验时操作出现失误,看到碳棒和铜棒上都有气泡产生且铜棒没有被腐蚀。请你分析其原因:
(3)由氢气和氧气反应生成1 mol水蒸气,放出241.8 kJ热量(25℃、101 kPa下测得)
①写出该反应的热化学方程式:
②若1 mol水蒸气转化为液态水放热44kJ,氢气的燃烧热为
您最近一年使用:0次

 的过程可描述为
的过程可描述为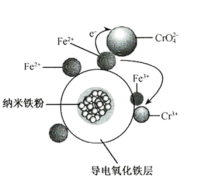 。
。


