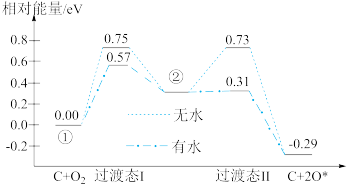
某可逆反应的△H=+146kJ/mol,下列关于该反应的叙述正确的是
| A.正反应的活化能比逆反应的活化能大146kJ/mol |
| B.正反应的活化能一定小于146kJ/mol |
| C.逆反应的活化能一定大于146kJ/mol |
| D.逆反应的活化能一定大于正反应的活化能 |
更新时间:2016-12-09 09:36:31
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列与化学反应能量变化相关的叙述正确的是( )
| A.生成物能量一定低于反应物总能量 |
| B.热化学方程式的化学计量数可表示分子的个数 |
| C.反应热指的是反应过程中放出的热量 |
| D.同温同压下,H2(g)+Cl2(g)= 2HCl(g)在光照和点燃条件的△H相同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法不正确的是
| A.化学反应速率是可以通过实验测定的 |
| B.研究反应热时需要明确体系与环境 |
C.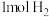 完全燃烧生成气态水时所放出的热量称为氢气的燃烧热 完全燃烧生成气态水时所放出的热量称为氢气的燃烧热 |
| D.可以采用定性和定量的方法研究影响化学反应速率的因素 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】我国有较多的科研人员在研究甲醛的氧化,有人提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如图(图中只画出了HAP的部分结构)。
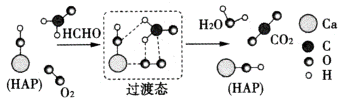
下列说法正确的是

下列说法正确的是
| A.该过程中有极性键形成 |
| B.HCHO在反应过程中有C=O键发生断裂 |
| C.根据图示信息,CO2分子中的氧原子全部来自O2 |
| D.HAP能提高HCHO与O2反应的活化能,但不改变焓变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法正确的是
| A.放热反应不需要加热就能发生 |
| B.升高温度或加入催化剂,均可以改变化学反应的反应热 |
| C.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同 |
| D.一定条件下某吸热反应能自发进行,说明该反应是熵增大的反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】参照反应Br+H2―→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
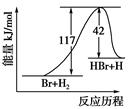

| A.正反应为吸热反应 |
| B.正反应为放热反应 |
| C.加入催化剂,该化学反应的反应热增大 |
| D.从图中可看出,该反应的反应热与反应途径有关 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
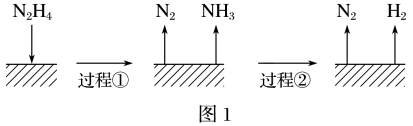
【推荐2】肼(N2H4)在不同条件下分解产物不同,200 ℃时在Cu表面分解的机理如图1。已知200 ℃时:
反应Ⅰ:3N2H4(g)=N2(g)+4NH3(g) ΔH1=-32.9 kJ·mol-1
反应Ⅱ:N2H4(g)+H2(g)=2NH3(g) ΔH2=-41.8 kJ·mol-1
下列说法不正确 的是
反应Ⅰ:3N2H4(g)=N2(g)+4NH3(g) ΔH1=-32.9 kJ·mol-1
反应Ⅱ:N2H4(g)+H2(g)=2NH3(g) ΔH2=-41.8 kJ·mol-1
下列说法


| A.图1所示过程①是放热反应、②是吸热反应 |
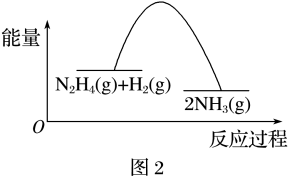
| B.反应Ⅱ的能量过程示意图如图2所示 |
| C.断开3 mol N2H4(g)中的化学键吸收的能量大于形成1 mol N2(g)和4 mol NH3(g)中的化学键释放的能量 |
| D.200 ℃时,肼分解生成氮气和氢气的热化学方程式为N2H4(g)=N2(g)+2H2 (g) ΔH=+50.7 kJ·mol-1 |
您最近一年使用:0次

 在光照和点燃条件下的
在光照和点燃条件下的 相同
相同 、
、
 ),活化氧可以快速氧化
),活化氧可以快速氧化 ,从而消除雾霾。其活化过程中的能量变化如图所示,下列说法错误的是
,从而消除雾霾。其活化过程中的能量变化如图所示,下列说法错误的是