在100mLNaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物,加热使之充分反应,下图表示加入固体的质量与产生气体的体积(标准状况)的关系。
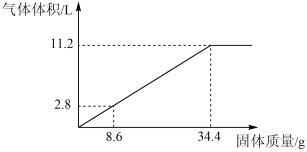
试计算:
(1) NaOH溶液的物质的量浓度是_______________ mol·L-1
(2) 当NaOH溶液为140mL,固体为51.6g时,充分反应产生的气体为______________ L(标准状况)
(3) 当NaOH溶液为180mL,固体仍为51.6g时,充分反应产生的气体为___________ L(标准状况)。

试计算:
(1) NaOH溶液的物质的量浓度是
(2) 当NaOH溶液为140mL,固体为51.6g时,充分反应产生的气体为
(3) 当NaOH溶液为180mL,固体仍为51.6g时,充分反应产生的气体为
12-13高一上·黑龙江绥化·期末 查看更多[4]
(已下线)2011-2012学年黑龙江省绥棱县第一中学高一上学期期末考试化学试卷2016届北京西城(南区)重点中学高三第一学期课堂综合练习化学试卷上海市南洋模范中学2016-2017学年高一下学期期中考试化学试题(已下线)第17讲 氨的转化与生成-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)
更新时间:2016-12-09 09:54:14
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】现有一定量铝粉和铁粉的混合物与一定体积稀硝酸充分反应,反应过程中无气体放出(硝酸的还原产物是NH4NO3)。在反应结束后的溶液中,逐滴加入2mol∙L-1的NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量的关系如图所示。
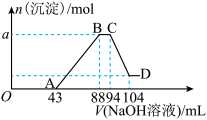
(1)写出OA段反应的离子方程式:____________________________ 。
(2)B点时溶液中含有溶质的化学式为____________ 。
(3)a的数值为__________ 。
(4)原硝酸溶液中HNO3的物质的量为__________ mol。

(1)写出OA段反应的离子方程式:
(2)B点时溶液中含有溶质的化学式为
(3)a的数值为
(4)原硝酸溶液中HNO3的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】MnCO3可用作电讯器材元件材料,还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率随温度的变化,如图所示。则300℃时,剩余固体中n(Mn):n(O)为___ ;图中C点对应固体的成分为___ (填化学式)。
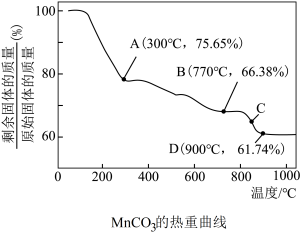

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】按要求回答问题。
(1)将19.4gCO2和水蒸气的混合气体,与足量的Na2O2反应,收集到标准状况下5.6L的气体,试确定混合气体的平均相对分子质量为___________ ,CO2与水蒸气的物质的量之比为___________ 。
(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入4.032L(标准状况下的)O2,在高温下充分反应后测得气体的密度为1.34g·L-1(已折算成标准状况,AlN不跟O2反应),则所得气体的摩尔质量为___________ g·mol-1,该气体的成分是___________ (写化学式),该样品中含杂质碳___________ g。
(3)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。草酸钴是制备钴的氧化物的重要原料。如图为二水合草酸钴(CoC2O4·2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物。
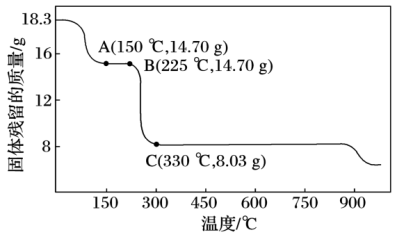
①通过计算确定C点剩余固体的化学成分为___________ (填化学式)。试写出B点对应的物质与O2在225~300℃发生反应的化学方程式:___________ 。
②取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480mL5mol·L-1盐酸恰好完全溶解固体,得到CoCl2溶液和4.48L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物质的量之比为___________ 。
(1)将19.4gCO2和水蒸气的混合气体,与足量的Na2O2反应,收集到标准状况下5.6L的气体,试确定混合气体的平均相对分子质量为
(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入4.032L(标准状况下的)O2,在高温下充分反应后测得气体的密度为1.34g·L-1(已折算成标准状况,AlN不跟O2反应),则所得气体的摩尔质量为
(3)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。草酸钴是制备钴的氧化物的重要原料。如图为二水合草酸钴(CoC2O4·2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物。

①通过计算确定C点剩余固体的化学成分为
②取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480mL5mol·L-1盐酸恰好完全溶解固体,得到CoCl2溶液和4.48L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物质的量之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】某研究性学习小组对铝热反应实验展开研究。现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理?答:_________________ (填“合理”或“不合理)
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试是_______________ 。
(3)实验室溶解该熔融物,下列试剂中最好的是____________ (填序号)。
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液
II.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:
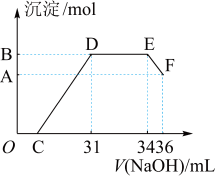
(4)图中OC段没有沉淀生成,此阶段发生反应的化学方程式为__________________________________ 。
(5)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式是
______________________________________________ ;
上述现象说明溶液中_________________________ 结合OH-的能力比_______ 强(填离子符号)。
(6)B与A的差值为_________ mol。B点对应的沉淀的物质的量为________ mol,C点对应的氢氧化钠溶液的体积为___________ mL
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理?答:
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试是
(3)实验室溶解该熔融物,下列试剂中最好的是
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液
II.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:

(4)图中OC段没有沉淀生成,此阶段发生反应的化学方程式为
(5)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式是
上述现象说明溶液中
(6)B与A的差值为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
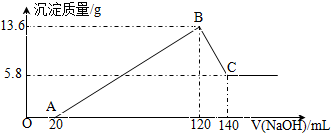
【推荐2】将一定质量的Mg—Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。回答下列问题。_________ ,合金中Mg与Al的物质的量之比是________ ;
(2)所加NaOH溶液的物质的量浓度是________________ ;
(3)原HCl溶液的物质的量浓度是_____________________ 。
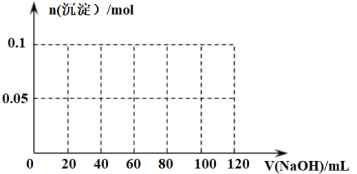
(4)向含有0.1molNH4Al(SO4)2的溶液中逐滴加入5 mol·L-1NaOH溶液,开始发现熔液中出现白色沉淀并逐渐增多;一段时间后有刺激性气味的气体(NH3)逸出;最后白色沉淀逐渐减少并最终消失。请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图。________
(2)所加NaOH溶液的物质的量浓度是
(3)原HCl溶液的物质的量浓度是
(4)向含有0.1molNH4Al(SO4)2的溶液中逐滴加入5 mol·L-1NaOH溶液,开始发现熔液中出现白色沉淀并逐渐增多;一段时间后有刺激性气味的气体(NH3)逸出;最后白色沉淀逐渐减少并最终消失。请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图。
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】取四份不同质量的(NH4)2SO4和NH4HSO4的混合物样品,分别加入到200mL1 mol/L的NaOH溶液中,充分反应,加热,再将逸出气体干燥后用浓H2SO4吸收,测定结果如下表:
回答下列问题:
(1)分析上表中的数据,求m的值。
(2)在研究时发现,浓硫酸增加的质量(g)与样品的质量(g)之间满足一定的函数关系。假设样品的质量为x,浓硫酸增加的质量为y,写出当x在不同范围时y与x的函数关系。
| 实验编号 | I | II | III | IV |
| 样品的质量(g) | 9.88 | 19.76 | 29.64 | 49.40 |
| 浓硫酸增加的质量(g) | m | m | 1.36 | 0 |
(1)分析上表中的数据,求m的值。
(2)在研究时发现,浓硫酸增加的质量(g)与样品的质量(g)之间满足一定的函数关系。假设样品的质量为x,浓硫酸增加的质量为y,写出当x在不同范围时y与x的函数关系。
您最近一年使用:0次



