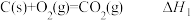1840年,俄国化学家盖斯(G·H·Hess)从大量的实验事实中总结出了盖斯定律。盖斯定律在生产和科学研究中有很重要的意义,有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得。已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知单质碳的燃烧热为Y kJ/mol,则1 mol C与O2反应生成CO的反应热△H为
| A.-Y kJ/mol | B.-(5X-0.5Y) kJ/mol |
| C.-(10X-Y) kJ/mol | D.+(10X-Y) kJ/mol |
15-16高二上·湖南衡阳·期中 查看更多[3]
(已下线)1.1.2 反应热的测量和计算(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)吉林省吉林地区普通高中友好学校联合体第三十一届2019-2020学年高二上学期期中考试化学试题2015-2016学年湖南省衡阳一中高二上学期期中(理)化学试卷
更新时间:2016-12-09 09:58:34
|
【知识点】 燃烧热
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列指定反应的离子方程式正确的是
A. 的燃烧热为 的燃烧热为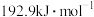 ,则甲醇的燃烧热的热化学方程式为: ,则甲醇的燃烧热的热化学方程式为: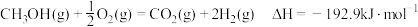 |
B.向沸水中滴加 溶液制 溶液制 胶体: 胶体: |
C. 溶液与少量的 溶液与少量的 溶液混合: 溶液混合: |
D.向明矾溶液中加入氢氧化钡溶液至沉淀的质量最大: |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列表述正确的是 ( )
| A.已知在常温常压下:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH= -890.3kJ·mol-1甲烷的燃烧热为ΔH= -890.3kJ·mol-1, |
| B.加入催化剂可以改变化学反应的反应热,使反应更容易发生. |
| C.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
您最近半年使用:0次

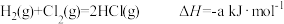
 的燃烧热
的燃烧热
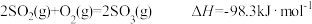
 的能量一定比
的能量一定比 能量高
能量高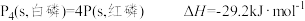
 (s,白磷)比P(s,红磷)稳定
(s,白磷)比P(s,红磷)稳定