W、X、Y和Z是周期表中前20号元素,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是____________ ;Z元素是____________ 。
(2)化合物WY和WX2的化学式分别是____________ 和____________ 。
(3)Y和Z形成的两种常见化合物的分子式是____________ 和____________ 。
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:____________ 。
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是
(2)化合物WY和WX2的化学式分别是
(3)Y和Z形成的两种常见化合物的分子式是
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:
2007·全国·高考真题 查看更多[7]
2007年普通高等学校招生全国统一考试(全国卷Ⅰ)理综化学部分(已下线)2012届河南省南阳一中高三上学期第四次月考化学试卷2015-2016学年吉林省吉林第一中学高一入学摸底化学试卷陕西省黄陵中学高新部2018届高三上学期期末考试化学试题福建省福州市第一中学2020年高一在线自测自评质检化学试题河南省林州市第一中学2021-2022学年高一下学期开学检测化学试题(已下线)BBWYhjhx1008.pdf
更新时间:2016-12-09 00:49:37
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
(1)C在元素周期表中的位置为___________ ,G的原子结构示意图是___________ 。
(2)D与E按原子个数比1∶1形成化合物甲,其电子式为___________ ,所含化学键类型为___________ 。
(3)D、E、F、G形成的简单离子,半径由大到小的顺序是___________ 。(用离子符号表示)
(4)B、C、F、G最高价氧化物对应水化物酸性最强的是___________ 。(填对应物质的化学式)
(5)写出一种由A、B、C、D四种元素组成的离子化合物的化学式___________ 。
(1)C在元素周期表中的位置为
(2)D与E按原子个数比1∶1形成化合物甲,其电子式为
(3)D、E、F、G形成的简单离子,半径由大到小的顺序是
(4)B、C、F、G最高价氧化物对应水化物酸性最强的是
(5)写出一种由A、B、C、D四种元素组成的离子化合物的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F均是短周期元素,其原子序数依次增大,A和B同周期,A和E同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C、D的阳离子电子层结构相同,C与B可生成C2B或C2B2,D的阳离子半径是同周期最小的,F的原子半径是所在周期中最小的。请回答:
(1)E在元素周期表中的位置是_______ 。
(2)C所在周期电负性最强的是_______ ;AB2的结构式是_______ 。
(3)B、C、F的离子半径由大到小的顺序为_______ (用化学式回答,下同);A、D、E元素的最高价氧化物对应水化物中,酸性最强的是_______ 。
(4)B的简单氢化物比H2S沸点高的原因是_______ 。
(5)C与D两元素的最高价氧化物对应水化物反应的离子方程式:_______ 。
(6)用一个离子方程式证明A、E的非金属性强弱:_______ 。
(1)E在元素周期表中的位置是
(2)C所在周期电负性最强的是
(3)B、C、F的离子半径由大到小的顺序为
(4)B的简单氢化物比H2S沸点高的原因是
(5)C与D两元素的最高价氧化物对应水化物反应的离子方程式:
(6)用一个离子方程式证明A、E的非金属性强弱:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】处于相邻三个周期的元素A、B、C,原子序数依次增大,三者原子序数之和为25,且知B、C处于同一主族,1.8gD与足量盐酸反应生成DCl3和2.24L氢气(标况),E和D处于同周期,且E离子和D离子具有相同的电子结构,元素F和C能形成FC型离子化合物,又知C离子比F离子多一个电子层,试判断:
1、六种元素的符号分别为A______ ,B_______ ,C______ ,D______ ,E______ ,F_______ 。
2、写出A、B、C三种元素形成的常见化合物的化学式______ ,其分子是原子之间含_____ 键的_____________ 化合物。
3、用电子式表示:
(1)A与C形成化合物的过程________________________ 。
(2)C与E形成化合物的过程________________________ 。
1、六种元素的符号分别为A
2、写出A、B、C三种元素形成的常见化合物的化学式
3、用电子式表示:
(1)A与C形成化合物的过程
(2)C与E形成化合物的过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有五种元素,其中A、B、C为短周期主族元素,D、E为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)B元素基态原子中能量最高的电子的电子云在空间有_______ 个伸展方向,原子轨道呈_______ 形。
(2)E位于第_______ 族_______ 区,该元素原子的核外电子排布式为_______ 。
(3)已知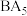 为离子化合物,写出其电子式:
为离子化合物,写出其电子式:_______ 。
(4)检验D元素的方法是_______ ,请用原子结构的知识解释产生此现象的原因:_______ 。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
C元素的第一至第四电离能如下: 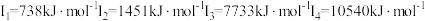 |
| D是前四周期中电负性最小的元素 |
| E在周期表的第七列 |
(2)E位于第
(3)已知
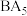 为离子化合物,写出其电子式:
为离子化合物,写出其电子式:(4)检验D元素的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F为原子序数依次增大的六种元素,其中A、B、C、D、E为短周期元素,F为第四周期元素。已知:A原子核外电子只有一种自旋取向;B元素原子核外有三个未成对电子;C原子的第一至第四电离能数据分别为: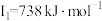 、
、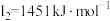 、
、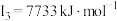 、
、 ;D原子核外最外层所有p轨道均为半充满;E元素的族序数与周期序数的差为4;F元素原子的最外层只有一个电子,其次外层的所有电子均成对。
;D原子核外最外层所有p轨道均为半充满;E元素的族序数与周期序数的差为4;F元素原子的最外层只有一个电子,其次外层的所有电子均成对。
回答下列问题:
(1)写出A的元素符号_______ ,写出C元素在周期表中位置_______ ;
(2)B元素基态原子的轨道表示式为_______ ,其中电子占据最高能级的电子云轮廓图为_______ 形
(3)比较D、E的电负性:_______ >_______ (用元素符号表示);
(4)写出元素F的基态原子简化电子排布式_______ ;
(5)B、C、D三种元素的原子半径由大到小的顺序_______ (用元素符号表示)。
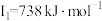 、
、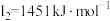 、
、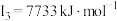 、
、 ;D原子核外最外层所有p轨道均为半充满;E元素的族序数与周期序数的差为4;F元素原子的最外层只有一个电子,其次外层的所有电子均成对。
;D原子核外最外层所有p轨道均为半充满;E元素的族序数与周期序数的差为4;F元素原子的最外层只有一个电子,其次外层的所有电子均成对。回答下列问题:
(1)写出A的元素符号
(2)B元素基态原子的轨道表示式为
(3)比较D、E的电负性:
(4)写出元素F的基态原子简化电子排布式
(5)B、C、D三种元素的原子半径由大到小的顺序
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。请用具体的元素回答下列问题:
(1)E元素基态原子电子排布式为_______ 。
(2)用电子排布图表示F元素原子的价电子构型:_______ 。
(3)F、G元素对应的最高价含氧酸中酸性较强的酸的分子式为_______ 。
(4)离子半径:D+_______ B3-,第一电离能:B_______ C(填“<”“>”或“=”)
(5)A、C形成的一种“绿色”氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为_______ ,所含化学键类型_______
(6)写出E与D的最高价氧化物对应水化物反应的化学方程式:_______
(1)E元素基态原子电子排布式为
(2)用电子排布图表示F元素原子的价电子构型:
(3)F、G元素对应的最高价含氧酸中酸性较强的酸的分子式为
(4)离子半径:D+
(5)A、C形成的一种“绿色”氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为
(6)写出E与D的最高价氧化物对应水化物反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】四种短周期元素的核电荷数依次增大,它们相关信息如下表。
完成下列填空:
(1)W所形成的负离子的电子式为_______ ,该离子核外能量最高的电子位于_______ (填电子层符号)层。
(2)X用于测定文物年代的X核素的符号为_______ ;该核素核内中子数与质子数之差为_______ 。
(3)证明Y的气态氢化物极易溶于水的实验装置如所示。简述引发实验的操作。_______
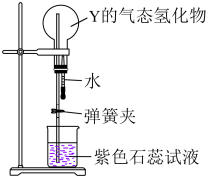
用相关化学方程式解释实验过程中紫色石蕊试液变色的原因:_______ 。
(4)Z在元素周期表中的位置是_______ ,比较X与Z原子半径的相对大小并说明理由。_______
(5)通过如下装置可以比较X、Y、Z三种元素的非金属性强弱。
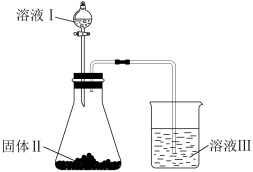
溶液Ⅰ的溶质是_______ (填化学式);进行实验时溶液Ⅲ中的现象是_______ 。有人认为上述装置存在缺陷,无法达到实验目的,请写出改进的措施。_______
| 元素代号 | W | X | Y | Z |
| 相关信息 | 原子得到1个电子后达到稀有气体稳定结构 | 某种核素常用于测定文物年代 | 气态氢化物极易溶于水 | 原子最外层电子是最内层电子的2倍 |
(1)W所形成的负离子的电子式为
(2)X用于测定文物年代的X核素的符号为
(3)证明Y的气态氢化物极易溶于水的实验装置如所示。简述引发实验的操作。

用相关化学方程式解释实验过程中紫色石蕊试液变色的原因:
(4)Z在元素周期表中的位置是
(5)通过如下装置可以比较X、Y、Z三种元素的非金属性强弱。

溶液Ⅰ的溶质是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期主族元素A、B、C、D、E、F的原子序数依次增大,其中B、E同主族,且E的原子序数是B的2倍,A的某种氢化物M可作为火箭推进剂的燃料,C的原子半径在短周期主族元素中最大,D的氢氧化物是胃舒平的主要成分。用元素符号 回答下列问题:
(1)B在周期表中的位置为___________ ,氢化物M的电子式为___________ 。
(2)B、E、F所形成的简单离子半径由大到小的顺序为___________ 。
(3)C2B2含有的化学键类型为___________ ,其与水反应的离子方程式为:___________ 。
(4)D的最高价氧化物与C的最高价氧化物的水化物反应的化学方程式为:___________ 。
(1)B在周期表中的位置为
(2)B、E、F所形成的简单离子半径由大到小的顺序为
(3)C2B2含有的化学键类型为
(4)D的最高价氧化物与C的最高价氧化物的水化物反应的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最大。
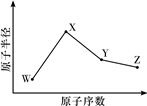
(1)X位于元素周期表中的位置是____________________ 。
(2)Z的气态氢化物和溴化氢相比,较稳定的是____________ (写化学式)。
(3)W与X形成的一种化合物和水反应能生成W的单质,请写出该反应的化学方程式:________________________________________________________________________ 。
(4)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是________________________________________________________________________ 。

(1)X位于元素周期表中的位置是
(2)Z的气态氢化物和溴化氢相比,较稳定的是
(3)W与X形成的一种化合物和水反应能生成W的单质,请写出该反应的化学方程式:
(4)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是
您最近一年使用:0次



