一氧化碳是一种用途广泛的化工基础原料。
(l)在高温下CO可将SO2还原为单质硫。已知:2CO(g)+O2(g)=2CO2(g) △H1=-566.0kJ·mol-1;S(s)+O2(g)=SO2(g) △H2=-296.0kJ·mol-1;
请写出CO还原SO2的热化学方程式______________________ 。
(2)工业上用一氧化碳制取氢气的反应为:CO(g)+H2O(g) CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为
CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为___________________ ,H2的平均生成速率为__________ mol·L-1·min-1。
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图:

电池总反应为:2CH3OH+3O2=2CO2+4H2O,则c电极是____________ (填正极或负极),c电极的反应方程式为__________________ 。若用该电池电解精炼铜(杂质含有Ag和Fe),粗铜应该接此电源的________ 极(填c或d),反应过程中析出精铜64g,则上述CH3OH燃料电池,消耗的O2在标况下的体积为__________ L。
(l)在高温下CO可将SO2还原为单质硫。已知:2CO(g)+O2(g)=2CO2(g) △H1=-566.0kJ·mol-1;S(s)+O2(g)=SO2(g) △H2=-296.0kJ·mol-1;
请写出CO还原SO2的热化学方程式
(2)工业上用一氧化碳制取氢气的反应为:CO(g)+H2O(g)
 CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为
CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图:

电池总反应为:2CH3OH+3O2=2CO2+4H2O,则c电极是
更新时间:2016-12-09 14:49:19
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】研究化学反应原理对于生产、生活及环境保护具有重要意义。
(1)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H=+64.39kJ•mol-1
2H2O2(l)=2H2O(l)+O2(g) △H=-196.46kJ•mol-1
H2(g)+1/2O2(g)=H2O(l) △H=-285.84kJ•mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为___________________ 。
(2)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
①已知0.4 mol KBrO3在反应中得到2 mol电子生成X,则X的化学式为_____ ;该反应的还原剂及其配平后的系数是___ 。
②根据上述反应可推知____ 。
a.氧化性:KBrO3>H3AsO4
b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X
d.还原性:X>AsH3
(1)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H=+64.39kJ•mol-1
2H2O2(l)=2H2O(l)+O2(g) △H=-196.46kJ•mol-1
H2(g)+1/2O2(g)=H2O(l) △H=-285.84kJ•mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
(2)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
①已知0.4 mol KBrO3在反应中得到2 mol电子生成X,则X的化学式为
②根据上述反应可推知
a.氧化性:KBrO3>H3AsO4
b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X
d.还原性:X>AsH3
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】工业上可以利用废气中的CO2为原料制取甲醇,其反应方程式为:CO2+3H2 CH3OH+H2O。请回答下列问题:
CH3OH+H2O。请回答下列问题:
(1)已知常温常压下下列反应的能量变化如下图所示:

写出由二氧化碳和氢气制备甲醇的热化学方程式__________________ ,该反应的△S____________ 0(填“>”或“<”或“=”),在_______________ 情况下有利于该反应自发进行。
(2)如果上述反应方程式的平衡常数K值变大,则该反应_______ (选填编号)。
(3)若反应的容器容积为2.0L,反应时间4.0 min,容器内氢气的质量减少了4.8g,在这段时间内CO2的平均反应速率为____________________ 。
 CH3OH+H2O。请回答下列问题:
CH3OH+H2O。请回答下列问题:(1)已知常温常压下下列反应的能量变化如下图所示:

写出由二氧化碳和氢气制备甲醇的热化学方程式
(2)如果上述反应方程式的平衡常数K值变大,则该反应
| A.一定向正反应方向移动 |
| B.在平衡移动时正反应速率先增大后减小 |
| C.一定向逆反应方向移动 |
| D.在平衡移动时逆反应速率先减小后增大 |
(3)若反应的容器容积为2.0L,反应时间4.0 min,容器内氢气的质量减少了4.8g,在这段时间内CO2的平均反应速率为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】工业废气、汽车尾气排放出的SO2、NOx等,是形成雾霾的重要因素。霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾。
(1)NOx和SO2 在空气中存在下列平衡:2NO(g)+O2(g)
在空气中存在下列平衡:2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1,2SO2(g)+O2(g)
2NO2(g) ΔH=-113.0 kJ·mol-1,2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1。SO2通常在NO2的存在下,进一步被氧化生成SO3(g)。写出NO2和SO2反应生成NO(g)和SO3(g)的热化学方程式为
2SO3(g) ΔH=-196.6 kJ·mol-1。SO2通常在NO2的存在下,进一步被氧化生成SO3(g)。写出NO2和SO2反应生成NO(g)和SO3(g)的热化学方程式为________ 。
(2)提高2SO2(g)+O2(g) 2SO3(g)反应中SO2的转化率,是减少SO2排放的有效措施。
2SO3(g)反应中SO2的转化率,是减少SO2排放的有效措施。
①温度为T℃时,在2 L的密闭容器中加入2.0 mol 和1.0 mol O2发生反应,达到平衡时容器内气体压强变为起始时的
和1.0 mol O2发生反应,达到平衡时容器内气体压强变为起始时的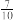 。该反应的平衡常数为
。该反应的平衡常数为_____ 。
②在①中条件下,反应达到平衡后,改变下列条件,能使SO2的转化率提高的是_____ 。
A.在其他条件不变时,减少容器的体积
B.在其他条件不变时,改用高效催化剂
C.在其他条件不变时,升高体系温度
D.1.0mol温度和容器体积不变,充入1.0 mol氦气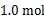
E.温度和容器体积不变,充入1.0 mol O2
(3)利用如图所示的电解装置,可将雾霾中的NO、SO2转化为硫酸铵,从而实现废气的回收再利用。通入NO的电极反应式为______ ;若通入的NO体积为4.48 L(标况下),则理论上另一电极通入SO2的物质的量应为_______ 。
(1)NOx和SO2
 在空气中存在下列平衡:2NO(g)+O2(g)
在空气中存在下列平衡:2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1,2SO2(g)+O2(g)
2NO2(g) ΔH=-113.0 kJ·mol-1,2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1。SO2通常在NO2的存在下,进一步被氧化生成SO3(g)。写出NO2和SO2反应生成NO(g)和SO3(g)的热化学方程式为
2SO3(g) ΔH=-196.6 kJ·mol-1。SO2通常在NO2的存在下,进一步被氧化生成SO3(g)。写出NO2和SO2反应生成NO(g)和SO3(g)的热化学方程式为(2)提高2SO2(g)+O2(g)
 2SO3(g)反应中SO2的转化率,是减少SO2排放的有效措施。
2SO3(g)反应中SO2的转化率,是减少SO2排放的有效措施。①温度为T℃时,在2 L的密闭容器中加入2.0 mol
 和1.0 mol O2发生反应,达到平衡时容器内气体压强变为起始时的
和1.0 mol O2发生反应,达到平衡时容器内气体压强变为起始时的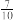 。该反应的平衡常数为
。该反应的平衡常数为②在①中条件下,反应达到平衡后,改变下列条件,能使SO2的转化率提高的是
A.在其他条件不变时,减少容器的体积
B.在其他条件不变时,改用高效催化剂
C.在其他条件不变时,升高体系温度
D.1.0mol温度和容器体积不变,充入1.0 mol氦气
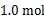
E.温度和容器体积不变,充入1.0 mol O2
(3)利用如图所示的电解装置,可将雾霾中的NO、SO2转化为硫酸铵,从而实现废气的回收再利用。通入NO的电极反应式为

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】2020年9月在75届联合国大会上,中国庄严承诺:2030年前实现碳达峰,2060年前实现碳中和。实现CO2大规模减排,需要多措并举,其中碳资源的综合利用成为重中之重。二甲醚(CH3OCH3)是未来制取低碳烯烃的主要原料之一,也是一种优良的洁净燃料。
利用CO2催化加氢制备二甲醚过程中发生的化学反应为:
反应I:CO2(g)+H2(g) CO(g)+H2O(g) ∆H1>0
CO(g)+H2O(g) ∆H1>0
反应II:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H2<0
CH3OH(g)+H2O(g) ∆H2<0
反应III:2CH3OH(g) CH3OCH3(g)+H2O(g) ∆H3<0
CH3OCH3(g)+H2O(g) ∆H3<0
一定温度下,向体积为1L的恒容密闭容器中通入1molCO2和3molH2进行上述反应,反应经10min达到平衡,此时CO2的平衡转化率为30%,容器中CO(g)为0.05mol,CH3OH(g)为0.05mol。0~10min,用CH3OCH3(g)的物质的量浓度变化表示的平均反应速率v(CH3OCH3)=_____ 。
利用CO2催化加氢制备二甲醚过程中发生的化学反应为:
反应I:CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H1>0
CO(g)+H2O(g) ∆H1>0反应II:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H2<0
CH3OH(g)+H2O(g) ∆H2<0反应III:2CH3OH(g)
 CH3OCH3(g)+H2O(g) ∆H3<0
CH3OCH3(g)+H2O(g) ∆H3<0一定温度下,向体积为1L的恒容密闭容器中通入1molCO2和3molH2进行上述反应,反应经10min达到平衡,此时CO2的平衡转化率为30%,容器中CO(g)为0.05mol,CH3OH(g)为0.05mol。0~10min,用CH3OCH3(g)的物质的量浓度变化表示的平均反应速率v(CH3OCH3)=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应:2X(g) Y(g)+3Z(g)。
Y(g)+3Z(g)。
(1)经5min后达平衡,此时容器内压强为起始时的1.2倍,则用Y表示的速率为____________ mol/(L·min)。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一时间内测得的反应速率分别为:甲:ν(X)=3.5 mol/(L min);乙:ν(Y)=2 mol/(L
min);乙:ν(Y)=2 mol/(L min);丙:ν(Z)=4.5 mol/(L
min);丙:ν(Z)=4.5 mol/(L min);丁:ν(X)=0.075 mol/(L
min);丁:ν(X)=0.075 mol/(L s)。若其他条件相同,温度不同,温度由高到低的顺序是(填序号)
s)。若其他条件相同,温度不同,温度由高到低的顺序是(填序号)________________ 。
(3)若向达到(1)的平衡体系中充入氮气,则平衡向___ (填“左”“右”或“不”,下同)移动;若将达到(1)的平衡体系中移走部分混合气体,则平衡向___ 移动。
(4)若在相同条件下向达到(1)所述平衡体系中再充入0.5molX气体,则平衡后X的转化率与(1)的平衡中X的转化率相比___ 。
A.无法确定 B.前者一定大于后者
C.前者一定等于后者 D.前者一定小于后者
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达平衡时仍与(1)的平衡等效,则a、b、c应满足的关系为____________ 。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达平衡时仍与(1)的平衡等效,则起始时维持化学反应向逆反应方向进行,则c的取值范围应为______________ 。
 Y(g)+3Z(g)。
Y(g)+3Z(g)。(1)经5min后达平衡,此时容器内压强为起始时的1.2倍,则用Y表示的速率为
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一时间内测得的反应速率分别为:甲:ν(X)=3.5 mol/(L
 min);乙:ν(Y)=2 mol/(L
min);乙:ν(Y)=2 mol/(L min);丙:ν(Z)=4.5 mol/(L
min);丙:ν(Z)=4.5 mol/(L min);丁:ν(X)=0.075 mol/(L
min);丁:ν(X)=0.075 mol/(L s)。若其他条件相同,温度不同,温度由高到低的顺序是(填序号)
s)。若其他条件相同,温度不同,温度由高到低的顺序是(填序号)(3)若向达到(1)的平衡体系中充入氮气,则平衡向
(4)若在相同条件下向达到(1)所述平衡体系中再充入0.5molX气体,则平衡后X的转化率与(1)的平衡中X的转化率相比
A.无法确定 B.前者一定大于后者
C.前者一定等于后者 D.前者一定小于后者
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达平衡时仍与(1)的平衡等效,则a、b、c应满足的关系为
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达平衡时仍与(1)的平衡等效,则起始时维持化学反应向逆反应方向进行,则c的取值范围应为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】丙酮的碘代反应CH3COCH3+I2→CH3COCH2I+HI的速率方程为v=k·cm(CH3COCH3)·cn(I2)·cp(H+),其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为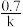 ,其中k=A
,其中k=A (k为速率常数,Ea为活化能,A为比例系数)。
(k为速率常数,Ea为活化能,A为比例系数)。
(1)在保持酸性不变的条件下,改变下列条件时,反应的瞬时速率如表所示。
①下列关于速率常数k的说法中正确的是______ (填标号)。
A.速率常数k只受温度影响
B.加入催化剂,可使k增大
C.可逆反应中的正逆反应速率常数k正和k逆相等
②当T2>T1时,vx______ 2.8mol•L-1•min-1(填:“大于”、“小于”或“等于”)。
③速率方程中:m=_____ ;n=_____ ;k=_____ 。
(2)若T1℃时,v=k·cm(CH3COCH3)·cn(I2)·cp(H+),c(I2)、c(CH3COCH3)、c(H+)的起始浓度依次是0.01mol•L-1、0.1mol•L-1、0.01mol•L-1。当c(I2)的浓度降低为原来一半时,反应速率将_____ (填:“变大”、“变小”或“不变”)。
(3)在过量的I2存在,c(H+)=1mol•L-1时。反应掉75%的CH3COCH3所需的时间是_____ min。
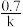 ,其中k=A
,其中k=A (k为速率常数,Ea为活化能,A为比例系数)。
(k为速率常数,Ea为活化能,A为比例系数)。(1)在保持酸性不变的条件下,改变下列条件时,反应的瞬时速率如表所示。
| 序号 | 温度 | c(CH3COCH3)/(mol•L-1) | c(I2)/(mol•L-1) | v/(10-3mol•L-1•min-1) |
| 1 | T1 | 0.25 | 0.050 | 1.4 |
| 2 | T1 | 0.50 | 0.050 | 2.8 |
| 3 | T1 | 1.00 | 0.050 | 5.6 |
| 4 | T1 | 0.50 | 0.100 | 2.8 |
| 5 | T2 | 0.50 | 0.100 | 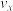 |
A.速率常数k只受温度影响
B.加入催化剂,可使k增大
C.可逆反应中的正逆反应速率常数k正和k逆相等
②当T2>T1时,vx
③速率方程中:m=
(2)若T1℃时,v=k·cm(CH3COCH3)·cn(I2)·cp(H+),c(I2)、c(CH3COCH3)、c(H+)的起始浓度依次是0.01mol•L-1、0.1mol•L-1、0.01mol•L-1。当c(I2)的浓度降低为原来一半时,反应速率将
(3)在过量的I2存在,c(H+)=1mol•L-1时。反应掉75%的CH3COCH3所需的时间是
您最近一年使用:0次



