下列关于化学键和物质结构的说法中正确的是
| A.干冰和水晶熔化时,所克服的作用力相同 |
| B.原子晶体氮化硅制成的陶瓷具有熔点高、硬度大等特点 |
| C.由非金属元素组成的化合物一定是共价化合物 |
| D.不同元素组成的多原子分子里的化学键一定是极性键 |
10-11高三上·河南新乡·阶段练习 查看更多[1]
(已下线)2011届河南省卫辉市高级中学高三上学期第四次月考(理综)化学部分
更新时间:2016-12-09 01:23:43
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】我国科学家结合光谱实验和理论计算,证明了五个水分子就可以构成最小水滴(微观结构如图所示)。关于该最小水滴的说法正确的是
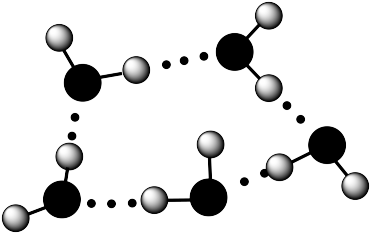

| A.是纯净物 | B.是一种胶体 |
| C.水分子内形成氢键 | D.水分子内存在非极性键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中不正确的是
| A.甲硫醇(CH3SH)比甲醇的熔点低的原因是甲醇分子间易形成氢键 |
| B.碘易溶于四氯化碳,甲烷难溶于水都可用“相似相溶”原理解释 |
C.在NH 和[Cu(NH3)4]2+中都存在配位键 和[Cu(NH3)4]2+中都存在配位键 |
| D.液态氟化氢中氟化氢分子之间形成氢键,可写为(HF)n,则NO2分子间也是因氢键而聚合形成N2O4 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于晶体的说法正确的组合是
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、H2O、H2S晶体的熔点依次降低
④氯化钠熔化时离子键被破坏
⑤离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑥熔点:NaF>MgF2>AlF3
⑦离子晶体中阴离子的配位数:CsCl>NaCl>CaF2
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、H2O、H2S晶体的熔点依次降低
④氯化钠熔化时离子键被破坏
⑤离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑥熔点:NaF>MgF2>AlF3
⑦离子晶体中阴离子的配位数:CsCl>NaCl>CaF2
| A.①②③⑥ | B.①②④ | C.③⑤⑥ | D.③④⑦ |
您最近半年使用:0次
【推荐2】下列有关微粒间作用力的说法正确的是
| A.硼酸[B(OH)3]晶体具有与石墨相似的层状结构,则分子中B原子发生的是sp2杂化,不同层分子间主要作用力是范德华力 |
| B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所以与共价键类似也有方向性和饱和性 |
| C.干冰气化和冰融化克服的分子间作用力相同 |
| D.离子晶体熔融状态电离过程中,只有离子键被破坏 |
您最近半年使用:0次