在两份15mL、1mol/L的Ba(OH)2溶液中,分别滴入H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如右图所示。下列分析不正确的是
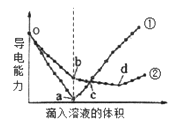
| A.o-b段,发生的离子方程式:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B.bd段,发生的离子方程式:OH-+H+=H2O |
| C.c点,两溶液中阴、阳离子的浓度之和相等 |
| D.o-a段加入溶液的体积为20mL,则NaHSO4溶液的浓度为0.75mol/L |
更新时间:2017-03-11 20:20:57
|
【知识点】 离子反应在生活、生产中的应用解读
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】连接装置如图1所示,烧杯中盛放的是 溶液,当通过滴定管逐渐加入
溶液,当通过滴定管逐渐加入 溶液时,溶液的导电性的变化趋势如图2所示。滴加
溶液时,溶液的导电性的变化趋势如图2所示。滴加 溶液至图2中
溶液至图2中 点时,灯泡几乎熄灭,
点时,灯泡几乎熄灭, 溶液中含有的溶质可能是
溶液中含有的溶质可能是

 溶液,当通过滴定管逐渐加入
溶液,当通过滴定管逐渐加入 溶液时,溶液的导电性的变化趋势如图2所示。滴加
溶液时,溶液的导电性的变化趋势如图2所示。滴加 溶液至图2中
溶液至图2中 点时,灯泡几乎熄灭,
点时,灯泡几乎熄灭, 溶液中含有的溶质可能是
溶液中含有的溶质可能是
A.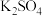 | B. | C.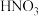 | D. |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】氯化亚铜,化学式CuCl或Cu2Cl2。为白色立方结晶或白色粉末,微溶于水,溶于浓盐酸生成氯化亚铜酸(HCuCl2强酸),溶于氨水生成氯化二氨合亚铜,不溶于乙醇。
实验室制备氯化亚铜∶
方法1∶CuCl2溶于浓盐酸,加入铜屑并加热,生成HCuCl2溶液,加水稀释可得CuCl沉淀;
方法2∶向含有铜丝、氯化铵、盐酸的溶液中加入硝酸作催化剂,通入氧气并加热,将反应得到的NH4[CuCl2]用大量的水稀释可得CuCl沉淀。
工业制法∶向CuSO4和NaCl的混合溶液中加入Fe粉或通入SO2,充分反应后再用大量的水稀释,过滤、酒精洗涤、真空干燥。
上述氯化亚铜性质及制备过程中涉及的离子方程式书写正确的是
实验室制备氯化亚铜∶
方法1∶CuCl2溶于浓盐酸,加入铜屑并加热,生成HCuCl2溶液,加水稀释可得CuCl沉淀;
方法2∶向含有铜丝、氯化铵、盐酸的溶液中加入硝酸作催化剂,通入氧气并加热,将反应得到的NH4[CuCl2]用大量的水稀释可得CuCl沉淀。
工业制法∶向CuSO4和NaCl的混合溶液中加入Fe粉或通入SO2,充分反应后再用大量的水稀释,过滤、酒精洗涤、真空干燥。
上述氯化亚铜性质及制备过程中涉及的离子方程式书写正确的是
| A.CuCl+2NH3•H2O=[Cu(NH3)2]++Cl-+2H2O |
B.CuCl2+Cu+2Cl- 2[CuCl2]- 2[CuCl2]- |
| C.Cu2++Cl-+Fe=CuCl↓+Fe2+ |
D.2Cu2++SO2+4Cl-+4OH-=2[CuCl2]-+SO +2H2O +2H2O |
您最近一年使用:0次



