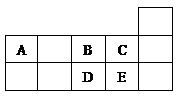W、X、Y、Z、N、M元素,它们在周期表中位置如图所示,下列说法不正确的是
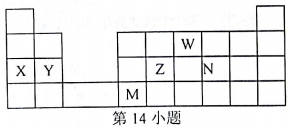
| A.离子半径:W>X>Y | B.单质的还原性:X>Y>N |
| C.硒与元素N同主族,最高价氧化物的水化物的酸性比N的弱 | D.元素M位于金属与非金属的分界线附近,推测M元素的单质一定可以做半导体材料 |
更新时间:2017-04-06 18:42:18
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
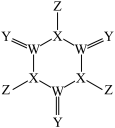
【推荐1】科学家研制了一种可水解生成次氯酸的新型漂白剂,其分子结构可用如图表示。W、X、Y、Z均为原子序数依次增大的短周期元素。常温下,0.1mol∙L-1Z的氢化物的水溶液pH=1,且Z与Y位于不同周期。下列叙述正确的是

A.原子半径: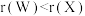 |
| B.最简单氢化物的热稳定性:X>Y |
| C.Z的含氧酸的酸性可能弱于W的含氧酸酸性 |
| D.如图分子中的 W=Y键是极性共价键,且共用电子对偏向W |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】W、X、Y、Z是原子序数依次增大的前四周期元素,W是第二周期简单氢化物沸点最高的非金属元素,X的最高正价与最低负价的代数和为4,非金属Y的族序数大于W,Z元素是常见的金属元素,能形成多种氧化物,其中的一种氧化物具有磁性。下列说法错误的是
| A.简单离子半径:X>Y>W |
| B.W、X、Y的氢化物均只含极性共价键 |
| C.W、Y的常见单质均有较强的氧化性 |
| D.Z与Y形成的二元化合物均可通过化合反应制得 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】元素X、Y、Z和Q在周期表中的位置如图所示,其中元素Q位于第四周期,X、Y、Z原子的最外层电子数之和为17,下列说法不正确的是。
| X | |||
| Y | Z | ||
| Q |
| A.原子半径(r):r(Q)>r(Y)>r(Z) |
| B.元素X有-4,+2,+4等多种价态 |
| C.Y、Z的氧化物对应的水化物均为强酸 |
| D.气态的氢化物的稳定性:Z>Y>Q |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】X、Y、Z、T四种原子序数递增的短周期元素,其部分性质或结构如下
下列说法正确的是
| 元素编号 | 元素性质或原子结构 |
| X | 形成的简单阳离子核外无电子 |
| Y | 元素的气态氢化物和它的最高价氧化物对应的水化物能发生化合反应 |
| Z | 元素在周期表的族序数等于周期序数的3倍 |
| T | 同周期元素中形成的简单离子半径最小 |
| A.原子半径大小顺序:T>Z>Y>X |
| B.X分别与Y、Z均可形成既含极性键又含非极性键的化合物 |
| C.T的单质与Y的最高价氧化物对应水化物的溶液不反应 |
| D.由X、Y和Z三种元素构成的强电解质,对水电离均起抑制作用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】现有部分元素的原子结构特点如表,下列叙述中正确的是
| X | L层电子数是K层电子数的3倍 |
| Y | 核外电子层数等于原子序数 |
| Z | L层电子数是K层和M层电子数之和 |
| W | 共用三对电子形成双原子分子,常温下为气体单质 |
A.W原子结构示意图为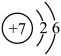 |
| B.元素X和Y只能形成原子个数比为1∶2的化合物 |
| C.元素X比元素Z的非金属性强 |
| D.X、Y、Z、W四种元素不能形成离子化合物 |
您最近一年使用:0次