根据要求完成下列化学方程式或离子 方程式。
(1)工业用电解饱和食盐水制氯气的化学方程式为____________________ 。
(2)向新制的Na2S 溶液中滴加新制的氯水的离子 方程式为_______________ 。
(3)氯化铝与过量NaOH 溶液反应的离子 方程式为____________________ 。
(4)乙醇催化氧化制乙醛的化学方程式为____________________ 。
(1)工业用电解饱和食盐水制氯气的化学方程式为
(2)向新制的Na2S 溶液中滴加新制的氯水的
(3)氯化铝与过量NaOH 溶液反应的
(4)乙醇催化氧化制乙醛的化学方程式为
更新时间:2017/08/14 15:38:57
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氢氧化钾;⑦氢氧化铁胶体;⑧氯水;⑨空气;⑩硫酸亚铁溶液。
(1)属于电解质的是___________ ,上述状态下能导电的是_____________ 。
(2)除去③中少量②的操作是____________ ,化学方程式为____________ 。
(3)向⑧中滴入几滴石蕊溶液,现象是___________ ,说明⑧具有_________ 性。
(4)向⑩中加入⑥的水溶液,产生的现象是_______________ 。
(1)属于电解质的是
(2)除去③中少量②的操作是
(3)向⑧中滴入几滴石蕊溶液,现象是
(4)向⑩中加入⑥的水溶液,产生的现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】验证次氯酸光照分解的产物可以设计成数字化实验(同时开始采集数据),此实验可以测定光照过程中氯水的pH、氯水中氯离子的浓度、广口瓶中氧气的体积分数的变化。三者变化趋势如图所示,回答下列问题:
(1)如图所示:
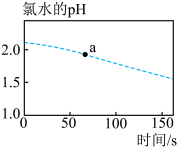
①新制氯水中所含微粒的种类有___________ 种。
②往a点对应的溶液中滴入淀粉碘化钾溶液,可能观察到的现象为___________ 。
③0~150s的过程中,氯水的pH逐渐减小的原因为___________ (用离子方程式表示)。
(2)如图所示:
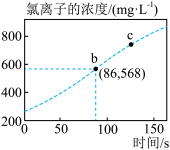
①b点对应的溶液中,所含氯离子的浓度为___________  。
。
②c点对应的溶液中,加入少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(3)如图所示:
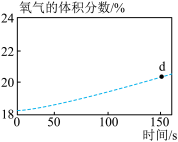
①写出一种 的用途:
的用途:___________ 。
②相同原子个数的 与
与 的质量之比为
的质量之比为___________ 。
③标准状况下,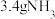 与
与___________ g 所含的电子总数相同。
所含的电子总数相同。
(1)如图所示:

①新制氯水中所含微粒的种类有
②往a点对应的溶液中滴入淀粉碘化钾溶液,可能观察到的现象为
③0~150s的过程中,氯水的pH逐渐减小的原因为
(2)如图所示:

①b点对应的溶液中,所含氯离子的浓度为
 。
。②c点对应的溶液中,加入少量的
 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(3)如图所示:

①写出一种
 的用途:
的用途:②相同原子个数的
 与
与 的质量之比为
的质量之比为③标准状况下,
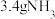 与
与 所含的电子总数相同。
所含的电子总数相同。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】元素化合物在生产生活中有很多应用,写出与下列应用相关的化学方程式 。
(1)漂白粉生效原理______________________________________________
(2)粗硅的制取___________________________________________________
(3)过氧化氢氧化碘离子___________________________________________
(4)实验室制取氨气_______________________________________________
(5)过量二氧化硫与澄清石灰水反应_____________________________________________
(6)氯碱工业生产氯气_____________________________________________
(1)漂白粉生效原理
(2)粗硅的制取
(3)过氧化氢氧化碘离子
(4)实验室制取氨气
(5)过量二氧化硫与澄清石灰水反应
(6)氯碱工业生产氯气
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氯气和氯化氢在生产生活中有着重要的应用。回答下列问题:
(1)氯碱工业是化工重要制备之一,写出工业生成氯气的化学方程式:___________ 。
(2)氯气可以制得漂粉精和消毒水(有效成分为NaClO),漂粉精可用于游泳池中水的消毒,原因是(用化学方程式表示):___________ 。将一瓶NaClO溶液(只含一种溶质),长时间放置在空气中,最终变为___________ (填溶质的化学式)。
(3)在标准状态下,224体积的氯化氢溶解在1体积的水中,形成密度为1.2g/cm3的溶液。则该溶液的物质的量浓度为___________ 。(结果保留一位小数)
(4)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系,共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质,写出一个包含上述七种物质的氧化还原反应方程式(不用配平):___________ 。上述反应中,还原剂是:___________ ,还原产物是:___________ 。
(1)氯碱工业是化工重要制备之一,写出工业生成氯气的化学方程式:
(2)氯气可以制得漂粉精和消毒水(有效成分为NaClO),漂粉精可用于游泳池中水的消毒,原因是(用化学方程式表示):
(3)在标准状态下,224体积的氯化氢溶解在1体积的水中,形成密度为1.2g/cm3的溶液。则该溶液的物质的量浓度为
(4)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系,共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质,写出一个包含上述七种物质的氧化还原反应方程式(不用配平):
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】I(1)在MgCl2溶液中滴加少量NaOH溶液,现象为______________ ,继续加入过量的NaOH溶液,现象为________________ 。
(2)在AlCl3溶液中滴加少量NaOH溶液,现象为_________________ ,所发生反应的离子方程式为________________________ ,继续加入过量的NaOH溶液,现象为___________ ,所发生反应的离子方程式为___________ 。
II将下列现象或用途中硫酸所表现出来的性质填写在空白处。
(1)把锌粒放入稀硫酸中时,有气体放出,_____________________ 。
(2)浓硫酸能够用于干燥某些气体,___________________________ 。
(3)用玻璃棒蘸浓硫酸滴在纸上时,纸变黑,_______________________ 。
(4)把木炭放入热的浓硫酸中时,有气体放出,_____________________ 。
III漂白液、漂白粉和漂粉精既可作漂白棉、麻、纸张的漂白剂,又可用作游泳池及环境的消毒剂。
(1)在常温下,将氯气通入NaOH溶液中制取漂白液的化学方程式为:____________ 。
(2)漂白粉或漂粉精的有效成分是___________ ,使用漂白粉或漂粉精时通常要加入少量的水并通入CO2,此操作方法的目的是:_____________________________ 。
(2)在AlCl3溶液中滴加少量NaOH溶液,现象为
II将下列现象或用途中硫酸所表现出来的性质填写在空白处。
(1)把锌粒放入稀硫酸中时,有气体放出,
(2)浓硫酸能够用于干燥某些气体,
(3)用玻璃棒蘸浓硫酸滴在纸上时,纸变黑,
(4)把木炭放入热的浓硫酸中时,有气体放出,
III漂白液、漂白粉和漂粉精既可作漂白棉、麻、纸张的漂白剂,又可用作游泳池及环境的消毒剂。
(1)在常温下,将氯气通入NaOH溶液中制取漂白液的化学方程式为:
(2)漂白粉或漂粉精的有效成分是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)向AlCl3溶液中,滴加少量NaOH溶液,现象是____________ ,继续滴加NaOH溶液至过量,现象是________________ 。
(2)钠与水反应的离子方程式为________________ ,该反应中氧化剂是_______ ,产生1mol H2时,转移电子的物质的量为______ mol。
(2)钠与水反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】4种有机化合物之间存在下列转化关系。
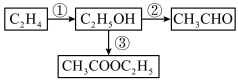
(1)在上述4种有机化合物中,属于烃的是________ (填名称),其分子中的官能团是________ 。
(2)反应②的实验中用到Cu丝,其作用是作________ 剂。
(3)反应③的反应类型属于________ 反应,该反应的化学方程式是________ 。

(1)在上述4种有机化合物中,属于烃的是
(2)反应②的实验中用到Cu丝,其作用是作
(3)反应③的反应类型属于
您最近一年使用:0次
【推荐2】乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。
(1)乙烯的电子式为_______ ,属于_______ 分子(填“极性”或“非极性”)。
(2)仅用下列物质能除去甲烷中的杂质乙烯的试剂是_______ (填序号)。
a.稀硫酸 b.溴的四氯化碳溶液 c.水 d.酸性高锰酸钾溶液
(3)下列物质中,不能通过乙烯加成反应得到的是_______(填序号)。
(4)已知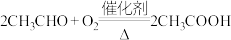 。若以乙烯为主要原料合成乙酸,其合成路线如下图所示:
。若以乙烯为主要原料合成乙酸,其合成路线如下图所示:_______ 。
(5)工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为_______ ,反应类型是_______ 。
(1)乙烯的电子式为
(2)仅用下列物质能除去甲烷中的杂质乙烯的试剂是
a.稀硫酸 b.溴的四氯化碳溶液 c.水 d.酸性高锰酸钾溶液
(3)下列物质中,不能通过乙烯加成反应得到的是_______(填序号)。
A. | B.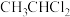 | C. | D. |
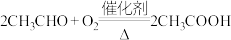 。若以乙烯为主要原料合成乙酸,其合成路线如下图所示:
。若以乙烯为主要原料合成乙酸,其合成路线如下图所示: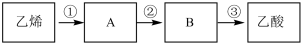
(5)工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】乙烯是来自石油的重要有机化工原料。结合路线回答:
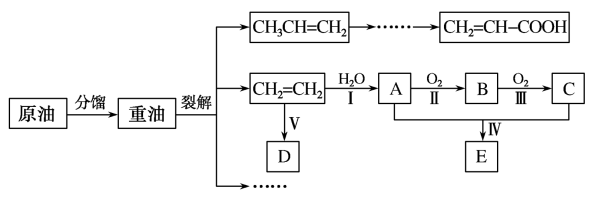
(1)产物CH2=CH−COOH中官能团的名称为___________ 。反应Ⅰ的化学方程式为___________ 。
(2)D是高分子,用来制造包装材料,则反应V类型是___________ 。产物CH2=CHCOOH也能发生相同类型的化学反应,其化学方程式为:___________ 。
(3)E有香味,实验室用A和C反应来制取E。
①反应IV的化学方程式是___________ 。该反应中的浓硫酸的作用是___________ 。
②实验室制取E时在试管里加入试剂的顺序是___________ (填以下字母序号)。
a.先浓硫酸再A后C b.先浓硫酸再C后A c.先A再浓硫酸后C
③实验中用到饱和碳酸钠溶液,其作用是___________ 。
(4)①A是乙醇,与A相对分子质量相等且元素种类相同的有机物的结构简式是:___________ 。
②为了研究乙醇的化学性质,利用如图装置在D处进行乙醇的催化氧化实验,并检验其产物,其中C装置的试管中盛有无水乙醇。(加热、固定和夹持装置已略去)
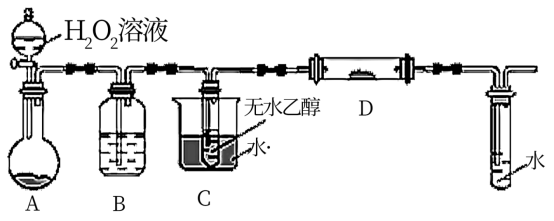
装置A圆底烧瓶内的固体物质是___________ ,C装置的实验条件是___________ 。实验时D处装有铜粉,D中发生的主要反应的化学方程式为___________

(1)产物CH2=CH−COOH中官能团的名称为
(2)D是高分子,用来制造包装材料,则反应V类型是
(3)E有香味,实验室用A和C反应来制取E。
①反应IV的化学方程式是
②实验室制取E时在试管里加入试剂的顺序是
a.先浓硫酸再A后C b.先浓硫酸再C后A c.先A再浓硫酸后C
③实验中用到饱和碳酸钠溶液,其作用是
(4)①A是乙醇,与A相对分子质量相等且元素种类相同的有机物的结构简式是:
②为了研究乙醇的化学性质,利用如图装置在D处进行乙醇的催化氧化实验,并检验其产物,其中C装置的试管中盛有无水乙醇。(加热、固定和夹持装置已略去)

装置A圆底烧瓶内的固体物质是
您最近一年使用:0次

 溶液的试管中逐滴滴加少量的
溶液的试管中逐滴滴加少量的 溶液,可观察到的现象是
溶液,可观察到的现象是 所属的物质类别是
所属的物质类别是

