硫酸工业尾气中的SOj是常见的大气污染物,可通过以下几种方式变废为宝:
(1)电化学处理法:硫酸工业尾气中的SO2经分离后,可用于制备硫酸,同时获得电能,装置如图所示(电极均为惰性材料)写出N极发生的电极反应式________________________ ;溶液中的阳离子向______ 极(M或N)移动,标准状况下,当有22.4LSO2参加反应时,溶液中有________ mol阳离子向该极移动。

(2)钠碱循环法:用Na2SO3溶液作为吸收液来吸收SO2,尾气通入1mol/L的Na2SO3溶液中,①当溶液的PH约为6时,Na2SO3溶液吸收SO2的能力显著下降,此时溶液中c (SO32-)的浓度是0.2mol/L,则此时溶液中离子浓度由大到小的顺序为_______________ 。
②当溶液的PH降至约为6时,需送至电解槽再生,再生示意图如下:
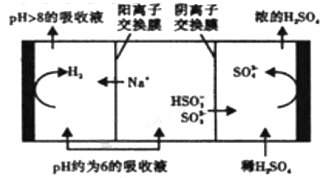
HSO3-在阳极放电的电极反应式是______________________________ 。
当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理:___________ 。
(1)电化学处理法:硫酸工业尾气中的SO2经分离后,可用于制备硫酸,同时获得电能,装置如图所示(电极均为惰性材料)写出N极发生的电极反应式

(2)钠碱循环法:用Na2SO3溶液作为吸收液来吸收SO2,尾气通入1mol/L的Na2SO3溶液中,①当溶液的PH约为6时,Na2SO3溶液吸收SO2的能力显著下降,此时溶液中c (SO32-)的浓度是0.2mol/L,则此时溶液中离子浓度由大到小的顺序为
②当溶液的PH降至约为6时,需送至电解槽再生,再生示意图如下:

HSO3-在阳极放电的电极反应式是
当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理:
更新时间:2017-09-02 13:15:48
|
【知识点】 化学反应原理综合考查解读
相似题推荐
填空题
|
适中
(0.65)
【推荐1】实验测得反应溶液的pH、温度对铁黄产率的影响如图所示。反应温度宜选择___________ ;pH大于4.5时铁黄产率降低的主要原因可能是___________ 。


您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】 氢氟酸是一种弱酸,可用来刻蚀玻璃。已知
氢氟酸是一种弱酸,可用来刻蚀玻璃。已知 时
时

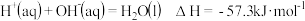
氢氟酸电离的热化学方程式可表示为___________________________________________ ;
氟化氢电离过程“放热”,其主要原因可能是____________________________________ 。
 已知
已知 的第二级电离常数
的第二级电离常数 ,HClO的电离常数
,HClO的电离常数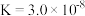
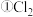 与水反应的化学平衡常数表达式为
与水反应的化学平衡常数表达式为_________________________________________ ;
写出下列条件下所发生反应的离子方程式:
 少量
少量 通入到过量的
通入到过量的 溶液中:
溶液中:_________________________________________ ;
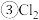 与
与 按物质的量之比
按物质的量之比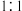 恰好反应:
恰好反应:__________________________________ ;
 少量
少量 通入到过量的NaClO溶液中:
通入到过量的NaClO溶液中:_________________________________________ 。
 氢氟酸是一种弱酸,可用来刻蚀玻璃。已知
氢氟酸是一种弱酸,可用来刻蚀玻璃。已知 时
时 
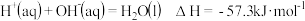
氢氟酸电离的热化学方程式可表示为
氟化氢电离过程“放热”,其主要原因可能是
 已知
已知 的第二级电离常数
的第二级电离常数 ,HClO的电离常数
,HClO的电离常数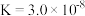
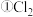 与水反应的化学平衡常数表达式为
与水反应的化学平衡常数表达式为写出下列条件下所发生反应的离子方程式:
 少量
少量 通入到过量的
通入到过量的 溶液中:
溶液中: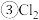 与
与 按物质的量之比
按物质的量之比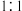 恰好反应:
恰好反应: 少量
少量 通入到过量的NaClO溶液中:
通入到过量的NaClO溶液中:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】纳米级Cu2O由于具有优良的催化性能而受到科学家的不断关注,下列为制取Cu2O的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是_________________________ 。
(2)方法Ⅱ利用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为______________________________ ;电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解,通过离子交换膜的阴离子的物质的量为________ mol。(离子交换膜只允许OH-通过)
(3)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制的Cu(OH)2来制备纳米级Cu2O,同时放出N2。生成1molN2时,生成Cu2O的物质的量为________________ 。
(4)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。写出肼-空气燃料电池放电时负极的电极反应式:___________________________ 。
| 方法Ⅰ | 用碳粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法,原理为2Cu+H2O Cu2O+H2↑ Cu2O+H2↑ |
| 方法Ⅲ | 用肼(N2H4)还原新制的Cu(OH)2 |
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是
(2)方法Ⅱ利用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为

(3)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制的Cu(OH)2来制备纳米级Cu2O,同时放出N2。生成1molN2时,生成Cu2O的物质的量为
(4)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。写出肼-空气燃料电池放电时负极的电极反应式:
您最近一年使用:0次



